甲、乙、丙三种固体物质在水中的溶解度曲线如图所示。请回答:
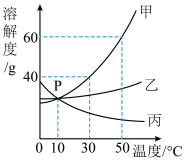
(1)图中P点的意义是____________________________ 。
(2)若甲中混有少量的乙,最好采用_______________ 的方法提纯甲。
(3)使30℃接近饱和的甲溶液变成该温度下的饱和溶液,可采用的一种方法是___ 。
(4)使50℃甲、乙、丙三种物质的饱和溶液降温到10℃,则其溶质质量分数不变的是_________ 。
(5)向100g 50℃的水中加入65g甲固体,发现全部溶解,一段时间后又有部分甲的晶体析出。你认为“全部溶解”的原因可能是__________________________ 。

(1)图中P点的意义是
(2)若甲中混有少量的乙,最好采用
(3)使30℃接近饱和的甲溶液变成该温度下的饱和溶液,可采用的一种方法是
(4)使50℃甲、乙、丙三种物质的饱和溶液降温到10℃,则其溶质质量分数不变的是
(5)向100g 50℃的水中加入65g甲固体,发现全部溶解,一段时间后又有部分甲的晶体析出。你认为“全部溶解”的原因可能是
更新时间:2016-11-28 12:20:22
|
相似题推荐
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】甲、乙两种固体的溶解度曲线如图所示。

甲、乙溶解度相等时的温度为______ ℃﹔若甲中混有少量乙,可用_______ (填“降温”或“蒸发”)结晶的方法提纯甲;t2℃时将75g甲的饱和溶液与50g水充分混合后,所得溶液溶质质量分数为_______ 。

甲、乙溶解度相等时的温度为
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】如图为甲、乙两种固体的溶解度曲线,请据图回答问题:
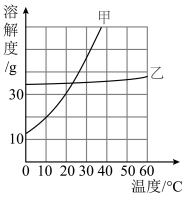
(1)20℃时,甲的溶解度为30g。20℃时,在50g水中加入50g甲,充分搅拌后形成溶液的质量为______ g。
(2)甲中混有少量乙杂质,可用______ 的方法提纯甲。

(1)20℃时,甲的溶解度为30g。20℃时,在50g水中加入50g甲,充分搅拌后形成溶液的质量为
(2)甲中混有少量乙杂质,可用
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】1.分析处理图表中的信息是学习化学的一种重要方法。
(1)下表是KNO3、NaCl在不同温度下的溶解度(单位:g/100g水)
Ⅰ.20℃时,NaCl的溶解度是___________ g。
Ⅱ.30℃时,KNO3溶液的最大浓度(溶质质量分数)为___________ (只列计算式,不需要计算结果)。
Ⅲ.KNO3 中含少量氯化钠时,提纯硝酸钾的一般方法是___________ 。
Ⅳ.根据表内数据可知,KNO3和NaCl在某一温度时具有相同的溶解度X,则X的取值范围是___________ 。
(2)如下图是对20℃一定质量的甲的溶液进行恒温蒸发结晶的实验过程,请回答.

Ⅰ.蒸发前原溶液是___________ (填“饱和”或“不饱和”)溶液,n的数值是___________ 。
Ⅱ.依据上述实验,你认为甲的溶解度随温度变化的趋势是___________ (填字母)。
A.随温度升高而增大 B.随温度升高而减小 C.无法判断
(1)下表是KNO3、NaCl在不同温度下的溶解度(单位:g/100g水)
| 温度(℃) | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 | 100 |
| KNO3 | 13.3 | 20.9 | 32 | 45.8 | 64 | 85.5 | 110 | 138 | 169 | 202 | 246 |
| NaCl | 35.7 | 35.8 | 36 | 36.3 | 36.6 | 37 | 37.3 | 37.8 | 38.4 | 39 | 39.8 |
Ⅱ.30℃时,KNO3溶液的最大浓度(溶质质量分数)为
Ⅲ.KNO3 中含少量氯化钠时,提纯硝酸钾的一般方法是
Ⅳ.根据表内数据可知,KNO3和NaCl在某一温度时具有相同的溶解度X,则X的取值范围是
(2)如下图是对20℃一定质量的甲的溶液进行恒温蒸发结晶的实验过程,请回答.

Ⅰ.蒸发前原溶液是
Ⅱ.依据上述实验,你认为甲的溶解度随温度变化的趋势是
A.随温度升高而增大 B.随温度升高而减小 C.无法判断
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
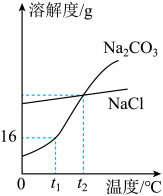
【推荐1】我国著名化学家侯德榜先生创立了联合制碱法,促进了世界制碱技术的发展。Na2CO3和NaCl的溶解度曲线如图所示,试回答下列问题:______ (填最简整数比)。
(2)将t2℃时相同质量的Na2CO3饱和溶液和NaCl饱和溶液均降温至 t1℃,此时所得两溶液溶质质量分数相比较______ 大(溶质化学式)。
(3)Na2CO3中混有少量NaCl时。可用______ 物理方法提纯Na2CO3。
(2)将t2℃时相同质量的Na2CO3饱和溶液和NaCl饱和溶液均降温至 t1℃,此时所得两溶液溶质质量分数相比较
(3)Na2CO3中混有少量NaCl时。可用
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】甲、乙两种固体(均不含结晶水)的溶解度曲线如图2所示,请回答下列问题:

(1)t3℃时,乙的溶解度是___________ g。
(2)t3℃时,甲形成的饱和溶液中溶质与溶液的质量比为___________ 。
(3)t3℃时,将15克乙物质加入到50克水中,充分溶解后,所得溶液的质量是___________ g。
(4)若甲的饱和溶液中含有少量乙,提纯甲的方法是___________ 。
(5)t1℃,把等质量甲、乙两种物质分别放入两只烧杯中,加入100g水,充分搅拌,溶解情况如图1所示,则B烧杯内溶质是___________ (填“甲”或“乙”)。现对图1中两烧杯内物质同时作如下处理,有关说法正确的是___________ 。
A.升温至t2℃,均形成不饱和溶液
B.升温至t2℃,所得溶液中溶质的质量分数相同
C.先升温至t3℃,再通过恒温蒸发溶剂的方法使两溶液均刚好达到饱和,蒸发水的质量:烧杯A=烧杯B

(1)t3℃时,乙的溶解度是
(2)t3℃时,甲形成的饱和溶液中溶质与溶液的质量比为
(3)t3℃时,将15克乙物质加入到50克水中,充分溶解后,所得溶液的质量是
(4)若甲的饱和溶液中含有少量乙,提纯甲的方法是
(5)t1℃,把等质量甲、乙两种物质分别放入两只烧杯中,加入100g水,充分搅拌,溶解情况如图1所示,则B烧杯内溶质是
A.升温至t2℃,均形成不饱和溶液
B.升温至t2℃,所得溶液中溶质的质量分数相同
C.先升温至t3℃,再通过恒温蒸发溶剂的方法使两溶液均刚好达到饱和,蒸发水的质量:烧杯A=烧杯B
您最近一年使用:0次
【推荐3】(1)根据图中提供的信息,请回答下列问题:

①由图1可知,钙的相对原子质量为____________ ,x=_____________ 。
②图2中与钙元素化学性质相似的是___________ 。
③ABC中位于同周期的是___________ 。
(2)某固态物质的溶解度曲线如图所示。

①若将B点状态溶液变化为A点,简单的实验操作为___________ 。
②取用某一温度下的该固态物质饱和溶液时,下列物理量不随所取溶液体积的多少而变化的是_______ (填字母标号)。
A溶液中溶质的质量
B溶液的质量
C溶液的溶质质量分数
D溶液的密度
③t1℃时,向100g水中加入30g该物质充分溶解,溶液质量为__________ 。

①由图1可知,钙的相对原子质量为
②图2中与钙元素化学性质相似的是
③ABC中位于同周期的是
(2)某固态物质的溶解度曲线如图所示。

①若将B点状态溶液变化为A点,简单的实验操作为
②取用某一温度下的该固态物质饱和溶液时,下列物理量不随所取溶液体积的多少而变化的是
A溶液中溶质的质量
B溶液的质量
C溶液的溶质质量分数
D溶液的密度
③t1℃时,向100g水中加入30g该物质充分溶解,溶液质量为
您最近一年使用:0次
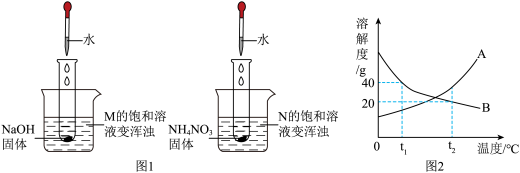
【推荐1】为探究固体物质溶解的热现象及温度对物质溶解度的影响,某老师设计了如下实验:将NaOH固体和NH4NO3固体分别加入两支试管中,向两支试管中分别滴加适量水,如图1所示,M、N两种固体物质的溶解度曲线如图2所示。则N的溶解度曲线为___________ (填“A”或“B”);若N的饱和溶液中有少量的M,可以用___________ 的方法提纯N;若在t2℃时,B曲线所代表的物质的42g饱和溶液降温至t1℃,需要再加入___________ g固体才能使溶液达到饱和。

您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
真题
【推荐2】甲、乙、丙三种固体(均不含结晶水)的溶解度曲线如图所示,请回答下列问题:
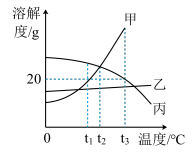
(1)t2℃时,甲、乙、丙三种物质溶解度大小关系是____
(2)t3℃时,将20g物质丙加入50g水中充分溶解,所得溶液的质量为_____ g.
(3)在不改变溶质质量分数的前提下,将甲的不饱和溶液转化为饱和溶液的方法是_____
(4)下列说法正确的是_____
A 甲中混有少量乙时,可用降温结晶的方法提纯甲;
B t2℃时,甲、丙两物质饱和溶液中所含溶质质量相等;
C 将t3℃时的甲、丙的饱和溶液降低温度至t2℃,溶质的质量分数相等;
D t1℃时,用甲、乙、丙三种固体配制等质量的饱和溶液,所需水的质量大小关系是乙>甲>丙。

(1)t2℃时,甲、乙、丙三种物质溶解度大小关系是
(2)t3℃时,将20g物质丙加入50g水中充分溶解,所得溶液的质量为
(3)在不改变溶质质量分数的前提下,将甲的不饱和溶液转化为饱和溶液的方法是
(4)下列说法正确的是
A 甲中混有少量乙时,可用降温结晶的方法提纯甲;
B t2℃时,甲、丙两物质饱和溶液中所含溶质质量相等;
C 将t3℃时的甲、丙的饱和溶液降低温度至t2℃,溶质的质量分数相等;
D t1℃时,用甲、乙、丙三种固体配制等质量的饱和溶液,所需水的质量大小关系是乙>甲>丙。
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】在t℃时,分别取甲、乙两种固体的溶液,恒温蒸发水分,得到蒸发水的质量(X)与析出晶体质量(Y)的关系如图所示(析出的晶体不含结晶水)。
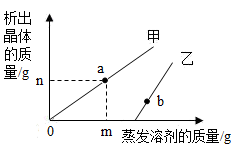
(1)t℃时,在0点乙的溶液是_______ 溶液(填“饱和”或“不饱和”)。
(2)t℃时,甲、乙的溶解度大小关系为:甲___ 乙(填“<”>”或“=”)。
(3)t℃时,甲的溶解度为_____ (用含m、n的代数式表示)。
(4)下列说法不正确的是 (填序号)。

(1)t℃时,在0点乙的溶液是
(2)t℃时,甲、乙的溶解度大小关系为:甲
(3)t℃时,甲的溶解度为
(4)下列说法不正确的是 (填序号)。
| A.甲、乙两种物质的溶解度都随温度升高而变大 |
| B.根据m、n可计算出:t℃时甲的饱和溶液中溶质的质量分数 |
| C.t℃时在甲、乙的饱和溶液中分别蒸发等量的水,析出晶体的质量:甲>乙 |
| D.t℃时用甲饱和溶液和水配制50g一定浓度的稀溶液时,量取甲溶液时仰视读数,则会使溶液浓度偏大 |
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐1】如图是甲、乙两种物质的溶解度曲线,请回答:

(1)t3℃时,两种物质溶解度的大小关系为甲__ 乙;(填“大于”、“小于”或“等于”)
(2)t3℃时,把30g固体甲放入50g水中,充分溶解后可得到甲的溶液_____ g;
(3)在其他条件不变的情况下,若把t1℃时甲、乙的饱和溶液分别升温至t2℃,此时两种溶液中溶质的质量分数关系为甲__ 乙(选填:>、<或=)。

(1)t3℃时,两种物质溶解度的大小关系为甲
(2)t3℃时,把30g固体甲放入50g水中,充分溶解后可得到甲的溶液
(3)在其他条件不变的情况下,若把t1℃时甲、乙的饱和溶液分别升温至t2℃,此时两种溶液中溶质的质量分数关系为甲
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】如图是甲、乙、丙三种物质的溶解度曲线。现有甲、乙、丙三种物质的饱和溶液(无固体存在),请根据如图回答:
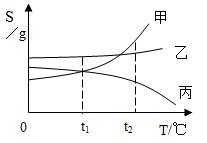
(1)t1℃时,甲、乙、丙三者的溶解度关系为______ ;
(2)t2℃时,乙的溶解度为60g,将甲、乙、丙的固体各25g分别加入50g水中充分溶解后,能形成饱和溶液的是______ ;
(3)将t2℃时甲、乙、丙三种物质饱和溶液的温度降低到t 1℃时,三种溶液中溶质的质量分数由大到小的关系是______ 。

(1)t1℃时,甲、乙、丙三者的溶解度关系为
(2)t2℃时,乙的溶解度为60g,将甲、乙、丙的固体各25g分别加入50g水中充分溶解后,能形成饱和溶液的是
(3)将t2℃时甲、乙、丙三种物质饱和溶液的温度降低到t 1℃时,三种溶液中溶质的质量分数由大到小的关系是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐3】t2°C时,将甲、乙各90 g分别加到盛有110 g水的两只烧杯中,充分溶解后,恢复到t2°C,现象如图一。甲和乙的溶解度曲线如图二。请回答下列问题:
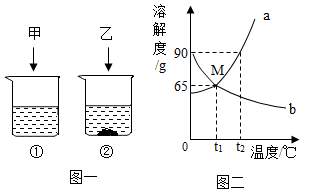
(1)M点的含义是____________ 。
(2)固体甲对应的溶解度曲线是____ (填“a”或“b”)。
(3)向烧杯①中加入___ g水,可得到溶质质量分数为30%的溶液。
(4)将甲、乙t2°C时的饱和溶液分别降温到t1°C时,有关说法正确的是___ (填序号)。
A 甲溶液一定是饱和溶液 B 乙溶液一定是饱和溶液
C 两溶液的溶质质量相等 D 两溶液溶质质量分数相等

(1)M点的含义是
(2)固体甲对应的溶解度曲线是
(3)向烧杯①中加入
(4)将甲、乙t2°C时的饱和溶液分别降温到t1°C时,有关说法正确的是
A 甲溶液一定是饱和溶液 B 乙溶液一定是饱和溶液
C 两溶液的溶质质量相等 D 两溶液溶质质量分数相等
您最近一年使用:0次



