某钢铁厂实验室为测定赤铁矿中Fe2O3%的含量,将矿石粉碎(其中杂质既不溶于水也不与酸反应),进行如下实验:
(1)上述实验过程中发生反应的化学方程式为______ 。
(2)样品中Fe2O3的质量分数是______ 。
(3)若向最终滤液中加入l6g水,所得不饱和溶液中溶质的质量分数为______ 。
(4)若用溶质质量分数为98%的浓硫酸配制实验所需的稀硫酸,则所需浓硫酸与水的质量最简比为______ ;配制溶液时所需的实验仪器有烧杯、量筒和______ (填选项字母):
A.铁架台 B.玻璃棒 C.漏斗 D.胶头滴管
(5)该钢铁厂每天用上述赤铁矿石1900t来生产生铁,则理论上日产含杂质5%的生铁的质量为______ 。
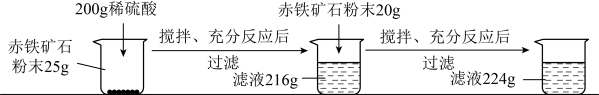
(1)上述实验过程中发生反应的化学方程式为
(2)样品中Fe2O3的质量分数是
(3)若向最终滤液中加入l6g水,所得不饱和溶液中溶质的质量分数为
(4)若用溶质质量分数为98%的浓硫酸配制实验所需的稀硫酸,则所需浓硫酸与水的质量最简比为
A.铁架台 B.玻璃棒 C.漏斗 D.胶头滴管
(5)该钢铁厂每天用上述赤铁矿石1900t来生产生铁,则理论上日产含杂质5%的生铁的质量为
2024·黑龙江哈尔滨·二模 查看更多[3]
2024年黑龙江省哈尔滨市南岗区虹桥初级中学中考二模理化综合试卷-初中化学2024年黑龙江省哈尔滨市虹桥中学九年级下学期(二模)化学试卷 (已下线)押深圳卷第16题 综合化学计算题-备战2024年中考化学临考题号押题(深圳专用)
更新时间:2024-05-06 11:03:08
|
相似题推荐
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】I.硅胶是常用的一种干燥剂。利用氯化钴含有不同数目的结晶水呈现不同颜色的性质,在制备硅胶时加入一些氯化钴得到变色硅胶。用CoCl2·xH2O 表示含结晶水的氯化钴。试计算:
(1)若其中一种含结晶水的氯化钴的相对分子质量为 238,则 x=________ ,该结晶水合物中的氯、氧原子个数比为________ ;
(2)若 x=2,则氧元素的质量分数为________ (计算结果精确到 0.1%)。
II.“蛟龙号”是我国研制出的大深度载人潜水器。为保证载人潜水器长时间潜水,需要在潜水器里配备供氧装置。
(3)过氧化物供氧是一种常见的供氧技术,原理是用过氧化钠(化学式为 Na2O2)固体常温下与二氧化碳反应,生成碳酸钠和氧气。若用这种方法制取 96g 氧气,则至少需要含过氧化钠 60%的过氧化钠样品多少克?(要有计算过程,反应的化学方程式为: )
)
(1)若其中一种含结晶水的氯化钴的相对分子质量为 238,则 x=
(2)若 x=2,则氧元素的质量分数为
II.“蛟龙号”是我国研制出的大深度载人潜水器。为保证载人潜水器长时间潜水,需要在潜水器里配备供氧装置。
(3)过氧化物供氧是一种常见的供氧技术,原理是用过氧化钠(化学式为 Na2O2)固体常温下与二氧化碳反应,生成碳酸钠和氧气。若用这种方法制取 96g 氧气,则至少需要含过氧化钠 60%的过氧化钠样品多少克?(要有计算过程,反应的化学方程式为:
 )
)
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】某同学在实验室中将31.6克的高锰酸钾放在试管中加热一段时间后,冷却,称得试管中剩余固体的质量为28.4克。
(1)大家纷纷猜想所得固体物质的成分:
猜想一:锰酸钾和二氧化锰;猜想二(写化学式): 。
(2)实验中生成氧气质量是 克。
(3)试通过计算参加反应的高锰酸钾质量来确定哪一种猜想是正确的。
(1)大家纷纷猜想所得固体物质的成分:
猜想一:锰酸钾和二氧化锰;猜想二(写化学式): 。
(2)实验中生成氧气质量是 克。
(3)试通过计算参加反应的高锰酸钾质量来确定哪一种猜想是正确的。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐3】请回答下列问题。
(1)如图为某钙片标签上的部分文字,请仔细阅读后回答下列问题。
维生素D2的化学式为C28H44O,试计算:
①维生素D2中碳、氢、氧三种元素的质量比为____ 。
②每克钙片中含碳酸钙(CaCO3)的质量为_____ (其他成分不含钙)。
(2)在实验室加热32.5g二氧化锰和氯酸钾的固体混合物制取氧气时,剩余固体物质的质量变化如图所示。请计算:

①完全反应时,生成氧气的质量为____ g。
②混合物中氯酸钾的质量是____ g。(写出计算过程)
(1)如图为某钙片标签上的部分文字,请仔细阅读后回答下列问题。
| 【主要原料】碳酸钙、维生素D 【功效成分】补钙 |
| 每片含钙(以Ca计)500mg、维生D100ug 【食用方法】每日一次,每次一片 【规格】2.5g/片 |
①维生素D2中碳、氢、氧三种元素的质量比为
②每克钙片中含碳酸钙(CaCO3)的质量为
(2)在实验室加热32.5g二氧化锰和氯酸钾的固体混合物制取氧气时,剩余固体物质的质量变化如图所示。请计算:

①完全反应时,生成氧气的质量为
②混合物中氯酸钾的质量是
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】如表是硝酸钾在不同温度时的溶解度,根据表中数据回答下列问题。

(1)10℃时,100克水中最多可溶解硝酸钾的质量为___________克。
(2)20℃时,将10克硝酸钾加入40克水中,所得溶液溶质质量分数为___________。
(3)如图是硝酸钾溶液的变化情况,请写出两种可采用的操作方法___________。(写出计算过程)

| 温度/℃ | 0 | 10 | 20 | 30 | 40 |
| 溶解度/g | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 |
(1)10℃时,100克水中最多可溶解硝酸钾的质量为___________克。
(2)20℃时,将10克硝酸钾加入40克水中,所得溶液溶质质量分数为___________。
(3)如图是硝酸钾溶液的变化情况,请写出两种可采用的操作方法___________。(写出计算过程)
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】计算
(1)用质量分数为10%的氢氧化钠溶液配制5%的氢氧化钠溶液200g,需要水______ g。
(2)取160g溶质质量分数为5%的NaOH溶液中和146g的稀盐酸,恰好完全反应,所得溶液中溶质的质量分数是多少(结果精确到0.1%)(化学方程式: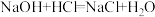 )
)
(1)用质量分数为10%的氢氧化钠溶液配制5%的氢氧化钠溶液200g,需要水
(2)取160g溶质质量分数为5%的NaOH溶液中和146g的稀盐酸,恰好完全反应,所得溶液中溶质的质量分数是多少(结果精确到0.1%)(化学方程式:
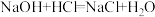 )
)
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐3】为了测定某含杂质5%的黄铜样品中铜的质量分数(杂质中不含铜、锌元素,杂质不溶于水,不与其它物质反应,受热也不分解),某化学小组进行了如下实验:
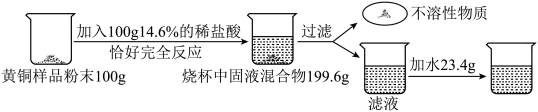
(1)配制上述质量分数为14.6%的稀盐酸,需质量分数为36.5%的浓盐酸质量是_ ;
(2)发生反应的化学方程式为___________________;
(3)根据已知条件列出求解100g该黄铜样品中锌的质量(x)的比例式为_____ ;
(4)该黄铜样品中铜的质量分数是__________ ;
(5)向过滤后所得滤液中加入23.4g水,则最终所得溶液中溶质的质量分数是___ 。

(1)配制上述质量分数为14.6%的稀盐酸,需质量分数为36.5%的浓盐酸质量是_ ;
(2)发生反应的化学方程式为___________________;
(3)根据已知条件列出求解100g该黄铜样品中锌的质量(x)的比例式为_____ ;
(4)该黄铜样品中铜的质量分数是__________ ;
(5)向过滤后所得滤液中加入23.4g水,则最终所得溶液中溶质的质量分数是___ 。
您最近一年使用:0次
计算题
|
适中
(0.65)
真题
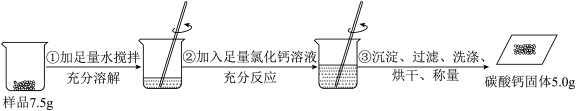
【推荐1】某碳酸钠样品中混有少量氯化钠,根据如图所示信息计算该样品中碳酸钠的质量分数。(计算结果精确到0.1%)(反应的化学方程式:CaCl2+Na2CO3===CaCO3↓+2NaCl)

您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐2】在一次实验课上,同学们取50g过氧化氢溶液与2g二氧化锰混合制取氧气,充分反应后,测得剩余液体的质量是48.4g。请计算该过氧化氢溶液中溶质的质量分数。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐3】某造纸厂在生成过程中会产生含有氢氧化钠的废水,需经处理至中性后才能排放。现要处理含有20kg氢氧化钠的废水,理论上需要质量分数为5%的稀盐酸的质量是多少?
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】小明在协助老师清理实验储备室,发现了一瓶存放多年的氢氧化钙,为检 验 其变质情况,进行如下探究:取氢氧化钙样品11.4g 于锥形瓶中,加入38.6g的水,然后逐滴滴加14.6%的稀盐酸,加入稀盐酸的质量与锥形瓶中物质的质量关系如图所示,请问:

(1)与氢氧化钙反应的稀盐酸溶液的质量为______g
(2)计算11.4g该样品中氢氧化钙的质量。
(3)根据计算所得数据画出生成CO2的质量曲线(并进行必要的标注)


(1)与氢氧化钙反应的稀盐酸溶液的质量为______g
(2)计算11.4g该样品中氢氧化钙的质量。
(3)根据计算所得数据画出生成CO2的质量曲线(并进行必要的标注)

您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】实验室测定一瓶稀硫酸中溶质的质量分数,取10g该待测液,向其中逐滴加入溶质质量分数为8%的氢氧化钠溶液,加入氢氧化钠溶液的质量与溶液pH的变化关系如图所示。请根据题意填空并计算:

(1)A点对应的溶液中含有的溶质是___________(填化学式);
(2)20g8%的氢氧化钠溶液中所含溶质的质量是___________;
(3)计算待测液中溶质的质量分数(写计算过程)。

(1)A点对应的溶液中含有的溶质是___________(填化学式);
(2)20g8%的氢氧化钠溶液中所含溶质的质量是___________;
(3)计算待测液中溶质的质量分数(写计算过程)。
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】实验室有一包黑色粉末,已知主要成分是氧化铜,为测定黑色粉末中氧化铜的质量分数,化学兴趣小组同学做如下实验:在盛有200g稀硫酸的烧杯中加入一定量该黑色粉末,搅拌使其充分反应后过滤,再向所得滤液中第二次加入一定量该黑色粉末,再搅拌使其充分反应后再过滤,实验过程所得数据如下表(已知黑色粉末中含有的杂质既不溶于水,也不与稀硫酸反应):
请回答下列问题:
(1)该黑色粉末中氧化铜的质量分数为____________ 。
(2)计算上述所用稀硫酸的溶质质量分数是多少?
| 实验次数 | 第一次 | 第二次 |
| 黑色粉末 | 31.25g | 20g |
| 滤液 | 225g | 240g |
请回答下列问题:
(1)该黑色粉末中氧化铜的质量分数为
(2)计算上述所用稀硫酸的溶质质量分数是多少?
您最近一年使用:0次



