实验课上,老师给了同学们一包红色粉末,该粉末可能是铜粉和氧化铁粉末中的一种或两种,为确定该粉末的成分,同学们进行了如下探究:
【作出猜想】
(1)①铜粉;②_______ ;③铜粉和氧化铁粉末。
【进行实验】
(2)同学们取少量红色粉末于试管中,滴加足量的_______ (选填“氯化钠溶液”或“稀盐酸”)振荡,若观察到红色粉末逐渐减少,则说明猜想_______ 不正确。
(3)同学们又取红色粉末放入硬质玻璃管中(装置气密性良好,如图),先通一会CO,然后用酒精喷灯加热至充分反应后,停止加热并继续通入CO气体至玻璃管冷却。实验过程中观察到硬质玻璃管中的红色粉末全部变为_______ 且澄清石灰水变浑浊,则证明猜想②正确,写出硬质玻璃管内发生反应的化学方程式:_______ 。_______ 。
(5)上图中虚线框内的装置是用于吸收CO2并收集CO气体的,请从图中选择最合适的装置_______(填字母)。
【作出猜想】
(1)①铜粉;②
【进行实验】
(2)同学们取少量红色粉末于试管中,滴加足量的
(3)同学们又取红色粉末放入硬质玻璃管中(装置气密性良好,如图),先通一会CO,然后用酒精喷灯加热至充分反应后,停止加热并继续通入CO气体至玻璃管冷却。实验过程中观察到硬质玻璃管中的红色粉末全部变为
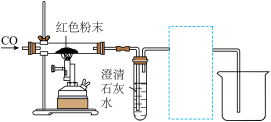
(5)上图中虚线框内的装置是用于吸收CO2并收集CO气体的,请从图中选择最合适的装置_______(填字母)。
A.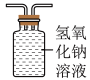 | B.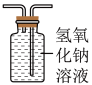 | C. |
更新时间:2024-05-09 15:36:02
|
相似题推荐
科学探究题
|
适中
(0.65)
解题方法
【推荐1】兴趣小组同学设计图8实验探究铁钉锈蚀的条件。
(1)一周后观察铁钉锈蚀最严重的试管是_______ (填试管编号),铁锈的成分主要是_______ 。
(2)生产生活中为防止汽车的铁制外壳锈蚀,可以采用的防锈方法是_______ 。
(3)铁钉生锈过程中,铁会与氧气、水共同作用,化合生成羟基氧化铁(FeOOH),该反应的化学方程式为_______ 。
(4)为了研究溶液中的不同离子对铁钉锈蚀速率的影响,同学们又设计如图1实验,用传感器测定的试管内氧气的体积分数变化如图2所示。
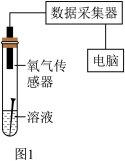
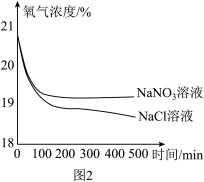
①依据图2的实验结果,要证明铁在空气中锈蚀需要氧气和水共同作用,可省略图8中的_______ (填实验编号)实验。
②由以上实验数据推知,溶液中NO3-加快铁钉锈蚀的能力_______ (填“强”或“弱)于C1-。
| 实验 |  |  | 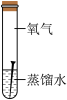 | 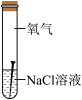 |
| 编号 | A | B | C | D |
(2)生产生活中为防止汽车的铁制外壳锈蚀,可以采用的防锈方法是
(3)铁钉生锈过程中,铁会与氧气、水共同作用,化合生成羟基氧化铁(FeOOH),该反应的化学方程式为
(4)为了研究溶液中的不同离子对铁钉锈蚀速率的影响,同学们又设计如图1实验,用传感器测定的试管内氧气的体积分数变化如图2所示。


①依据图2的实验结果,要证明铁在空气中锈蚀需要氧气和水共同作用,可省略图8中的
②由以上实验数据推知,溶液中NO3-加快铁钉锈蚀的能力
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐2】实现2030年碳达峰、2060年碳中和,是我国政府对国际社会的重要承诺。为此某小组对二氧化碳的来源、吸收以及低碳措施产生兴趣,开启了“低碳行动”项目化学习探究之旅。
任务一:探究二氧化碳的来源
(1)同学们通过调查发现,水泥生产过程中石灰石高温分解会生成两种氧化物,其中一种就是二氧化碳,试写出该反应的化学方程式___________________ 。
任务二:探究二氧化碳的吸收
(2)大气中CO2溶于水是自然界“碳循环”的重要环节。一位同学在实验室进行了模拟实验,如下图所示:
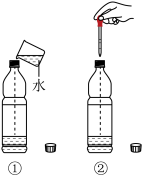
(3)请写出实验中发生反应的化学方程式___________________ 。
(4)小明同学认为步骤②还有待完善,请你补充一个对照实验___________________ 。
任务三:制定低碳行动措施
(5)生活中,良好的行为习惯也有助于完成低碳目标。请写出你在日常生活中的一种低碳行为___________________ 。
任务一:探究二氧化碳的来源
(1)同学们通过调查发现,水泥生产过程中石灰石高温分解会生成两种氧化物,其中一种就是二氧化碳,试写出该反应的化学方程式
任务二:探究二氧化碳的吸收
(2)大气中CO2溶于水是自然界“碳循环”的重要环节。一位同学在实验室进行了模拟实验,如下图所示:

| 实验步骤 | 实验现象 | 实验结论 |
| ①向充满二氧化碳的软塑料瓶中注入约1/3体积的蒸馏水,拧紧瓶盖后振荡。 | ||
| ②继续向瓶中滴加紫色石蕊溶液,振荡 | 二氧化碳能与水反应 |
(4)小明同学认为步骤②还有待完善,请你补充一个对照实验
任务三:制定低碳行动措施
(5)生活中,良好的行为习惯也有助于完成低碳目标。请写出你在日常生活中的一种低碳行为
您最近一年使用:0次
【推荐3】实验室新购进一批导线。标签显示导线外皮是聚氯乙烯(一种塑料)。同学们想对这批导线的外皮进行探究。初步认识:
(1)聚氯乙烯属于______材料。(填字母)
实验探究:取一小块导线外皮,点燃。闻到刺激性气味,同学们想了解产生此现象的原因,于是进行探究。
活动一:探究聚氯乙烯在充足的氧气中完全燃烧的产物
【查阅资料】①聚氯乙烯由C、H、Cl三种元素组成; ②无水CuSO4遇水由白变蓝;
③碱石灰为NaOH和CaO固体的混合物④氯气(Cl2)是一种黄绿色的有毒气体。
【实验分析】
(2)点燃酒精灯前,先通干燥的氧气目的是______ 。
(3)装置B中出现______ 现象,证明聚氯乙烯完全燃烧生成了水。C、D中产生白色沉淀,证明聚氯乙烯完全燃烧还产生了______ ,写出D中反应的化学方程式______ 。
【实验反思】
(4)下列有关上述探究活动的说法中,正确的是______(填字母)。
(5)聚氯乙烯燃烧有刺激性气味,因此,不能用焚烧的方法处理废弃塑料制品。请你写出一条防治“白色污染”的措施______ 。
(1)聚氯乙烯属于______材料。(填字母)
| A.无机材料 | B.合成材料 | C.复合材料 | D.金属材料 |
实验探究:取一小块导线外皮,点燃。闻到刺激性气味,同学们想了解产生此现象的原因,于是进行探究。
活动一:探究聚氯乙烯在充足的氧气中完全燃烧的产物
【查阅资料】①聚氯乙烯由C、H、Cl三种元素组成; ②无水CuSO4遇水由白变蓝;
③碱石灰为NaOH和CaO固体的混合物④氯气(Cl2)是一种黄绿色的有毒气体。

【实验分析】
(2)点燃酒精灯前,先通干燥的氧气目的是
(3)装置B中出现
【实验反思】
(4)下列有关上述探究活动的说法中,正确的是______(填字母)。
| A.装置B、C顺序不可颠倒,否则无法检验产生的H2O |
| B.将装置C中液体换作NaHCO3溶液,对实验结论无影响 |
| C.装置E的作用是防止空气中的CO2和H2O进入D,影响实验结果 |
(5)聚氯乙烯燃烧有刺激性气味,因此,不能用焚烧的方法处理废弃塑料制品。请你写出一条防治“白色污染”的措施
您最近一年使用:0次
科学探究题
|
适中
(0.65)
【推荐1】化学是以实验为基础的科学,实验是科学探究的重要手段。
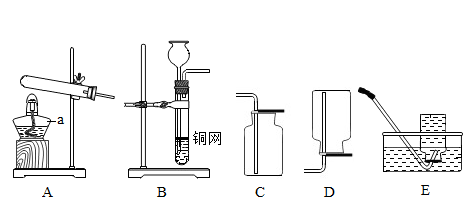
(1)如图是初中化学常见的仪器和装置,请回答下列问题。
①写出a的名称____________ ;②实验室选用装置A、E组合制取氧气,写出反应的化学方程式__________ ;③实验室用B、C装置制取二氧化碳时,若用铁丝网代替铜网,产生的后果是__________ 。
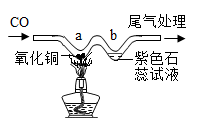
(2)如图所示,用“W”型玻璃管进行微型实验。
①b处发生的现象是_____________ ;②写出a处发生反应的化学方程式__________ ;③请简述该实验的尾气处理方法_____________ 。
(3)可燃冰(天然气水合物)是资源量丰富的高效清洁能源。科学家开采出一种可燃冰,取100g样品放置在一密闭容器内,该样品迅速转化为甲烷和水,将甲烷分离并完全燃烧,得到35.2g二氧化碳。求该可燃冰样品中甲烷的质量分数(精确到0.1%)_____ 。

(1)如图是初中化学常见的仪器和装置,请回答下列问题。
①写出a的名称

(2)如图所示,用“W”型玻璃管进行微型实验。
①b处发生的现象是
(3)可燃冰(天然气水合物)是资源量丰富的高效清洁能源。科学家开采出一种可燃冰,取100g样品放置在一密闭容器内,该样品迅速转化为甲烷和水,将甲烷分离并完全燃烧,得到35.2g二氧化碳。求该可燃冰样品中甲烷的质量分数(精确到0.1%)
您最近一年使用:0次
科学探究题
|
适中
(0.65)
【推荐2】某兴趣小组的同学对甲烷燃烧的产物产生了兴趣,设计如下实验进行探究:
【提出问题】甲烷燃烧后生成哪些物质?
【查阅资料】①含碳元素的物质完全燃烧生成 ,不完全燃烧生成
,不完全燃烧生成 ;
;
②白色无水 粉末遇水变蓝色。
粉末遇水变蓝色。
【猜想与假设】猜想一: 、
、 ; 猜想二:
; 猜想二: 、
、 ; 猜想三:
; 猜想三: 、
、 、
、
【实验探究】将甲烷在一定量的纯净氧气中燃烧的产物依次通过如图装置(部分夹持、固定装置省略)进行验证:
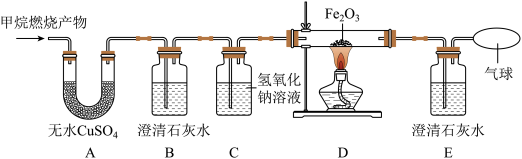
(1)实验过程中观察到 中白色粉末变为蓝色,
中白色粉末变为蓝色, 、
、 中澄清石灰水变浑浊,
中澄清石灰水变浑浊, 中红棕色粉末变成黑色,由此推断猜想
中红棕色粉末变成黑色,由此推断猜想______ 成立。
(2)实验过程中B装置的作用是______ ,C装置的作用是______ 。
(3)D装置中发生反应的化学方程式是______ 。
(4)实验过程中 、
、 装置的顺序不能颠倒,原因是
装置的顺序不能颠倒,原因是______ 。
【反思与交流】日常生活中使用含碳燃料一定要注意通风,防止______ 中毒。
【提出问题】甲烷燃烧后生成哪些物质?
【查阅资料】①含碳元素的物质完全燃烧生成
 ,不完全燃烧生成
,不完全燃烧生成 ;
;②白色无水
 粉末遇水变蓝色。
粉末遇水变蓝色。【猜想与假设】猜想一:
 、
、 ; 猜想二:
; 猜想二: 、
、 ; 猜想三:
; 猜想三: 、
、 、
、
【实验探究】将甲烷在一定量的纯净氧气中燃烧的产物依次通过如图装置(部分夹持、固定装置省略)进行验证:

(1)实验过程中观察到
 中白色粉末变为蓝色,
中白色粉末变为蓝色, 、
、 中澄清石灰水变浑浊,
中澄清石灰水变浑浊, 中红棕色粉末变成黑色,由此推断猜想
中红棕色粉末变成黑色,由此推断猜想(2)实验过程中B装置的作用是
(3)D装置中发生反应的化学方程式是
(4)实验过程中
 、
、 装置的顺序不能颠倒,原因是
装置的顺序不能颠倒,原因是【反思与交流】日常生活中使用含碳燃料一定要注意通风,防止
您最近一年使用:0次
科学探究题
|
适中
(0.65)
【推荐3】资料显示:炭还原四氧化三铁制得铁的温度在700℃-800℃。某校化学兴趣小组在探究用炭冶炼铁的原理的实验时,取一定质量的炭粉和四氧化三铁粉的混合物,在700℃-800℃的高温条件下使其充分反应,设计的实验装置如图:

(1)写出炭还原四氧化三铁的化学方程式_____ 。该实验中观察到的实验现象是:_____ 。对反应后试管中剩余的固体是什么,兴趣小组的同学做出了如下猜想:甲同学认为是铁粉,乙同学认为是炭粉和铁粉的混合物,丙同学的猜想_____ 。
(2)乙同学设计一个用化学方法证明自己的猜想是否正确,他的方法是_____ 。理由是_____ 。
(3)丙同学认为要验证自己的猜想是否正确可用磁铁去吸引,你认为丙同学的实验方案是否可行:_____ ,理由是_____ 。请你设计一个实验证明丙同学的猜想_____ 。

(1)写出炭还原四氧化三铁的化学方程式
(2)乙同学设计一个用化学方法证明自己的猜想是否正确,他的方法是
(3)丙同学认为要验证自己的猜想是否正确可用磁铁去吸引,你认为丙同学的实验方案是否可行:
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐1】某实验小组的同学用氢氧化钙和稀盐酸进行酸碱中和反应的实验时,向烧杯中的氢氧化钙溶液中滴加稀盐酸一会儿后,发现忘记了滴加指示剂。此时,他们停止滴加稀盐酸,并对烧杯内的溶质的成分进行探究。
(1)写出该中和反应的化学方程式:______ 。
(2)探究烧杯内溶液中溶质的成分。
[提出问题]该烧杯内的溶液中溶质是什么?
[猜想]猜想一:可能是CaCl2和Ca(OH)2;猜想二:可能只有CaCl2;猜想三:______ 。
[查阅资料]氯化钙溶液呈中性。
[进行实验]
实验步骤:取少量烧杯内溶液于试管中,滴入几滴酚酞溶液,振荡,实验现象:______ 。结论:猜想一不正确。
实验步骤:取少量烧杯内溶液于另一试管中,加入碳酸钠溶液至过量。实验现象:产生大量气泡。
结论:猜想二不正确,猜想三正确。
[反思与拓展]
(3)在分析化学反应后所得物质成分时,除考虑生成物外还需考虑______ 。
(4)根据所学化学知识,验证烧杯内溶液中的溶质含有 HCl,除以上方法外,下列哪些物质单独使用也能完成该实验?______(填序号)
(5)烧杯中的溶液未经处理直接倒入下水道,可能造成的危害是______ (写一条)。要处理烧杯内的溶液,使其溶质只含有CaCl2,应向烧杯中加入过量的______ 。
(1)写出该中和反应的化学方程式:
(2)探究烧杯内溶液中溶质的成分。
[提出问题]该烧杯内的溶液中溶质是什么?
[猜想]猜想一:可能是CaCl2和Ca(OH)2;猜想二:可能只有CaCl2;猜想三:
[查阅资料]氯化钙溶液呈中性。
[进行实验]
实验步骤:取少量烧杯内溶液于试管中,滴入几滴酚酞溶液,振荡,实验现象:
实验步骤:取少量烧杯内溶液于另一试管中,加入碳酸钠溶液至过量。实验现象:产生大量气泡。
结论:猜想二不正确,猜想三正确。
[反思与拓展]
(3)在分析化学反应后所得物质成分时,除考虑生成物外还需考虑
(4)根据所学化学知识,验证烧杯内溶液中的溶质含有 HCl,除以上方法外,下列哪些物质单独使用也能完成该实验?______(填序号)
| A.pH试纸 | B.铜 | C.紫色石蕊溶液 |
您最近一年使用:0次
科学探究题
|
适中
(0.65)
名校
解题方法
【推荐2】某化学小组在学习甲烷的性质时,发现甲烷与氢气、一氧化碳在性质上有很多相似之处。已知氢气和一氧化碳都具有还原性,那么甲烷有没有还原性呢?他们查阅相关资料后进行以下实验探究。
【查阅资料】无水硫酸铜是白色固体,遇水变蓝。

【实验过程】小组同学组装了上图装置,并进行实验。
C中反应的化学方程式为_______ 。
【交流讨论】实验开始时先通一段时间甲烷的目的是_______ ;D中气球的作用是_______ 。
【实验总结】利用甲烷还原氧化铁的化学方程式为_______ 。
【查阅资料】无水硫酸铜是白色固体,遇水变蓝。

【实验过程】小组同学组装了上图装置,并进行实验。
| 实验操作 | 实验现象 | 实验结论 |
| ①检查装置气密性后,先通入一会儿CH4气体,再点燃酒精灯,一段时间后 | 观察到B中 | 说明有水和CO2生成 |
| ②继续加热一段时间后 | 观察到A中硬质玻璃管中的固体粉末 | 说明硬质玻璃管中有 |
| ③取少量反应后的粉末于试管中,加入足量稀盐酸,充分反应 | 观察到有气泡产生,固体会部溶解,溶液由无色变成 |
【交流讨论】实验开始时先通一段时间甲烷的目的是
【实验总结】利用甲烷还原氧化铁的化学方程式为
您最近一年使用:0次
【推荐3】食品安全大于天,“双吸剂”是常用的袋装食品的保鲜剂,可用来吸收氧气、二氧化碳、水蒸气等气体。某化学小组的同学在袋装食品中发现一包 “双吸剂”的保鲜剂,其标签如图所示。同学们对这包久置的“双吸剂”的固体样品设计实验进行探究。
【收集资料】:
1.查阅资料:铁与氯化铁溶液在常温下生成氯化亚铁:Fe + 2FeCl3 = 3FeCl2
2.打开固体包装观察:部分粉末呈黑色、部分粉末呈白色、另有少数红棕色的块状固体。
【作出猜想】:
(1)久置固体中可能含有Fe、Fe2O3、CaO、Ca(OH)2、CaCO3。你猜想固体中可能含有Fe2O3的依据是:__________ 。
【实验探究】:
(2)如表是甲组同学设计并记录的实验报告,请你补充完整。
【实验质疑】:
(3)乙组同学认为甲组同学在实验中得出“一定不含有Fe2O3”的结论是错误的,理由是______ ;
(4)你认为甲组同学操作_______ 得出的结论也不合理(填:“一”或“二”或“四”),理由是(用化学方程式表示)_________ 。
【继续探究】:
(5)为验证固体中是否含有Fe2O3,乙组同学用_____ 先分离出铁粉,向残留固体中加入足量_______ (填名称),若溶液呈黄色,证明固体中含有Fe2O3。

【收集资料】:
1.查阅资料:铁与氯化铁溶液在常温下生成氯化亚铁:Fe + 2FeCl3 = 3FeCl2
2.打开固体包装观察:部分粉末呈黑色、部分粉末呈白色、另有少数红棕色的块状固体。
【作出猜想】:
(1)久置固体中可能含有Fe、Fe2O3、CaO、Ca(OH)2、CaCO3。你猜想固体中可能含有Fe2O3的依据是:
【实验探究】:
(2)如表是甲组同学设计并记录的实验报告,请你补充完整。
| 实验操作 | 实验现象 | 实验结论 |
| 一、取少量固体加入足量蒸馏水,搅拌溶解 | 固体部分溶解,并放出大量热 | 固体中一定含有 |
| 二、过滤,取滤液滴加无色酚酞试液 | 溶液变红色 | 固体中一定含有氢氧化钙 |
| 三、取滤渣加入足量稀盐酸 | 固体逐渐消失,产生大量无色气体,得到浅绿色溶液 | 固体中一定含有 |
| 四、将操作三中产生的气体通入到澄清石灰水中 | 澄清石灰水变浑浊 | 固体中一定含有 |
【实验质疑】:
(3)乙组同学认为甲组同学在实验中得出“一定不含有Fe2O3”的结论是错误的,理由是
(4)你认为甲组同学操作
【继续探究】:
(5)为验证固体中是否含有Fe2O3,乙组同学用
您最近一年使用:0次
科学探究题
|
适中
(0.65)
名校
解题方法
【推荐1】化学实验小组的同学将足量锌粒加入一定量浓硫酸中,发现有大量气泡产生。他们对此气体的成分进行了探究。
【提出问题】锌粒加入该硫酸溶液反应生成的气体是什么?
【查阅资料】
①浓硫酸能与锌反应,但不产生氢气,也不会产生氧气,能生成二氧化硫气体;
②二氧化硫气体有刺激性气味,易溶于水,能使品红(一种红色色素)溶液褪色。
【猜想与假设】
甲同学认为:气体可能是 ;
;
乙同学认为:气体可能是 ;
;
丙同学认为:气体还可能是_____ 。
【实验探究】
为了验证上述猜想,同学们在老师的指导下将产生的气体通过如下图的装置进行探究(部分夹持仪器略去)。

(1)实验开始后,观察到A中_____ 的现象,证明气体中含有 。
。
(2)C装置先通一段时间气体后,再点燃酒精灯。一段时间后观察到玻璃管内_____ 的现象,证明气体中含有 。
。
(3)D装置的作用是_____ 。
【实验结论】丙同学的猜想是正确的。
【反思与交流】
①锌和浓硫酸反应生成硫酸锌、水和二氧化硫,为什么反应过程中又产生了氢气呢?用文字简述原因:_____ 。
②锌与浓硫酸、稀硫酸反应都可以产生硫酸锌,如果需要制取硫酸锌,用锌与稀硫酸反应的优点是_____ (任填一种合理的答案)。
【提出问题】锌粒加入该硫酸溶液反应生成的气体是什么?
【查阅资料】
①浓硫酸能与锌反应,但不产生氢气,也不会产生氧气,能生成二氧化硫气体;
②二氧化硫气体有刺激性气味,易溶于水,能使品红(一种红色色素)溶液褪色。
【猜想与假设】
甲同学认为:气体可能是
 ;
;乙同学认为:气体可能是
 ;
;丙同学认为:气体还可能是
【实验探究】
为了验证上述猜想,同学们在老师的指导下将产生的气体通过如下图的装置进行探究(部分夹持仪器略去)。

(1)实验开始后,观察到A中
 。
。(2)C装置先通一段时间气体后,再点燃酒精灯。一段时间后观察到玻璃管内
 。
。(3)D装置的作用是
【实验结论】丙同学的猜想是正确的。
【反思与交流】
①锌和浓硫酸反应生成硫酸锌、水和二氧化硫,为什么反应过程中又产生了氢气呢?用文字简述原因:
②锌与浓硫酸、稀硫酸反应都可以产生硫酸锌,如果需要制取硫酸锌,用锌与稀硫酸反应的优点是
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐2】某化学兴趣小组在一个充满O2的密闭容器中加入一定量的纯净的碳粉,在高温条件下使其尽可能燃烧,待反应结束后,容器中的碳粉已完全消失。该小组对容器中反应后的气体进行如下探究:
【提示】①氢氧化钠可以吸收除去二氧化碳气体;②浓硫酸能吸水。
【提出猜想】
(1)小华对容器中气体的组成提出如下四种猜想,你认为其中明显不合理的有_________ (填字母)。
A可能有SO2 B可能有CO
C可能有CO2 D可能有CO2和O2的混合气体
(2)小军认为碳粉部分充分燃烧,还有部分没有充分燃烧,容器中的气体还可能是CO和CO2的混合气体;
【实验探究1】小军为了验证自己的猜想,按如下图所示装置进行探究。

请回答下列问题:
①小军的实验设计思路:装置A的作用是_______ ,若小军猜想正确,则可观察到装置A中的实验现象是_______ 。
②若原气体中含有CO气体,则D装置玻璃管中的现象是_______ ,气球作用是_______ 。
【实验探究2】小华认为容器中的气体是CO2和O2的混合气体,并进行实验改进和探究。小华把小军实验中的氧化铁换成了铜丝网,并去掉E装置进行验证。若小华的猜想成立,则装置D中的铜丝网的变化现象是_______ 。
【反思交流】有同学认为,小军应先通入容器中气体一段时间再加热,目的是________ 。
【提示】①氢氧化钠可以吸收除去二氧化碳气体;②浓硫酸能吸水。
【提出猜想】
(1)小华对容器中气体的组成提出如下四种猜想,你认为其中明显不合理的有
A可能有SO2 B可能有CO
C可能有CO2 D可能有CO2和O2的混合气体
(2)小军认为碳粉部分充分燃烧,还有部分没有充分燃烧,容器中的气体还可能是CO和CO2的混合气体;
【实验探究1】小军为了验证自己的猜想,按如下图所示装置进行探究。

请回答下列问题:
①小军的实验设计思路:装置A的作用是
②若原气体中含有CO气体,则D装置玻璃管中的现象是
【实验探究2】小华认为容器中的气体是CO2和O2的混合气体,并进行实验改进和探究。小华把小军实验中的氧化铁换成了铜丝网,并去掉E装置进行验证。若小华的猜想成立,则装置D中的铜丝网的变化现象是
【反思交流】有同学认为,小军应先通入容器中气体一段时间再加热,目的是
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐3】某实验小组对SO2的性质进行探究。用如图所示装置进行实验。
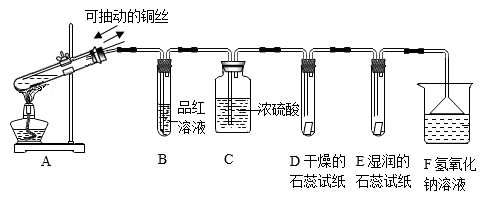
查阅资料:①二氧化硫的制取:铜和浓硫酸共热生成硫酸铜、二氧化疏、水
②二氧化硫可作为漂白剂,使品红溶液褪色;
③二氧化硫的化学性质与二氧化碳部分相似;
④氢氧化钠与二氧化硫反应: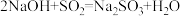
回答下列问题:
(1)A中用铜和浓硫酸制取SO2,使用可抽动的铜丝的优点是______ ,反应的化学方程式是______ 。
(2)在B中可观察到的现象为______ ;E中发生反应的化学方程式为:______ 。
(3)F装置的作用是______ 。

查阅资料:①二氧化硫的制取:铜和浓硫酸共热生成硫酸铜、二氧化疏、水
②二氧化硫可作为漂白剂,使品红溶液褪色;
③二氧化硫的化学性质与二氧化碳部分相似;
④氢氧化钠与二氧化硫反应:
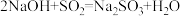
回答下列问题:
(1)A中用铜和浓硫酸制取SO2,使用可抽动的铜丝的优点是
(2)在B中可观察到的现象为
(3)F装置的作用是
您最近一年使用:0次



