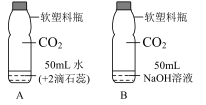
酸、碱、盐是几类重要的化合物,与人类生活和工农业生产关系十分密切。
(1)小组同学利用10%的氢氧化钠溶液制作叶脉书签。氢氧化钠属于______ (填“酸”“碱”或“盐”)。
(2)硝酸钾能为农作物生长提供养料。下表是硝酸钾的部分溶解度数据。
①40℃时,50g水中最多能溶解硝酸钾的质量为______ 。
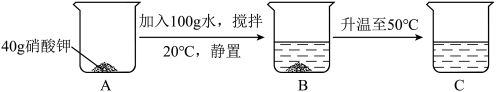
②小敏配制硝酸钾营养液时,操作过程如图所示。现要配制20%的硝酸钾营养液,需向烧杯C的溶液中加水______ g。______ ,说明氢氧化钠溶液和稀硫酸发生了化学反应。
②图B实验中加入碳酸钠溶液有气泡产生,写出该反应的化学方程式:______ 。
③图D实验是向图C实验后的试管中加入足量稀硝酸,发现沉淀部分溶解且有气泡产生,由此可判断图B实验后溶液中的溶质为______ (填化学式)。
(1)小组同学利用10%的氢氧化钠溶液制作叶脉书签。氢氧化钠属于
(2)硝酸钾能为农作物生长提供养料。下表是硝酸钾的部分溶解度数据。
| 温度/℃ | 20 | 30 | 40 | 50 |
| 溶解度/g | 31.6 | 45.8 | 63.9 | 85.5 |
②小敏配制硝酸钾营养液时,操作过程如图所示。现要配制20%的硝酸钾营养液,需向烧杯C的溶液中加水
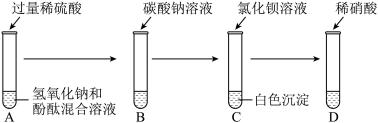
②图B实验中加入碳酸钠溶液有气泡产生,写出该反应的化学方程式:
③图D实验是向图C实验后的试管中加入足量稀硝酸,发现沉淀部分溶解且有气泡产生,由此可判断图B实验后溶液中的溶质为
更新时间:2024-05-10 14:05:05
|
相似题推荐
填空与简答-填空题
|
较易
(0.85)
解题方法
【推荐1】元素周期表是学习和研究化学的重要工具。请分析图中信息回答相关问题。
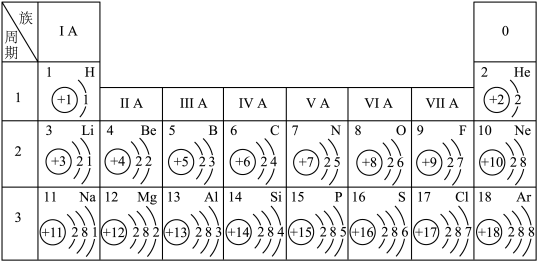
(1)氟元素的质子数是_____ ,在化学反应中容易_____ (填“得到”或“失去”)电子。
(2)原子序数为l、8、13的三种元素形成碱的化学式为_____ 。
(3)2019年5月美国制裁华为事件备受国人关注,华为旗下的芯片公司海思一夜由“备胎”“转正”。芯片是电脑、智能家电等的核心部件,芯片的主要成分是纯度极高的硅,其运算速率与硅的纯度有关。硅与金刚石结构相似,则构成硅的粒子是_____ (填粒子名称);1﹣18号元素中与硅的化学性质相似的是_____ (填元素符号)。

(1)氟元素的质子数是
(2)原子序数为l、8、13的三种元素形成碱的化学式为
(3)2019年5月美国制裁华为事件备受国人关注,华为旗下的芯片公司海思一夜由“备胎”“转正”。芯片是电脑、智能家电等的核心部件,芯片的主要成分是纯度极高的硅,其运算速率与硅的纯度有关。硅与金刚石结构相似,则构成硅的粒子是
您最近一年使用:0次
填空与简答-填空题
|
较易
(0.85)
解题方法
【推荐2】利用结构图对一些化学概念进行梳理是常用的学习方法,某同学用如图表示了一些概念间的关系,试回答:
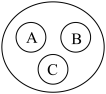
(1)若图中A、B、C代表酸、碱、盐三类物质,则大圈可代表______ 。
(2)若图中大圈表示吸热的物态变化,则A、B、C不可能代表的物态变化是_______ (写出一个名称即可)。

(1)若图中A、B、C代表酸、碱、盐三类物质,则大圈可代表
(2)若图中大圈表示吸热的物态变化,则A、B、C不可能代表的物态变化是
您最近一年使用:0次
填空与简答-填空题
|
较易
(0.85)
解题方法
【推荐3】人生中伴随着酸甜苦辣,化学中也有酸甜苦辣。请回答下列问题。
(1)酸:人的胃液中含有盐酸,食用含有铁粉的麦片后,铁粉会转化为______ (填离子符号)被人体吸收,从而有效预防______ 这一疾病。
(2)甜:蔗糖是储藏在甘蔗、甜菜等植物中的糖,日常生活中使用的白糖、冰糖和红糖的主要成分就是蔗糖,它是食品中常用的甜味剂。糖类在人体中的主要功能是______ 。
(3)苦:松花蛋的苦涩味道来自于草木灰(主要成分碳酸钾)、生石灰、水等通过一系列反应生成的氢氧化钾。按物质分类,氢氧化钾属于______ (填“酸”“碱”或“盐”)。
(4)辣:油泼辣子是陕西人餐桌上必不可少的调料。辣椒适宜在pH为6.2~7.2范围的土壤中种植,若某地区土壤pH约为5.2,若想在此地区种植辣椒,可以先加入适量的______ (填物质的俗称)调节土壤pH。
(1)酸:人的胃液中含有盐酸,食用含有铁粉的麦片后,铁粉会转化为
(2)甜:蔗糖是储藏在甘蔗、甜菜等植物中的糖,日常生活中使用的白糖、冰糖和红糖的主要成分就是蔗糖,它是食品中常用的甜味剂。糖类在人体中的主要功能是
(3)苦:松花蛋的苦涩味道来自于草木灰(主要成分碳酸钾)、生石灰、水等通过一系列反应生成的氢氧化钾。按物质分类,氢氧化钾属于
(4)辣:油泼辣子是陕西人餐桌上必不可少的调料。辣椒适宜在pH为6.2~7.2范围的土壤中种植,若某地区土壤pH约为5.2,若想在此地区种植辣椒,可以先加入适量的
您最近一年使用:0次
填空与简答-填空题
|
较易
(0.85)
真题
解题方法
【推荐1】溶液在日常生活,工农业生产和科学研究中具有广泛的用途。右图是硝酸钾和氯化钠两种物质的溶解度曲线,请回答:
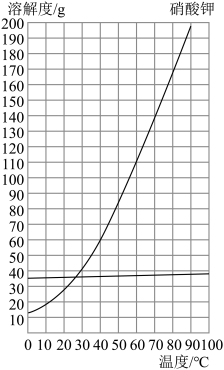
(1)在10℃时,氯化钠溶解度
(2)这两种物质中,
(3)60℃时,100g水里最多能溶解
您最近一年使用:0次
填空与简答-填空题
|
较易
(0.85)
解题方法
【推荐2】下表是某同学自制盐汽水的配料用量表。已知:20℃时,氯化钠的溶解度为36.0g。
表:盐汽水配料用量表
(1)盐汽水的能量很低,能量主要由______ 提供。
(2)20℃时,该盐汽水______ (填“能”或“不能”)继续溶解氯化钠固体氯化钠固体溶于水形成溶液的过程中,溶液的温度______ (填“降低”“升高”或“基本不变”)。
(3)柠檬酸(C6H8O7)中碳、氢元素的质量比为______ 。
(4)盐汽水中的“汽”是由柠檬酸与小苏打反应生成二氧化碳、水和柠檬酸钠(C6H5O7Na3)形成的,该反应的化学方程式为______ 。
表:盐汽水配料用量表
| 物质 | 用量/g |
| 纯净水 | 500 |
| 蔗糖 | 7.0 |
| 食盐 | 1.0 |
| 无水柠檬酸 | 1.3 |
| 小苏打 | 1.4 |
(2)20℃时,该盐汽水
(3)柠檬酸(C6H8O7)中碳、氢元素的质量比为
(4)盐汽水中的“汽”是由柠檬酸与小苏打反应生成二氧化碳、水和柠檬酸钠(C6H5O7Na3)形成的,该反应的化学方程式为
您最近一年使用:0次
【推荐3】根据图中KNO3,NaCl的溶解度曲线,回答下列问题:
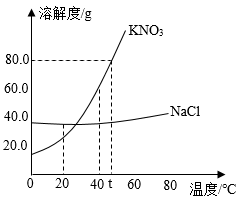
(1)40°C时 、NaCl两种物质的溶解度大小关系:KNO3
、NaCl两种物质的溶解度大小关系:KNO3___________ NaCl(填“>"“<”或“=”)。
(2)下列说法不正确的是___________(填字母)。
(3)同学们查阅NaCl的溶解度曲线后,欲配制20°C时100g溶质质量分数为10%的Na}Cl溶液。已知配制溶液的步骤有:①溶解;②计算;③装瓶存放;④称量。上述步骤的正确顺序为___________ (填序号)。

(1)40°C时
 、NaCl两种物质的溶解度大小关系:KNO3
、NaCl两种物质的溶解度大小关系:KNO3(2)下列说法不正确的是___________(填字母)。
| A.t°C时,将45gKNO3固体放入50g水中充分溶解,所得溶液的质量为95g |
| B.NaCl溶液中含有少量KNO3,可以采用蒸发结晶的方法提纯NaCl |
| C.40°C时,将KNO3的饱和溶液降温至20°C,溶液的溶质质量分数减小(不考虑水分损失) |
您最近一年使用:0次
填空与简答-填空题
|
较易
(0.85)
解题方法
【推荐1】如图为给病人输液用的氯化钠注射液的标签(部分文字)
(1)要配制一瓶该规格的注射液(密度约为1g/mL),需要氯化钠的质量为_____ g。
(2)若实验室用氯化钠固体配制该溶液,需要的玻璃仪器有烧杯、______ 、胶头滴管和量筒。
(3)若用量筒量取水时俯视读数(其他操作正确),会导致配制的溶液的溶质质量分数_______ (填“偏大”“偏小”或“不变”)。
| 氯化钠注射液 |
| 【规格】500mL,浓度(质量分数):0.9% 【适应症】各种原因所致的失水等 【用法】静脉滴注 |
(2)若实验室用氯化钠固体配制该溶液,需要的玻璃仪器有烧杯、
(3)若用量筒量取水时俯视读数(其他操作正确),会导致配制的溶液的溶质质量分数
您最近一年使用:0次
填空与简答-填空题
|
较易
(0.85)
解题方法
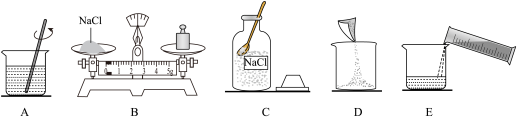
【推荐2】下面是配制100克质量分数为5%的氯化钠溶液的操作过程示意图:
(1)配制 溶质质量分数为5%的氯化钠溶液,需要氯化钠
溶质质量分数为5%的氯化钠溶液,需要氯化钠_______ g,需要水_______ g。
(2)上图按正确的实验操作排列顺序为_______ 。(选填序号)
①ABCDE②DECBA③CBEDA④CBDEA
(3)A步骤中,玻璃棒的作用是_______ 。
(4)某同学在实验过程E中,向烧杯中倒入水时不慎洒出少量水,所配制的溶液溶质质量分数将_______ (选填“偏大”“偏小”“不变”)。

(1)配制
 溶质质量分数为5%的氯化钠溶液,需要氯化钠
溶质质量分数为5%的氯化钠溶液,需要氯化钠(2)上图按正确的实验操作排列顺序为
①ABCDE②DECBA③CBEDA④CBDEA
(3)A步骤中,玻璃棒的作用是
(4)某同学在实验过程E中,向烧杯中倒入水时不慎洒出少量水,所配制的溶液溶质质量分数将
您最近一年使用:0次
填空与简答-流程题
|
较易
(0.85)
解题方法
【推荐1】一种“氢氧化锶-氯化镁法”制备“牙膏用氯化锶(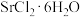 )”的工艺流程如图:
)”的工艺流程如图:
①欧锶的相关化合物(如SrO、SrCO3)的化学性质与相应的钙化合物类似,SrCO4、SrCO3不溶于水。
②SrCl2、MgCl2溶液皆为无色,呈中性。
(1)煅烧工业碳酸锶发生的反应与煅烧石灰石类似,则此过程的化学方程式为___________ 。
(2)“重结晶”是将蒸发结晶得到的无水氢氧化锶粗品溶于适量热水,趁热滤去未溶解的固体后,冷却结晶得到Sr(OH)2•8H2O。为探究蒸馏水用量对Sr(OH)2•8H2O纯度及产率的影响,设计一系列探究实验,结果如表所示。分析表格数据可知,最合适的实验条件为___________ (填序号),当蒸馏水用量大于该条件时,Sr(OH)2•8H2O产率减小,试推测其原因___________ 。
(3)步骤④中,为了保证氯化锶产出量,MgCl2溶液必须足量,判断MgCl2已经加足的方法是:取反应后的上层清液,___________ 。
(4)步骤⑤降温结晶制备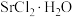 ,需要40%的SrCl2溶液100g,该溶液可由10%的SrCl2溶液蒸发
,需要40%的SrCl2溶液100g,该溶液可由10%的SrCl2溶液蒸发___________ g水获得。
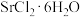 )”的工艺流程如图:
)”的工艺流程如图: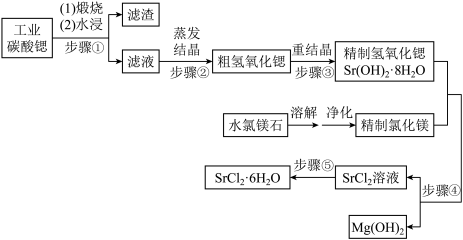
①欧锶的相关化合物(如SrO、SrCO3)的化学性质与相应的钙化合物类似,SrCO4、SrCO3不溶于水。
②SrCl2、MgCl2溶液皆为无色,呈中性。
(1)煅烧工业碳酸锶发生的反应与煅烧石灰石类似,则此过程的化学方程式为
(2)“重结晶”是将蒸发结晶得到的无水氢氧化锶粗品溶于适量热水,趁热滤去未溶解的固体后,冷却结晶得到Sr(OH)2•8H2O。为探究蒸馏水用量对Sr(OH)2•8H2O纯度及产率的影响,设计一系列探究实验,结果如表所示。分析表格数据可知,最合适的实验条件为
| 序号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
| 无水Sr(OH)2粗品质量/g | 10.0 | 10.0 | 10.0 | 10.0 | 10.0 | 10.0 | 10.0 |
| 蒸馏水质量/g | 40.0 | 50.0 | 60.0 | 70.0 | 80.0 | 90.0 | 100 |
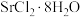 纯度/% 纯度/% | 98.6 | 98.6 | 98.6 | 98.6 | 98.6 | 98.6 | 98.6 |
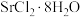 产率% 产率% | 17.91 | 53.36 | 63.50 | 72.66 | 92.17 | 89.65 | 88.93 |
(3)步骤④中,为了保证氯化锶产出量,MgCl2溶液必须足量,判断MgCl2已经加足的方法是:取反应后的上层清液,
(4)步骤⑤降温结晶制备
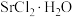 ,需要40%的SrCl2溶液100g,该溶液可由10%的SrCl2溶液蒸发
,需要40%的SrCl2溶液100g,该溶液可由10%的SrCl2溶液蒸发
您最近一年使用:0次
填空与简答-推断题
|
较易
(0.85)
解题方法
【推荐2】A、B、C、D、E、F六种物质都是初中化学内容中涉及的化合物,转化关系如图所示,其中D是最常见的溶剂。_______ ,E是_______ ,F是_______ (填写化学式)。
(2)写出反应①的化学方程式_______ ,写出反应②的化学方程式_______ ,反应④属于_______ 反应(填写基本反应类型)。
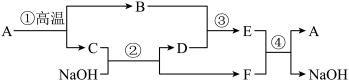
(2)写出反应①的化学方程式
您最近一年使用:0次