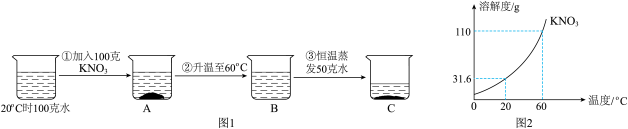
请结合图示实验和溶解度曲线图,回答以下问题:_______ (饱和/不饱和)溶液。
(2)过程③中,当蒸发掉50g水时析出KNO3,晶体的质量是_______ 克,此时烧杯A、B和C中溶液溶质质量分数由大到小的顺序是_______ 。
(3)根据过程②中KNO3的溶解原理,可推知若要从接近饱和的KNO3,溶液中获得少量KNO3晶体,可采用的方法是_______ 。
(2)过程③中,当蒸发掉50g水时析出KNO3,晶体的质量是
(3)根据过程②中KNO3的溶解原理,可推知若要从接近饱和的KNO3,溶液中获得少量KNO3晶体,可采用的方法是
2024·内蒙古呼和浩特·一模 查看更多[2]
更新时间:2024-05-11 15:20:24
|
相似题推荐
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】如图是甲、乙、丙三种固体物质的溶解度曲线,请回答下列问题:
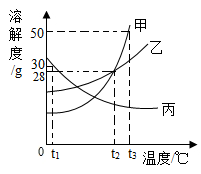
(1)三种物质中________ (填“甲”、“乙”或“丙”)的溶解度随温度变化的趋势与气体溶解度随温度变化的趋势相似。
(2)将t2℃时甲、乙两物质的饱和溶液分别蒸发等质量的水,析出固体的质量:甲_______ (填“>”、“<”或“=”)乙。
(3)若甲的饱和溶液中混有少量乙,可采用的________ 方法提纯甲。
(4)将t3℃时等质量的甲、乙、丙三种物质的饱和溶液同时降温至t1℃,所得溶液中溶剂质量由大到小的顺序为__________ 。

(1)三种物质中
(2)将t2℃时甲、乙两物质的饱和溶液分别蒸发等质量的水,析出固体的质量:甲
(3)若甲的饱和溶液中混有少量乙,可采用的
(4)将t3℃时等质量的甲、乙、丙三种物质的饱和溶液同时降温至t1℃,所得溶液中溶剂质量由大到小的顺序为
您最近一年使用:0次
【推荐2】北京冬奥会充分体现了“绿色冬奥”“科技冬奥”的理念,向世界展示了中国智慧。试回答下列问题:

(1)①冬奥会火炬“飞扬”的外壳采用了一种碳纤维与高新能树脂结合的新型材料,具有质量轻,强度大的优良性能。请问此材料属于_________ (填“有机高分子材料”“复合材料”“无机材料”之一)
②防疫黑科技,确保冬奥会的防疫安全。AOP-KF 固体碱是一种独特的空气净化材料,在消灭病毒的过程中释放出二氧化氯,从而消杀病毒。则二氧化氯中氯元素的化合价为________ 。
③张北的风,丰宁的水,五棵松的光,“风光水”三人组承包了冬奥会的绿电供应。五棵松冰上运动中心的光伏发电系统,是将________ 能转化为电能。
(2)1926 年,我国著名化学家侯德榜先生创立了“侯氏制碱法”,促进了世界制碱技术的发展,该技术以从海水中提取出来的食盐为主要原料制取纯碱。碳酸钠和氯化钠的溶解度曲线如图所示,试回答:
①在 t1℃时, Na2CO3的溶解度为______
②当Na2CO3固体中含有少量NaCl时 ,可采用___________ 方法提纯Na2CO3(填“蒸发结晶”“降温结晶”之一)。
③将t2℃时NaCl和Na2CO3的饱和溶液分别降温至t1℃,此时所得Na2CO3溶液的质量分数________ (填“小于”“等于”“大于”之一)NaCl溶液的质量分数。
④t1℃时,一小试管内盛有 Na2CO3的饱和溶液,试管底部还存有少许固体 Na2CO3固体,将小试管放入盛有水的烧杯中,然后将多量的 NaOH 固体加入烧杯的水中,观察到小试管内的固体物质逐渐溶解,原因是___________ 。

(1)①冬奥会火炬“飞扬”的外壳采用了一种碳纤维与高新能树脂结合的新型材料,具有质量轻,强度大的优良性能。请问此材料属于
②防疫黑科技,确保冬奥会的防疫安全。AOP-KF 固体碱是一种独特的空气净化材料,在消灭病毒的过程中释放出二氧化氯,从而消杀病毒。则二氧化氯中氯元素的化合价为

③张北的风,丰宁的水,五棵松的光,“风光水”三人组承包了冬奥会的绿电供应。五棵松冰上运动中心的光伏发电系统,是将
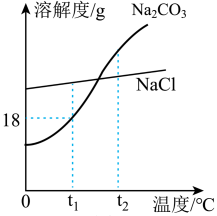
(2)1926 年,我国著名化学家侯德榜先生创立了“侯氏制碱法”,促进了世界制碱技术的发展,该技术以从海水中提取出来的食盐为主要原料制取纯碱。碳酸钠和氯化钠的溶解度曲线如图所示,试回答:

①在 t1℃时, Na2CO3的溶解度为
②当Na2CO3固体中含有少量NaCl时 ,可采用
③将t2℃时NaCl和Na2CO3的饱和溶液分别降温至t1℃,此时所得Na2CO3溶液的质量分数
④t1℃时,一小试管内盛有 Na2CO3的饱和溶液,试管底部还存有少许固体 Na2CO3固体,将小试管放入盛有水的烧杯中,然后将多量的 NaOH 固体加入烧杯的水中,观察到小试管内的固体物质逐渐溶解,原因是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】根据题意回答下列问题:
(1)在人类社会的发展进程中,金属起着重要的作用。

①美丽的大雁塔广场矗立着玄奘大师的青铜雕像,青铜是铜锡合金,其属于___________ (选填“金属”或“非金属”)材料。
②铁的化学性质比较活泼,在潮湿的空气中容易生锈,工人师傅常用稀盐酸除铁锈,观察到的现象为___________ 。
(2)如图为A、B、C三种固体物质的溶解度曲线,据图回答下列问题。
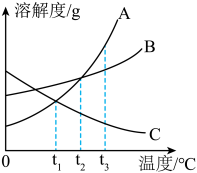
①t3°C时,A、B、C三种物质溶解度由大到小的顺序为___________ 。
②在不改变溶液中溶质的质量分数的前提下,要使接近饱和的C溶液变为饱和溶液,可采取的一种措施是___________ 。
③t3℃时,B中混有少量的A,则提纯B的方法是___________ 。
(1)在人类社会的发展进程中,金属起着重要的作用。

①美丽的大雁塔广场矗立着玄奘大师的青铜雕像,青铜是铜锡合金,其属于
②铁的化学性质比较活泼,在潮湿的空气中容易生锈,工人师傅常用稀盐酸除铁锈,观察到的现象为
(2)如图为A、B、C三种固体物质的溶解度曲线,据图回答下列问题。

①t3°C时,A、B、C三种物质溶解度由大到小的顺序为
②在不改变溶液中溶质的质量分数的前提下,要使接近饱和的C溶液变为饱和溶液,可采取的一种措施是
③t3℃时,B中混有少量的A,则提纯B的方法是
您最近一年使用:0次
填空与简答-简答题
|
适中
(0.65)
【推荐1】溶解是生活中常见的现象,不同物质在水中的溶解能力不同。
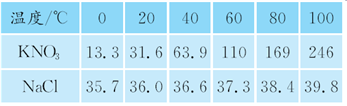
(1)下表是KNO3、NaCl在不同温度下的溶解度(单位:g/100 g水)。
Ⅰ.上表中的两种物质在40 ℃时,________ 的溶解度较大。
Ⅱ.请写出一种将KNO3的不饱和溶液转化为饱和溶液的方法_____________________ 。
Ⅲ.20 ℃时,将20 g NaCl放入50 g水中,所得溶液的质量是________ g。
Ⅳ.从NaCl溶液中得到NaCl晶体的方法是__________ 。
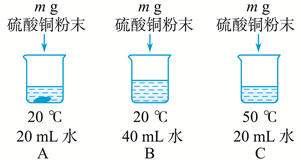
(2)用硫酸铜进行如下图所示的实验,完成下列填空(用编号表示)。
所得三个溶液中:一定属于饱和溶液的是__________ ,溶液中溶剂质量的大小关系是__________ 。

(1)下表是KNO3、NaCl在不同温度下的溶解度(单位:g/100 g水)。
Ⅰ.上表中的两种物质在40 ℃时,
Ⅱ.请写出一种将KNO3的不饱和溶液转化为饱和溶液的方法
Ⅲ.20 ℃时,将20 g NaCl放入50 g水中,所得溶液的质量是
Ⅳ.从NaCl溶液中得到NaCl晶体的方法是
(2)用硫酸铜进行如下图所示的实验,完成下列填空(用编号表示)。
所得三个溶液中:一定属于饱和溶液的是

您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】A、B、C三种固体物质的溶解度曲线如下图所示。据图回答问题:

(1)温度为______ ℃时,A与C物质的溶解度相等;
(2)t2℃时,把A、B物质各30g分别加到50g水中,不能形成饱和溶液的是________ (填字母代号),若要使之达到饱和状态,还需要向溶液中加入________ g该溶质。

(1)温度为
(2)t2℃时,把A、B物质各30g分别加到50g水中,不能形成饱和溶液的是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
真题
【推荐1】下图是甲、乙、丙三种固体物质的溶解度曲线,回答下列问题:
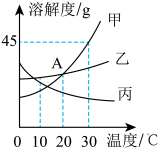
(1)A点的含义是_____________________ 。
(2)在30℃时,向30克甲物质中加入50克水,充分溶解后所得溶液是____________ 溶液(填“饱和”或“不饱和”)。
(3)若乙中混有少量甲,最好采用_________ 的方法提纯乙(填“降温结晶”或“蒸发结晶”)。
(4)将30℃时甲、乙、丙三种物质的饱和溶液降温到10℃,则其溶质质量分数不变的物质是_________________ 。

(1)A点的含义是
(2)在30℃时,向30克甲物质中加入50克水,充分溶解后所得溶液是
(3)若乙中混有少量甲,最好采用
(4)将30℃时甲、乙、丙三种物质的饱和溶液降温到10℃,则其溶质质量分数不变的物质是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】人类的日常生活和工农业生产离不开水。
(1)水在通电的条件下可以分解,该反应的化学方程式为________ 。
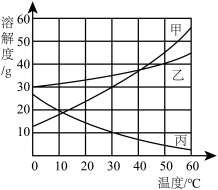
(2)甲、乙、丙三种固体物质的溶解度曲线如图所示。
①20℃时,甲、乙、丙三种物质的溶解度由大到小的顺序为________ 。
②20℃时,将50g乙物质放入100g水中充分溶解,所得溶液是_________ 溶液(填“饱和”或“不饱和”)。将此溶液升温至50℃,此时该溶液的溶质质量分数为_____________ %。(结果精确到0.1%)
③50℃时,将等质量的甲、乙、丙三种物质的饱和溶液同时降温至10℃,所得溶液中溶质质量分数最小的是__________ ,溶质质量分数最大的是_________ (填“甲”、“乙”或“丙”)。

(1)水在通电的条件下可以分解,该反应的化学方程式为
(2)甲、乙、丙三种固体物质的溶解度曲线如图所示。
①20℃时,甲、乙、丙三种物质的溶解度由大到小的顺序为
②20℃时,将50g乙物质放入100g水中充分溶解,所得溶液是
③50℃时,将等质量的甲、乙、丙三种物质的饱和溶液同时降温至10℃,所得溶液中溶质质量分数最小的是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
名校
解题方法
【推荐3】溶解度曲线中的任何一点都表示溶液的一种特定状态。 当溶液状态发生变化时,表示溶液状态的点的位置(坐标)也将发生相应的改变。某固态物质的溶解度曲线如图所示,试根据图回答下列问题。
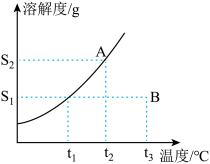
(1)当处于A、B点状态的该溶液分别发生下列变化(其他条件不变)时,试参考表中例示描述A、B点的变动过程。
(2)某温度下物质A的溶解度为25g,该温度下将47.53g的A投入172.85g水中充分溶解后得到溶液中A的质量分数为___________ (百分数表示)。

(1)当处于A、B点状态的该溶液分别发生下列变化(其他条件不变)时,试参考表中例示描述A、B点的变动过程。
| A点的变动 | B点的变动 | |
| ①升高温度 | 向右平移 | |
| ②降低温度至t1以下 | 沿曲线下移 | |
| ③蒸发溶剂 | ||
| ④稀释洛液 |
(2)某温度下物质A的溶解度为25g,该温度下将47.53g的A投入172.85g水中充分溶解后得到溶液中A的质量分数为
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
名校
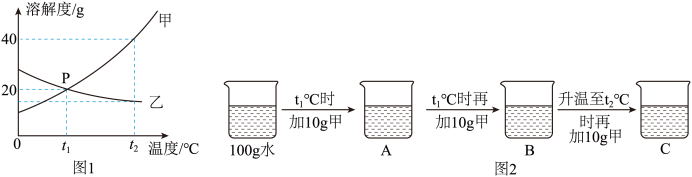
【推荐1】甲、乙两种固体物质的溶解度曲线如图所示,请回答问题:
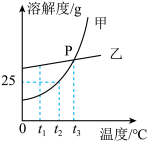
(1)t1℃时,甲、乙两种物质的溶解度大小关系为甲______ (填“<”“>”或“=”)乙;
(2)P点的含义______ ;
(3)t2℃时,把20 g固体甲放入50 g水中,充分搅拌,所得溶液的质量是______ g;
(4)欲将t2℃时乙物质的不饱和溶液变为该温度下的饱和溶液,可采取的一种方法是______ ;
(5)如果甲物质中含有少量乙物质,若要提纯甲,一般采用______ 的方法;
(6)将t2℃时甲、乙两种物质的饱和溶液降温到t1℃时,溶质质量分数的大小关系______ 。

(1)t1℃时,甲、乙两种物质的溶解度大小关系为甲
(2)P点的含义
(3)t2℃时,把20 g固体甲放入50 g水中,充分搅拌,所得溶液的质量是
(4)欲将t2℃时乙物质的不饱和溶液变为该温度下的饱和溶液,可采取的一种方法是
(5)如果甲物质中含有少量乙物质,若要提纯甲,一般采用
(6)将t2℃时甲、乙两种物质的饱和溶液降温到t1℃时,溶质质量分数的大小关系
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
名校
解题方法
【推荐2】t1℃时,烧杯A中装有R物质的饱和溶液,进行某些操作后,实验结果如图所示:
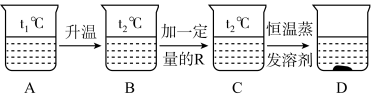
(1)B~D中,一定属于饱和溶液的是______ (填字母序号,下同),溶质的质量分数最小的是______ 。
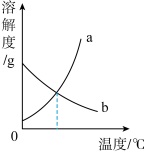
(2)R和N两种物质的溶解度曲线分别如图所示,则R物质的溶解度曲线是______ 。
(3)R的饱和溶液含有少量杂质N。若要从该溶液中提取纯净的R物质,具体的操作是______ 。


(1)B~D中,一定属于饱和溶液的是
(2)R和N两种物质的溶解度曲线分别如图所示,则R物质的溶解度曲线是
(3)R的饱和溶液含有少量杂质N。若要从该溶液中提取纯净的R物质,具体的操作是
| A.蒸发结晶、过滤、洗涤、干燥 |
| B.降温结晶、过滤、洗涤、干燥 |
| C.升温结晶、过滤、洗涤、干燥 |
您最近一年使用:0次