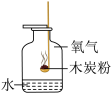
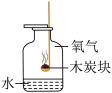
甲烷完全燃烧的化学方程式为_____ 。当氧气不足时,3.2g甲烷在密闭容器内燃烧会生成一氧化碳、二氧化碳和水,恢复到室温,测得所得气体中氧元素的质量分数为60%,则参加反应的氧气的质量是_____ g。燃料充分燃烧可以节约能源,使燃料充分燃烧,应考虑_____ 。
更新时间:2024-05-21 21:51:14
|
相似题推荐
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】2021辛丑牛年,南京博物院展出战国时期的“牛牛酒壶”错金银铜牺尊造型像;牛表面装饰了金银图案的青铜酒器。

(1)“牛牛酒壶”的主要材质是青铜,青铜的熔点___________ (选填“高于”“低于”“等于”)其组成金属的熔点。
(2)错金银铜牺尊表面的银装饰线已经发黑,原因之一是银与氧气、硫化氢反应生成了硫化银(Ag2S)。写出反应的化学方程式___________ 。
(3)历经千年,牺尊表面锈蚀生成了碱式碳酸铜(Cu2(OH)2CO3)。铜的锈蚀是铜与空气中的___________ (填化学式)等物质共同作用的过程。
(4)为研究Cu2(OH)2CO3的性质,实验室进行制备。
I:配制溶液:用电子天平分别称取7.20 g无水硫酸铜粉末和5.30 g碳酸钠粉末,将它们分别配制成60℃的饱和溶液。已知CuSO4的溶解度表:
①配制上述硫酸铜饱和溶液需要水的体积为 ___________ mL。
②配溶液时为加速溶解,可采取的措施是___________ 。
Ⅱ:制取碱式碳酸铜:将Ⅰ中所配制的CuSO4溶液(酸性)和Na2CO3溶液(过量)混合,可生成碱式碳酸铜。
①生成碱式碳酸铜的最佳条件:60℃,pH约为8.6.应选用的加料方式是___________ (填字母)。
a将CuSO4溶液与Na2CO3溶液同时加入到反应容器中
b将Na2CO3溶液缓慢加入到盛有CuSO4,溶液的反应容器中
c将CuSO4溶液缓慢加入到盛有Na2CO3溶液的反应容器中
②发生的反应为2CuSO4+ 2Na2CO3 + H2O= Cu2(OH)2CO3↓ + X↑ + 2Na2SO4.则X的化学式为___________ 。
Ⅲ:过滤、洗涤、烘干得到碱式碳酸铜
若上述制取过程无其它反应发生,请计算理论上可得到碱式碳酸铜的质量(写出计算过程)。___________

(1)“牛牛酒壶”的主要材质是青铜,青铜的熔点
(2)错金银铜牺尊表面的银装饰线已经发黑,原因之一是银与氧气、硫化氢反应生成了硫化银(Ag2S)。写出反应的化学方程式
(3)历经千年,牺尊表面锈蚀生成了碱式碳酸铜(Cu2(OH)2CO3)。铜的锈蚀是铜与空气中的
(4)为研究Cu2(OH)2CO3的性质,实验室进行制备。
I:配制溶液:用电子天平分别称取7.20 g无水硫酸铜粉末和5.30 g碳酸钠粉末,将它们分别配制成60℃的饱和溶液。已知CuSO4的溶解度表:
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 |
| 溶解度/g | 14.3 | 20.7 | 28.5 | 40 | 55 | 75.4 |
②配溶液时为加速溶解,可采取的措施是
Ⅱ:制取碱式碳酸铜:将Ⅰ中所配制的CuSO4溶液(酸性)和Na2CO3溶液(过量)混合,可生成碱式碳酸铜。
①生成碱式碳酸铜的最佳条件:60℃,pH约为8.6.应选用的加料方式是
a将CuSO4溶液与Na2CO3溶液同时加入到反应容器中
b将Na2CO3溶液缓慢加入到盛有CuSO4,溶液的反应容器中
c将CuSO4溶液缓慢加入到盛有Na2CO3溶液的反应容器中
②发生的反应为2CuSO4+ 2Na2CO3 + H2O= Cu2(OH)2CO3↓ + X↑ + 2Na2SO4.则X的化学式为
Ⅲ:过滤、洗涤、烘干得到碱式碳酸铜
若上述制取过程无其它反应发生,请计算理论上可得到碱式碳酸铜的质量(写出计算过程)。
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】四种金属氧化物:①CuO;②MgO;③Al2O3;④Fe3O4中,氧元素含量最高的是___________ ;5.2gC2H2在点燃时能与14.4gO2反应,得到13.2gCO2、3.6gH2O和mgCO,则m为___________ ,该反应的化学方程式为___________ 。
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐3】请回答下列问题。
(1)在A+B=C+D的反应中,5gA物质跟4gB物质恰好完全反应,生成3gC物质和____ 克D物质,这是根据_____ 定律进行上述计算的。
(2)冷风“吹灭”火焰的主要原因是_____ ;纯净的H2在空气中平静的燃烧而不会爆炸,说明H2燃烧的速率,与它和O2的____ 有关,氢气燃烧的化学方程式为_____ 。
(3)硝化甘油为一种烈性炸药,应用于矿山、国防等多方面。它的化学式为C3H5N3O9,每个分子中共有______ 个原子,它的相对分子质量是______ ,氢元素和氮元素的质量比为______ 。
(1)在A+B=C+D的反应中,5gA物质跟4gB物质恰好完全反应,生成3gC物质和
(2)冷风“吹灭”火焰的主要原因是
(3)硝化甘油为一种烈性炸药,应用于矿山、国防等多方面。它的化学式为C3H5N3O9,每个分子中共有
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】写出下列反应的化学方程式,并指明(1)、(3)基本反应的类型。
(1)红磷在氧气中燃烧_______________ ( ) 。
(2)铁在氧气中燃烧_____________________ 。
(3)加热高锰酸钾制取氧气_______________ ( ) 。
(4)电解水___________________ 。
(1)红磷在氧气中燃烧
(2)铁在氧气中燃烧
(3)加热高锰酸钾制取氧气
(4)电解水
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐2】硫酸锌可作为食品添加剂。工业上常用菱锌矿生产硫酸锌,菱锌矿的主要成分是ZnCO3,并含少量的FeO、CuO。工艺流程图如下:(假设每一步骤反应均完全)
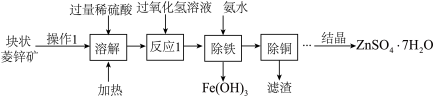
(1)为提高矿石的溶解速度,操作1是_________ 。
(2)菱锌矿溶解后所得的溶液中阳离子 有_________ 。
(3)反应1中H2O2转化为H2O,同时有Fe2(SO4)3生成,写出反应1中生成Fe2(SO4)3的化学方程式_________ 。
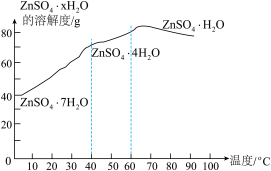
(4)硫酸锌晶体的溶解度曲线如图,若要获得ZnSO4·7H2O晶体,应控制结晶时温度范围为_________ 。
(5)流程中还可能得到一种紫罗兰色晶体(NH4)xFey(SO4)z·7H2O。已知该化合物中氮、铁元素质量比为1:4,则x:y:z=_________ 。

(1)为提高矿石的溶解速度,操作1是
(2)菱锌矿溶解后所得的溶液中
(3)反应1中H2O2转化为H2O,同时有Fe2(SO4)3生成,写出反应1中生成Fe2(SO4)3的化学方程式
(4)硫酸锌晶体的溶解度曲线如图,若要获得ZnSO4·7H2O晶体,应控制结晶时温度范围为

(5)流程中还可能得到一种紫罗兰色晶体(NH4)xFey(SO4)z·7H2O。已知该化合物中氮、铁元素质量比为1:4,则x:y:z=
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐3】(1)化学世界绚丽多彩,请选择适当的序号 填空:
A蓝色 B绿色 C黑色 D白色 E黄色 F红色
①硫酸铜溶液______ ;②铜丝______ ;③碱式碳酸铜______ ;④硫粉______ .
(2)化学世界千变万化,请写出下列反应的化学方程式 :
①生成两种气体单质的分解反应______ ;②铁置换硫酸铜溶液中的铜______ ;③汽车尾气中NO和CO在催化剂作用下生成空气中两种无毒气体______ ;④CO2和CH4在催化剂作用下生成CO和H2______ .
(3)化学世界源于生活,请选择适当的序号 填空.
A钛合金 B浓硫酸 C碳酸氢铵 D武德合金 E二氧化碳 F液氮
①具有吸水作用______ ;②用于制造航天航空器的材料______ ;③绿色植物光合作用的原料之一______ ;④用作保险丝的物质______ ;⑤用于农业生产做氮肥的物质______ ;⑥用作医疗冷冻的物质______ .
A蓝色 B绿色 C黑色 D白色 E黄色 F红色
①硫酸铜溶液
(2)化学世界千变万化,请写出下列反应的
①生成两种气体单质的分解反应
(3)化学世界源于生活,请选择适当的
A钛合金 B浓硫酸 C碳酸氢铵 D武德合金 E二氧化碳 F液氮
①具有吸水作用
您最近一年使用:0次
填空与简答-科普阅读题
|
适中
(0.65)
【推荐1】利用所学习的有关燃烧与灭火的知识完成下列小题。
(1)森林突发大火消防队员常使用一种手持式风力灭火机,它可以喷出类似十二级台风的高速气流将火吹灭。该灭火机的灭火原理是_____ 请你再举一种与上述灭火原理不同的森林大火的灭火措施_____ ;
一般不考虑用水灭森林大火的原因是_____ 。
(2)阅读材料,回答问题。
材料一:某年1月份某市酒吧发生一起特大火灾.该事故的起因是几个年轻人在酒吧内燃放烟花,引燃聚氨酯泡沫塑料天花板,聚氨酯泡沫塑料燃烧产生大量有毒烟气造成人员中毒身亡.
材料二:氢氧化镁是一种新型的阻燃剂.当温度达到380°C时,氢氧化镁开始分解出水蒸气同时生成耐高温的氧化镁固体。利用氢氧化镁这一性质将它添加在塑料等易燃性材料中能起阻燃作用。
①通过阅读用题中信息回答问题。请说出聚氨酯泡沫塑料的一点化学性质_____ ;
②燃的烟花在引发这场火灾中所起的作用是_____ (填标号)
A 提供氧气;
B 使可燃物的温度达到着火点;
C 提供可燃物
③根据灭火原理初步分析氢氧化镁能作阻燃剂的原因_____ 。氢氧化镁受热分解的化学方程式为_____ 。
(3)可燃性气体或粉尘在空气不流通的空间里聚集到一定浓度后,一旦遇到明火就会发生爆炸称为闪爆。下列物质可能会发生“闪爆”的是_____ (填字母序号).
A CH4
B CO2
C N2
D 面粉
(1)森林突发大火消防队员常使用一种手持式风力灭火机,它可以喷出类似十二级台风的高速气流将火吹灭。该灭火机的灭火原理是
一般不考虑用水灭森林大火的原因是
(2)阅读材料,回答问题。
材料一:某年1月份某市酒吧发生一起特大火灾.该事故的起因是几个年轻人在酒吧内燃放烟花,引燃聚氨酯泡沫塑料天花板,聚氨酯泡沫塑料燃烧产生大量有毒烟气造成人员中毒身亡.
材料二:氢氧化镁是一种新型的阻燃剂.当温度达到380°C时,氢氧化镁开始分解出水蒸气同时生成耐高温的氧化镁固体。利用氢氧化镁这一性质将它添加在塑料等易燃性材料中能起阻燃作用。
①通过阅读用题中信息回答问题。请说出聚氨酯泡沫塑料的一点化学性质
②燃的烟花在引发这场火灾中所起的作用是
A 提供氧气;
B 使可燃物的温度达到着火点;
C 提供可燃物
③根据灭火原理初步分析氢氧化镁能作阻燃剂的原因
(3)可燃性气体或粉尘在空气不流通的空间里聚集到一定浓度后,一旦遇到明火就会发生爆炸称为闪爆。下列物质可能会发生“闪爆”的是
A CH4
B CO2
C N2
D 面粉
您最近一年使用:0次
【推荐2】2016年12月3日12时左右,内蒙古赤峰市一煤矿发生的爆炸事故,此次爆炸为煤矿里的瓦斯气爆炸。瓦斯气的主要成分与天然气的主要成分相同,其主要成分为_______ (填名称),其燃烧的化学方程式是:_______ 。天然气与_______ 和_______ 被称之为三大化石燃料。化石燃料是不可再生资源,节约化石燃料走可持续发展道路,要使燃料充分燃烧一方面要_______ ;另一方面要_______ 。
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】关于燃烧的研究是一项重要的课题。学校实验小组以“探究燃烧的奥秘”为主题开展项目式学习。
【任务一】认识燃烧
(1)煤(含硫)石油、天然气是生活中常见的燃料,下列不属于三者完全燃烧共有的现象是__________(填字母)。
(2)写出天然气主要成分完全燃烧的化学方程式___________ 。
【任务二】燃烧的条件
(3)戴维发明了一种安全灯,采用一种网眼很小的普通金属网罩住火焰,使得金属网外的温度不会明显升高,这种灯在矿井里点燃不会引起可燃性气体的爆炸。结合燃烧条件请你分析可燃性气体不会爆炸的原因__________ 。

【任务三】燃烧的控制
(4)实验小组进行了以下实验,如表所示:
I.实验②中木炭粉燃烧的现象____________ ,实验②与实验③对比可以证明___________ 对物质燃烧有影响。
II.实验结束后,往实验②的集气瓶中滴加紫色石蕊溶液,溶液变红,请用化学方程式解释石蕊变红的原因____________ 。
【任务一】认识燃烧
(1)煤(含硫)石油、天然气是生活中常见的燃料,下列不属于三者完全燃烧共有的现象是__________(填字母)。
| A.产生的气体通入澄清石灰水中均变浑浊 | B.燃烧有光或火焰产生 |
| C.产生有刺激性气味的气体 | D.燃烧放热 |
(2)写出天然气主要成分完全燃烧的化学方程式
【任务二】燃烧的条件
(3)戴维发明了一种安全灯,采用一种网眼很小的普通金属网罩住火焰,使得金属网外的温度不会明显升高,这种灯在矿井里点燃不会引起可燃性气体的爆炸。结合燃烧条件请你分析可燃性气体不会爆炸的原因

【任务三】燃烧的控制
(4)实验小组进行了以下实验,如表所示:
| 实验 | ① | ② | ③ |
| 操作 |
|
|
|
II.实验结束后,往实验②的集气瓶中滴加紫色石蕊溶液,溶液变红,请用化学方程式解释石蕊变红的原因
您最近一年使用:0次
【推荐2】奥运火炬燃料的变迁史如下图所示。
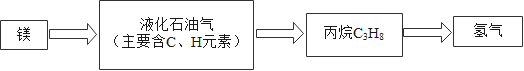
(1)镁燃烧时,能量的转化形式是_______ 能转化为热能和光能。
(2)丙烷完全燃烧的产物为_______ 。
(3)2022年冬奥会,科学家们利用太阳能和催化剂分解水制氢气,该反应的化学方程式为____ 。氢气做燃料的优点是_______ 。
(4)液化石油气中氢元素的质量分数约为12%。理论上,1 kg的液化石油气完全燃烧时,产生水的质量约为_______ kg。

(1)镁燃烧时,能量的转化形式是
(2)丙烷完全燃烧的产物为
(3)2022年冬奥会,科学家们利用太阳能和催化剂分解水制氢气,该反应的化学方程式为
(4)液化石油气中氢元素的质量分数约为12%。理论上,1 kg的液化石油气完全燃烧时,产生水的质量约为
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐3】(1)“洁厕灵”、“漂白精”是家庭常用的两种清洁剂。“洁厕灵”的有效成分是盐酸,可清除污垢,但不能用于清洁大理石制品,理由是(写化学方程式)______________ ;
(2)波尔多液是一种农业上的杀菌剂,它由石灰乳与硫酸铜等配制而成。请用化学方程式解释不能用铁制容器来配制波尔多液的原因是______________ ;
(3)我国与俄罗斯达成400亿美元的天然气购销协议.天然气的主要成分是_____ ,在空气中充分燃烧的化学方程式为______________ .
(2)波尔多液是一种农业上的杀菌剂,它由石灰乳与硫酸铜等配制而成。请用化学方程式解释不能用铁制容器来配制波尔多液的原因是
(3)我国与俄罗斯达成400亿美元的天然气购销协议.天然气的主要成分是
您最近一年使用:0次