回答下列问题。
(1)按要求从氢气、氯化钾、氧化钙、盐酸中选取合适的物质,将其化学式填写在下列横线上。
①一种可燃性气体_____________ ;
②一种可溶性的盐_____________ ;
③一种金属氧化物_____________ ;
④一种易挥发的酸___________________________ 。
(2)化学与生活、社会发展息息相关。
①在每一餐中,我们都需要摄取足够的蛋白质、碳水化合物、脂肪和各种维生素。如玉米、胡萝卜中的叶黄素(化学式为C40H56O2),有助于维护视力持久度,减少视觉伤害。叶黄素属于___________________ (填“有机物”“氧化物”之一),在叶黄素分子中,氧原子与氢原子的个数之比为_________ (填写最简整数比)。在叶黄素中质量分数最小的元素是_______________________ (填元素名称)。_________________ (选填“降低”“提高”之一)肥效。
③生产电脑芯片的材料主要是高纯硅。工业上可用以下方法制取硅:2H2+SiCl4 Si+4HCl,其反应类型为
Si+4HCl,其反应类型为__________ (选填“化合”“分解”“置换”“复分解”之一)反应。四氯化硅(SiCl4)中硅元素的化合价是__________ 价。
(1)按要求从氢气、氯化钾、氧化钙、盐酸中选取合适的物质,将其化学式填写在下列横线上。
①一种可燃性气体
②一种可溶性的盐
③一种金属氧化物
④一种易挥发的酸
(2)化学与生活、社会发展息息相关。
①在每一餐中,我们都需要摄取足够的蛋白质、碳水化合物、脂肪和各种维生素。如玉米、胡萝卜中的叶黄素(化学式为C40H56O2),有助于维护视力持久度,减少视觉伤害。叶黄素属于
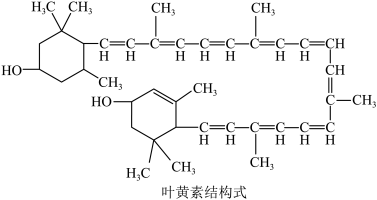
③生产电脑芯片的材料主要是高纯硅。工业上可用以下方法制取硅:2H2+SiCl4
 Si+4HCl,其反应类型为
Si+4HCl,其反应类型为
更新时间:2024-05-23 19:31:07
|
相似题推荐
填空与简答-推断题
|
适中
(0.65)
解题方法
【推荐1】如图“雪花”中的A、B、C、D、E、F是初中化学常见的六种物质。其中A是实验室常用的液体燃料,B是黑色固体,F能与血红蛋白结合。(其中部分反应物、生成物和反应条件都已省略,“一”表示物质间能相互发生反应,“→”表示物质间能发生转化)。请写出你的推断:
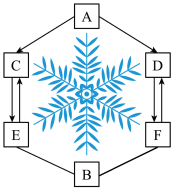
(1)写出物质的化学式:A___________ 、E___________ 。
(2)写出D→F的化学方程式_____________ 。
(3)图中所示的反应中,涉及的基本反应类型有___________ 。
(4)写出E与B反应的化学方程式_______________ 。

(1)写出物质的化学式:A
(2)写出D→F的化学方程式
(3)图中所示的反应中,涉及的基本反应类型有
(4)写出E与B反应的化学方程式
您最近一年使用:0次
填空与简答-科普阅读题
|
适中
(0.65)
解题方法
【推荐2】用化学方法改造物质
煤是一种重要的化工原料,我国是煤炭产量大国。气化是煤的主要利用途径之一,将煤加工转化为可作为工业或民用的煤气,常用的气化方法有以下两种:
空气煤气,以空气中的氧气作气化剂,得到的产物中主要有一氧化碳、氢气、甲烷、二氧化碳、硫化氢等。
水煤气:在高温条件下,水蒸气和碳反应,生成一氧化碳和氢气。
(1)初产品的空气煤气,通过碱溶液净化,可除去其中的(填化学式)_______ ,得到热值较高的家用燃料煤气。
(2)空气煤气的生产过程可以将一些灰分较高的劣质煤,通过转化充分利用。使用这样的燃料气与使用高灰分劣质煤相比,优点有(写一条)_______ 。
(3)用化学方程式表示水煤气的生产原理_______ ,该反应属于基本反应类型中的_______ ,从氧化一还原的角度分析,碳在反应中做(填“氧化剂”“还原剂”)_______ 。生产过程中需要持续提供热量,可以推断反应的能量转化过程为_______ 。
(4)写出水煤气主要成分之一燃烧的化学方程式_______ 。
煤是一种重要的化工原料,我国是煤炭产量大国。气化是煤的主要利用途径之一,将煤加工转化为可作为工业或民用的煤气,常用的气化方法有以下两种:
空气煤气,以空气中的氧气作气化剂,得到的产物中主要有一氧化碳、氢气、甲烷、二氧化碳、硫化氢等。
水煤气:在高温条件下,水蒸气和碳反应,生成一氧化碳和氢气。
(1)初产品的空气煤气,通过碱溶液净化,可除去其中的(填化学式)
(2)空气煤气的生产过程可以将一些灰分较高的劣质煤,通过转化充分利用。使用这样的燃料气与使用高灰分劣质煤相比,优点有(写一条)
(3)用化学方程式表示水煤气的生产原理
(4)写出水煤气主要成分之一燃烧的化学方程式
您最近一年使用:0次
填空与简答-推断题
|
适中
(0.65)
解题方法
【推荐3】下图是九年级化学中常见物质间的相互转化关系,A与C都是由相同两种元素组成的液体,A、C、E、G也为化合物,G为红棕色粉末,F为金属单质,其余反应条件、反应物和生成物均已省略。
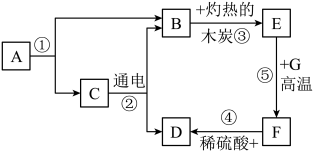
请根据上图推断:
(1)A的化学式______________ 、E的化学式 __________________ ;
(2)反应④的基本反应类型是________________ 反应;
(3)写出反应⑤的化学方程式__________________________________________________ 。

请根据上图推断:
(1)A的化学式
(2)反应④的基本反应类型是
(3)写出反应⑤的化学方程式
您最近一年使用:0次
填空与简答-科普阅读题
|
适中
(0.65)
解题方法
【推荐1】阅读下列短文,回答有关问题:
过氧化氢(H2O2)是一种绿色高效氧化剂,广泛应用于医药、食品和造纸等领域。
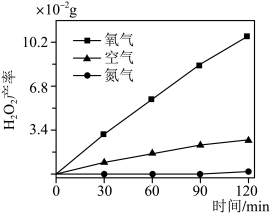
我国化学家通过静电纺丝辅助离子交换策略,制备出了梯型纤维异质结Nb2O5@NiS(NONS),作为光催化产过氧化氢的催化剂,实现无机复合光催化剂纯水过氧化氢光合成的新策略。实验测定在氧气、空气、氮气中过氧化氢的产率如图所示。
相较于以乙基蒽醌(C16H12O2)氧化法为主的传统制备方法,直接利用丰富的水和氧气为原料,以太阳能为能量来源的光催化合成过氧化氢对于促进太阳能源利用和实现“双碳”目标具有重要意义。
(1)写出实验室用过氧化氢溶液制取氧气的化学方程式_______ 。
(2)催化剂在反应前后的质量和_______ 不变。
(3)下列有关说法正确的是______。
(4)结合图分析,可得到的结论是_______ 。
过氧化氢(H2O2)是一种绿色高效氧化剂,广泛应用于医药、食品和造纸等领域。
我国化学家通过静电纺丝辅助离子交换策略,制备出了梯型纤维异质结Nb2O5@NiS(NONS),作为光催化产过氧化氢的催化剂,实现无机复合光催化剂纯水过氧化氢光合成的新策略。实验测定在氧气、空气、氮气中过氧化氢的产率如图所示。
相较于以乙基蒽醌(C16H12O2)氧化法为主的传统制备方法,直接利用丰富的水和氧气为原料,以太阳能为能量来源的光催化合成过氧化氢对于促进太阳能源利用和实现“双碳”目标具有重要意义。

(1)写出实验室用过氧化氢溶液制取氧气的化学方程式
(2)催化剂在反应前后的质量和
(3)下列有关说法正确的是______。
| A.乙基蒽醌中含有氧气 |
| B.光催化合成过氧化氢时太阳能转化为化学能 |
| C.过氧化氢和乙基蒽醌均属于氧化物 |
| D.实现“双碳”目标中“碳”是指碳元素 |
(4)结合图分析,可得到的结论是
您最近一年使用:0次
【推荐2】现有CO2、H2O、CH4、NO2(二氧化氮)、O3、SO2、NO(一氧化氮)等七种物质。
(1)其中不属于氧化物的是_________ 。
(2)二氧化硫与二氧化碳一样,都能与水发生化合反应。请写出二氧化硫与水反应的生成物的化学式_______ 。
(3)一氧化氮与氧气化合可生成二氧化氮,请写出反应的化学方程式___________ 。
(1)其中不属于氧化物的是
(2)二氧化硫与二氧化碳一样,都能与水发生化合反应。请写出二氧化硫与水反应的生成物的化学式
(3)一氧化氮与氧气化合可生成二氧化氮,请写出反应的化学方程式
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】化学用语是学习化学的重要工具。请用适当的化学符号填空。
(1)澄清石灰水中的溶质______ ;
(2)标出硫酸中硫元素的化合价______ ;
(3)2个氮分子______ ;
(4)两个镁离子______ 。
(1)澄清石灰水中的溶质
(2)标出硫酸中硫元素的化合价
(3)2个氮分子
(4)两个镁离子
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】下表是元素周期表的一部分,试回答下列问题
(1)写出①所示原子结构示意图_____ 。
(2)②所示元素与③所示元素形成化合物的化学式是_____ 。
| 第一周期 | 1 H | 2 He | ||||||
| 第二周期 | 3 Li | 4 Be | 5 B | ① | 7 N | 8 O | 9 F | 10 Ne |
| 第三周期 | ② | 12 Mg | 13 Al | 14 Si | 15 P | ③ | 17 Cl | 18 Ar |
(2)②所示元素与③所示元素形成化合物的化学式是
您最近一年使用:0次
填空与简答-科普阅读题
|
适中
(0.65)
【推荐1】认识氨气:材料:①氨气是无色有强烈的刺激气味的气体:②密度比空气小;③降温至-33.5℃可变为液态;④1体积水大约溶解700体积氨气,其水溶液显碱性;⑤在高温条件下分解生成氮气和氢气;⑥与氯化氢气体混合产生白烟(成分为氯化铵);⑦用于制液氮、氮水、硝酸、铵盐和胺类等。⑧工业上用氮气和氢气在高温高压催化剂作用下合成氨气;⑨实验室可用加热氯化铵和熟石灰两种固体的方法制取氨气
(1)物质的组成与结构。写出氨气的化学式并标注氮元素的化合价__________ ,由其化学式可获得关于氨气定量组成的信息是___________ (写一条)。
(2)物质的性质。阅读上文,归纳氨气的化学性质(至少两条)________________ 。
(3)物质的变化
I.用方程式表示工业和实验室制取氨气时发生的化学变化___________
II.变化③中不发生变化的是_____________ (填字母编号)。
a.氨分子的能量;
b.氨分子的运动速率;
c.氨分子的质量;
d.氨分子之间的相互作用;
e.氨分子的化学性质;
f.氨分子之间的间隔;
g.氨分子的构成
从微观的角度看变化③和⑥的本质区别是__________ 。
Ⅲ.描述变化⑤的微观过程_____________
(4)物质的制备
①工业制氨气所用催化剂可重复使用,其原因是_____________ 。
②实验室制取氨气应选取的发生装置______________ (填装置编号)是检查该装置气密性的方法是___________________ ,用D装置收集氨气时,验满的方法是_______________ ,将湿润的_____________ (填“红色”或“蓝色”)石蕊试纸。放在__________ (填“a”或“b”)处,观察到_________________ 证明集满。
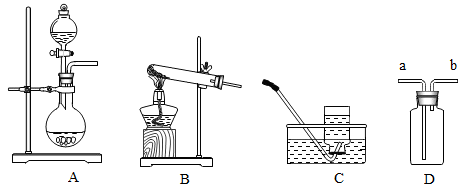
(1)物质的组成与结构。写出氨气的化学式并标注氮元素的化合价
(2)物质的性质。阅读上文,归纳氨气的化学性质(至少两条)
(3)物质的变化
I.用方程式表示工业和实验室制取氨气时发生的化学变化
II.变化③中不发生变化的是
a.氨分子的能量;
b.氨分子的运动速率;
c.氨分子的质量;
d.氨分子之间的相互作用;
e.氨分子的化学性质;
f.氨分子之间的间隔;
g.氨分子的构成
从微观的角度看变化③和⑥的本质区别是
Ⅲ.描述变化⑤的微观过程
(4)物质的制备
①工业制氨气所用催化剂可重复使用,其原因是
②实验室制取氨气应选取的发生装置

您最近一年使用:0次
【推荐2】在“碳达峰、碳中和”目标愿景下,氨气 作为一种零碳能源具有广泛应用前景。
作为一种零碳能源具有广泛应用前景。
(1)氨气易液化、方便储存和运输,含氢质量分数为_______ (精确到 ),是比较好的储氢介质。从微观角度解释氨气可以加压液化储存的原因
),是比较好的储氢介质。从微观角度解释氨气可以加压液化储存的原因_______ 。
(2)工业烟气中常含有 ,直接排放会造成
,直接排放会造成_______ 等环境问题。氨法脱硫是一种高效、低能耗的脱硫方式,最终产物 在农业上可作为
在农业上可作为_______ 。实验室检验铵根离子的方法是_______ 。
(3)如图是电解合成氨工艺综合利用流程图。_______ (选填“物理”或“化学”)变化。
②将氧气通入锅炉中进行富氧燃烧的意义是:燃烧速度快、_______ 。
③如图流程中产生氨气的反应总方程式为_______  。
。
④现有火力发电设施可以直接通入氨气燃烧,燃烧后会生成氮气和水,该化学反应方程式为_______ 。
(4)结合以上题目信息,谈一谈用氨气作为零碳能源可行性的理由:_______ 。
 作为一种零碳能源具有广泛应用前景。
作为一种零碳能源具有广泛应用前景。(1)氨气易液化、方便储存和运输,含氢质量分数为
 ),是比较好的储氢介质。从微观角度解释氨气可以加压液化储存的原因
),是比较好的储氢介质。从微观角度解释氨气可以加压液化储存的原因(2)工业烟气中常含有
 ,直接排放会造成
,直接排放会造成 在农业上可作为
在农业上可作为(3)如图是电解合成氨工艺综合利用流程图。
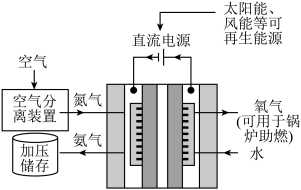
②将氧气通入锅炉中进行富氧燃烧的意义是:燃烧速度快、
③如图流程中产生氨气的反应总方程式为
 。
。④现有火力发电设施可以直接通入氨气燃烧,燃烧后会生成氮气和水,该化学反应方程式为
(4)结合以上题目信息,谈一谈用氨气作为零碳能源可行性的理由:
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】王强家菜地里的蔬菜叶色发黄。周日,爸爸叫王强去买化肥硝酸铵(NH4NO3),当他赶到商场时,硝酸铵刚好卖完。
(1)根据所学的化学知识,你建议他购买______ (填序号),也能起到与硝酸铵相同的作用。
①氯化钾 KCl ②尿素 CO(NH2)2 ③磷矿粉 Ca3(PO4)2
(2)硝酸铵是含氮量较高的化肥,硝酸铵中氮元素的质量分数为___________ 。
(3)硝酸铵不能与碱性物质混合施用是_________________________ 。
(1)根据所学的化学知识,你建议他购买
①氯化钾 KCl ②尿素 CO(NH2)2 ③磷矿粉 Ca3(PO4)2
(2)硝酸铵是含氮量较高的化肥,硝酸铵中氮元素的质量分数为
(3)硝酸铵不能与碱性物质混合施用是
您最近一年使用:0次

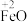 表示
表示 表示
表示



