有一种固体混合物质M,其中只可能含有Na2CO3、NaNO3、Na2SO4、CuCl2、BaCl2中的一种或几种。请根据以下实验操作回答下列问题。
操作I. 取少量M放入足量的水中充分搅拌、静置,得到白色沉淀和无色溶液,过滤。
操作II. 向滤出的沉淀中加入足量稀盐酸,沉淀全部溶解,此时所得溶液仍为无色。
(1)M中一定不含的物质是________________ ,不能确定是否含有的物质是_________ 。
(2)上述实验过程中,发生反应的化学方程式为_________________ 、_________________ 。
(3)向操作I后所得的无色溶液中滴加溶液AgNO3溶液,一定能发生的反应的化学方程式为_________________________________________________ 。
操作I. 取少量M放入足量的水中充分搅拌、静置,得到白色沉淀和无色溶液,过滤。
操作II. 向滤出的沉淀中加入足量稀盐酸,沉淀全部溶解,此时所得溶液仍为无色。
(1)M中一定不含的物质是
(2)上述实验过程中,发生反应的化学方程式为
(3)向操作I后所得的无色溶液中滴加溶液AgNO3溶液,一定能发生的反应的化学方程式为
更新时间:2016-11-28 13:03:17
|
相似题推荐
【推荐1】建立宏观、微观和符号之间的相互联系是化学学科的特点。
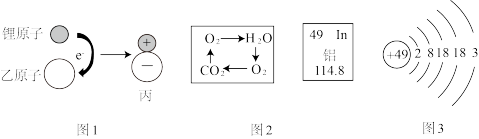
(1)图1表示锂原子与乙原子形成化合物丙的微观过程。
①该过程说明原子通过___________ 形成离子。
②写出符合该过程形成的化合物丙的化学式___________ 。(图中微粒大小忽略不计)
(2)图2表示水、二氧化碳和氧气的循环图。从宏观角度看,图中三种物质的组成中都含有_______ ,从微观角度看,图中三种物质都是由___________ 构成的。
(3)图3是铟元素在元素周期表中的部分信息,根据图3回答下列问题。
①铟属于_______ (填“金属”或“非金属”)元素,图3中“114.8”表示的是铟元素的________ ;
②铟与氯气反应生成氯化铟的微观过程表示如图4,请将B框中的信息补充完整______ 。(已知:氯气与氧气的微粒结构类似)
③写出如图反应过程的符号表达式:___________ 。


(1)图1表示锂原子与乙原子形成化合物丙的微观过程。
①该过程说明原子通过
②写出符合该过程形成的化合物丙的化学式
(2)图2表示水、二氧化碳和氧气的循环图。从宏观角度看,图中三种物质的组成中都含有
(3)图3是铟元素在元素周期表中的部分信息,根据图3回答下列问题。
①铟属于
②铟与氯气反应生成氯化铟的微观过程表示如图4,请将B框中的信息补充完整
③写出如图反应过程的符号表达式:

您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐2】过氧化钙晶体﹝CaO2·8H2O﹞较稳定,呈白色,微溶于水,广泛应用于环境杀菌、消毒。以贝壳为原料制备CaO2流程如下:

(1)气体X是__________ ;将过氧化钙晶体与溶液分离的方法是_________ 。
(2)反应Y需控制温度在0~5℃,可将反应容器放在冰水混合物中,反应产物是CaO2·8H2O,请写出化学方程式_______________________ ,该反应的基本反应类型是_________ 。获得的过氧化钙晶体中常含有Ca(OH)2杂质,原因是______________________ 。

(1)气体X是
(2)反应Y需控制温度在0~5℃,可将反应容器放在冰水混合物中,反应产物是CaO2·8H2O,请写出化学方程式
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】在宏观、微观和符号之间建立联系是化学学科的特点。甲、乙、丙、丁、戊五种物质,它们的部分化学式和微观示意图分别列于下表中、
(1)甲物质燃烧的化学方程式______ 。
(2)五种物质中,有可燃性的氧化物是______ (填项目序号,下同),属于清洁能源的是______ 。
(3)根据下列选项回答:物质在化学变化前后,可能变化的是______ (填序号,下同),一定变化的是______ 。
①原子种类 ②原子数目 ③分子数目 ④元素种类 ⑤元素化合价 ⑥分子种类
| 项目 | 甲 | 乙 | 丙 | 丁 | 戊 |  |
| 化学式 | ? | H2O | CO | H2 | CO2 | |
| 微观示意图 |  |  |  | 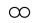 |  |
(2)五种物质中,有可燃性的氧化物是
(3)根据下列选项回答:物质在化学变化前后,可能变化的是
①原子种类 ②原子数目 ③分子数目 ④元素种类 ⑤元素化合价 ⑥分子种类
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐1】海水素有“液体工业原料”之美誉。工业“从海水中提取镁”的主要流程如下:
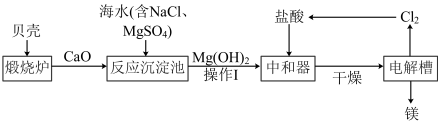
(1)煅烧炉中,发生反应的化学方程式为:CaCO3 CaO+CO2↑,此反应属于基本类型中的
CaO+CO2↑,此反应属于基本类型中的 ______ 反应。
(2)反应沉淀池中发生如下反应:
①CaO+H2O=Ca(OH)2;
②Ca(OH)2+ MgSO4= CaSO4 + Mg(OH)2↓,
操作Ⅰ为_________ 。
(3)电解槽中,能生成镁的反应物为____________ 。
(4)从海水中提取镁的过程中,镁元素的化合价变化为__________ 。

(1)煅烧炉中,发生反应的化学方程式为:CaCO3
 CaO+CO2↑,此反应属于基本类型中的
CaO+CO2↑,此反应属于基本类型中的 (2)反应沉淀池中发生如下反应:
①CaO+H2O=Ca(OH)2;
②Ca(OH)2+ MgSO4= CaSO4 + Mg(OH)2↓,
操作Ⅰ为
(3)电解槽中,能生成镁的反应物为
(4)从海水中提取镁的过程中,镁元素的化合价变化为
您最近一年使用:0次
填空与简答-推断题
|
适中
(0.65)
解题方法
【推荐2】A、B、C、D四种化合物,在日常家庭生活中都得到广泛应用。其中A、B通常情况下为液体,C、D为固体。A是生命之源,人们每天都必须饮用它;B是一种调味品的主要成分,用该调味品可除去水壶中的水垢;C常用作干果的干燥剂;把D加入经发酵后的面团中,能使馒头松软可口。回答下列问题。
(1)上述调味品是__________ ,C的俗称是___________ 。
(2)把适量的A滴到一小块C上,产生大量的A蒸气,其原因是_________________ 。
(3)写出A与C反应的产物的溶液跟D的溶液反应的化学方程式:______________ ,该反应类型是_____________________ 。
(1)上述调味品是
(2)把适量的A滴到一小块C上,产生大量的A蒸气,其原因是
(3)写出A与C反应的产物的溶液跟D的溶液反应的化学方程式:
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐3】以镁矿石(主要成分MgCO3、SiO2)为原料生产MgO的主要工艺流程如图:
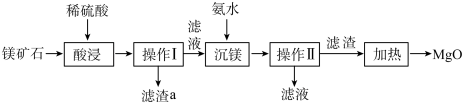
已知:“沉镁”过程中有Mg(OH)2生成,Mg(OH)2加热会分解得到两种氧化物。
(1)“酸浸”前,通常要将镁矿石粉碎,其目的是______ ,该过程中的化学方程式是______ 。
(2)操作I、II中需要用到的玻璃仪器是_______ 。
(3)经查验滤渣a的主要成分是SiO2,其中硅元素的化合价是______ 价。
(4)“加热”过程中的另一种产物的化学式是______ 。

已知:“沉镁”过程中有Mg(OH)2生成,Mg(OH)2加热会分解得到两种氧化物。
(1)“酸浸”前,通常要将镁矿石粉碎,其目的是
(2)操作I、II中需要用到的玻璃仪器是
(3)经查验滤渣a的主要成分是SiO2,其中硅元素的化合价是
(4)“加热”过程中的另一种产物的化学式是
您最近一年使用:0次
填空与简答-推断题
|
适中
(0.65)
【推荐1】有一包粉末,可能由KCl、K2SO4、K2CO3、CuCl2、MgCl2中的一种或几种物质组成。现在做如下实验:
(1)根据以下实验操作及现象,请回答:
实验1:取少量粉末,加水溶解,得到无色透明溶液。
实验2:取1所得溶液少许,加入NaOH溶液,看不到明显现象。
实验3:取1所得溶液少许,加入适量硝酸钡溶液,出现白色沉淀。
实验4:将实验3所得混合物过滤后,在沉淀中加入足量稀硝酸,沉淀部分溶解并有气泡生成。
原粉末中一定没有___________ ,原粉末中一定有___________ 。
(2)据上述实验现象,可推知原粉末中可能有,为了进一步验证原粉末中可能含有的成分是否存在,请你设计实验证明:
(1)根据以下实验操作及现象,请回答:
实验1:取少量粉末,加水溶解,得到无色透明溶液。
实验2:取1所得溶液少许,加入NaOH溶液,看不到明显现象。
实验3:取1所得溶液少许,加入适量硝酸钡溶液,出现白色沉淀。
实验4:将实验3所得混合物过滤后,在沉淀中加入足量稀硝酸,沉淀部分溶解并有气泡生成。
原粉末中一定没有
(2)据上述实验现象,可推知原粉末中可能有,为了进一步验证原粉末中可能含有的成分是否存在,请你设计实验证明:
| 操作步骤 | 现象 | 结论 |
| 该物质不存在 |
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
真题
名校
【推荐2】2020年奥运会奖牌制作原料来自于电子垃圾中提炼出来的金属。从废线路板中提炼贵重金属和制备硫酸铜晶体的一种工艺流程如下:
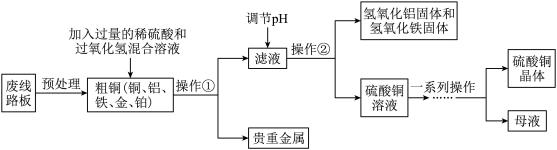
已知:在酸性环境中有过氧化氢存在时,铁和铜分别会转化为铁离子和铜离子。
(1)操作①的名称是______ ;
(2)提炼出的贵金属可制作奖牌,其成分是______ ;
(3)调节pH的主要目的是除去滤液中_____ (填金属离子符号);
(4)写出粗铜中的铜和过氧化氢的混合溶液发生反应的化学方程式:______ 。

已知:在酸性环境中有过氧化氢存在时,铁和铜分别会转化为铁离子和铜离子。
(1)操作①的名称是
(2)提炼出的贵金属可制作奖牌,其成分是
(3)调节pH的主要目的是除去滤液中
(4)写出粗铜中的铜和过氧化氢的混合溶液发生反应的化学方程式:
您最近一年使用:0次
填空与简答-简答题
|
适中
(0.65)
【推荐3】有一包白色粉末可能含有硫酸钡、碳酸钾和氢氧化钡中的一种或几种,取一定量该粉末加入到盛有足量水的烧杯中,搅拌、静置,观察到烧杯中有白色不溶物。
友情提示:氯化钡溶液为中性。
(1)不能确定白色粉末中一定含有硫酸钡,其理由(化学方程式表示) 。
(2)进一步确定白色固体成分,进行如下实验探究:

Ⅰ.步骤②中发生化学反应的方程式是 ;
Ⅱ.
(3)取少量滤渣B,加入过量的稀硝酸,若看到的现象是 , 就足以说明原白色粉末中只含有碳酸钾和氢氧化钡。
友情提示:氯化钡溶液为中性。
(1)不能确定白色粉末中一定含有硫酸钡,其理由(化学方程式表示) 。
(2)进一步确定白色固体成分,进行如下实验探究:

Ⅰ.步骤②中发生化学反应的方程式是 ;
Ⅱ.
| 实验操作 | 现象 | 结论 |
| 步骤③中,加入酚酞溶液 | 若溶液E为无色 | 原白色粉末的组成是 ; |
| 若溶液E为红色 | 滤液A中一定含有的溶质是 , 原白色粉末的可能组成分别是 。 |
(3)取少量滤渣B,加入过量的稀硝酸,若看到的现象是 , 就足以说明原白色粉末中只含有碳酸钾和氢氧化钡。
您最近一年使用:0次
填空与简答-推断题
|
适中
(0.65)
【推荐1】有一包粉末,可能由KCl、K2SO4、K2CO3、CuCl2、MgCl2中的一种或几种物质组成。现在做如下实验:
(1)根据以下实验操作及现象,请回答:
实验1:取少量粉末,加水溶解,得到无色透明溶液。
实验2:取1所得溶液少许,加入NaOH溶液,看不到明显现象。
实验3:取1所得溶液少许,加入足量硝酸钡溶液,出现白色沉淀。
实验4:将实验3所得混合物过滤后,在沉淀中加入足量稀硝酸,沉淀部分溶解并有气泡生成。原粉末中一定有_______________________ 。实验4中沉淀部分溶解的化学方程式为:____________________________ 。
(2)据上述实验现象,可推知原粉末中可能有______________ ,为了进一步验证原粉末中可能含有的成分是否存在,请你设计实验证明:
(1)根据以下实验操作及现象,请回答:
实验1:取少量粉末,加水溶解,得到无色透明溶液。
实验2:取1所得溶液少许,加入NaOH溶液,看不到明显现象。
实验3:取1所得溶液少许,加入足量硝酸钡溶液,出现白色沉淀。
实验4:将实验3所得混合物过滤后,在沉淀中加入足量稀硝酸,沉淀部分溶解并有气泡生成。原粉末中一定有
(2)据上述实验现象,可推知原粉末中可能有
操作步骤 | 现 象 | 结 论 |
该物质存在 |
您最近一年使用:0次
填空与简答-推断题
|
适中
(0.65)
解题方法
【推荐2】某固体样品中除含氯化钾外,可能含有氢氧化钾、硫酸钾、氢氧化钡、硝酸钾中的一种或几种,某兴趣小组为探究其成分做了以下实验:
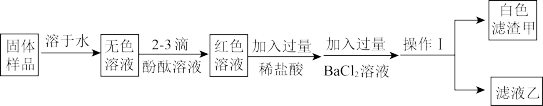
(1)原固体样品溶于水后pH______ 7(选填“大于”“小于”等于”)。
(2)操作Ⅰ的名称是______ ,生成白色滤渣甲的化学方程式为______ 。
(3)滤液乙中一定大量存在的阳离子有K+、______ (用离子符号表示)。
(4)该固体样品中一定不存在的物质是______ 。
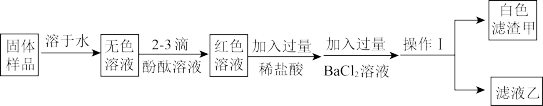
(1)原固体样品溶于水后pH
(2)操作Ⅰ的名称是
(3)滤液乙中一定大量存在的阳离子有K+、
(4)该固体样品中一定不存在的物质是
您最近一年使用:0次



