遂宁境内的卓筒井是手工制盐的活化石,被誉为“中国古代第五大发明”、“世界石油钻井之父”,不仅是古代劳动人民勤劳、智慧的象征,也造福了千秋万代。其工艺流程包括下面五个步骤:

请结合所学化学知识,回答下列问题:
(1)第②步汲出的卤水浑浊,浓度一般在7~10度(即溶质质量分数为7%~10%,下同),这样的卤水咸度低,耗燃料,成本高,为了把卤水浓度提高18~20度,就产生了“晒卤”这一环节。在“晒卤”的过程中溶液溶质质量分数_____ (填“不变”、“变大”或“变小”)。
(2)第④步“滤卤”和实验室“过滤”的原理一样,都是为了除去液体中的不溶性杂质。在实验室的过滤操作中,必须用到的玻璃仪器有:烧杯、玻璃棒、____ ,其中玻璃棒的作用是____ 。
(3)第⑤步“煎盐”和实验室___ 结晶(填结晶的方法)的原理相同。
(4)如图是甲、乙、丙三种物质的溶解度曲线图,
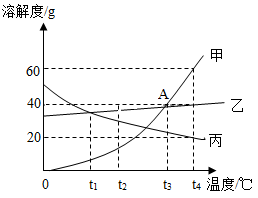
据图回答下列问题:
Ⅰ.甲、乙两种物质在___ ℃时溶解度相同。
Ⅱ.t2℃时,甲、乙、丙三种物质溶解度由大到小排列为______ 。
Ⅲ.t4℃时,将三种物质各ag分别加入100g水中,充分溶解后,只有一种能形成饱和溶液,则a的取值范围是__________ 。

请结合所学化学知识,回答下列问题:
(1)第②步汲出的卤水浑浊,浓度一般在7~10度(即溶质质量分数为7%~10%,下同),这样的卤水咸度低,耗燃料,成本高,为了把卤水浓度提高18~20度,就产生了“晒卤”这一环节。在“晒卤”的过程中溶液溶质质量分数
(2)第④步“滤卤”和实验室“过滤”的原理一样,都是为了除去液体中的不溶性杂质。在实验室的过滤操作中,必须用到的玻璃仪器有:烧杯、玻璃棒、
(3)第⑤步“煎盐”和实验室
(4)如图是甲、乙、丙三种物质的溶解度曲线图,

据图回答下列问题:
Ⅰ.甲、乙两种物质在
Ⅱ.t2℃时,甲、乙、丙三种物质溶解度由大到小排列为
Ⅲ.t4℃时,将三种物质各ag分别加入100g水中,充分溶解后,只有一种能形成饱和溶液,则a的取值范围是
2013·四川遂宁·中考真题 查看更多[5]
更新时间:2016-11-28 11:36:34
|
相似题推荐
综合应用题
|
适中
(0.65)
【推荐1】高纯碳酸钙广泛应用于精密电子陶瓷、医药等的生产,某兴趣小组按图所示实验步骤,模拟工业流程制备高纯碳酸钙,请回答下列问题。

(1)“酸溶”过程中,将一定浓度的盐酸缓慢加入粉碎后的优质石灰石中,同时搅拌。搅拌的目的是______ 。
(2)“操作1”的名称______ ,需要用到的玻璃仪器有烧杯、玻璃棒和______ ,其中玻璃棒的作用是______ 。
(3)如下图是“操作2”得到的“滤液”中所含溶质的溶解度曲线,在同一温度下,结晶出的物质是______ ,理由是______ 。

(4)上述流程中可循环利用的物质是______ 。
(5)为了测定高纯碳酸钙中碳酸钙的质量分数,进行如下实验(样品中除碳酸钙外,其余的成分既不与盐酸反应,也不溶于水),实验与所得的数据如下表:(每次取用的石灰石样品的质量相同,稀盐酸质量分数也相同)。
①计算上述表格中的m值______ 。
②实验中碳酸钙的质量分数是______ 。
③计算该稀盐酸的溶质质量分数______ (结果精确到0.1%)(写出计算过程)。

(1)“酸溶”过程中,将一定浓度的盐酸缓慢加入粉碎后的优质石灰石中,同时搅拌。搅拌的目的是
(2)“操作1”的名称
(3)如下图是“操作2”得到的“滤液”中所含溶质的溶解度曲线,在同一温度下,结晶出的物质是

(4)上述流程中可循环利用的物质是
(5)为了测定高纯碳酸钙中碳酸钙的质量分数,进行如下实验(样品中除碳酸钙外,其余的成分既不与盐酸反应,也不溶于水),实验与所得的数据如下表:(每次取用的石灰石样品的质量相同,稀盐酸质量分数也相同)。
| 实验 | 第一次 | 第二次 | 第三次 |
| 取用石灰石样品的质量/g | m | m | m |
| 取用稀盐酸的质量/g | 30 | 60 | 90 |
| 反应后过滤得到固体的质量(已干燥)/g | 6 | 2 | 1 |
②实验中碳酸钙的质量分数是
③计算该稀盐酸的溶质质量分数
您最近一年使用:0次
【推荐1】水是一切生合体生在所必委的物质。
(1)爱护水资源,在节约用水的同时防治水体污染,下列做法合理的是_____(填标号)。
(2)①某同学从三河中取间水样、用自制冷水器处理,净水器中活性炭可以_____ (填“吸附”或“蒸馏”)水样中的异味和色素。
②向处理后的水样中加入肥皂水,振荡。观察到泡沫较少,浮渣较多,则该水样属于_____ (填“硬水”或“软水")。
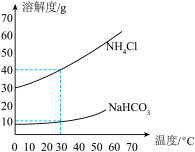
(3)碳酸氢钠和氯化铵的溶解度曲线如图所示。下列说法正确的是_____。
(1)爱护水资源,在节约用水的同时防治水体污染,下列做法合理的是_____(填标号)。
| A.水龙头漏水不及时更换 | B.生活河水集中处理和排放 |
| C.洗脸水冲厕所 | D.农业上合理使用农药和化肥 |
②向处理后的水样中加入肥皂水,振荡。观察到泡沫较少,浮渣较多,则该水样属于
(3)碳酸氢钠和氯化铵的溶解度曲线如图所示。下列说法正确的是_____。

| A.30℃时,NaHCO3的溶解度是40g |
| B.30℃时,饱和溶液的溶质质量分数NH4Cl小于NaHCO3 |
| C.将50℃时NH4Cl的饱和溶液降低到10℃,该饱和溶液的溶质质量分数变大 |
| D.饱和NaCl溶液通NH3至饱和再通入CO2,生成NaHCO3和NH4Cl,NaHCO3将结晶析出 |
您最近一年使用:0次
【推荐2】请利用所学化学知识回答下列问题:
(1)识别标签:如图为某天然矿泉水的标签。
①请写出该标签中硫酸根的离子符号________ 。
②可以用______ 来检验该矿泉水是硬水还是软水。
③若该瓶矿泉水为2L,根据标签中的信息,则至少含有钾离子__________ mg。
④写出由钙离子与氯离子构成的物质的化学式_______ 。
(2)健康生活:防疫情,测体温。体温测量仪功不可没。
①传统型——体温计。因为汞是人体中的________ (选填“必需”或“有害”)元素,含汞体温计将在2026年起全面禁止生产。汞的元素符号是__________ 。
②方便型——额温枪。某种额温枪的红外温度传感器所用材料含有钽酸锂(LiTaO3)。钽酸锂中锂元素(Li)的化合价为+1价,则钽元素(Ta)的化合价为________ 价。
(3)节能减排:节能减排中“减排”的一个重要手段是合理利用二氧化碳。科学家在一定条件下将二氧化碳转化为甲烷,其反应的微观过程如下图所示。

①甲、乙、丙、丁四种物质中属于氧化物的是_____ (填化学式)。
②该反应的化学方程式是______ 。
③通过分析该反应的微观过程。对于化学变化,从微观角度可以获得的信息是______ 。(写出一条即可)
(4)资源利用:盐田法是海水制盐的方法之一,其流程如图1所示。

①图1中M是________ 池(填“蒸发”或“冷却”),结合图2的溶解度曲线,说明用盐田法从海水中制取氯化钠的理由是_______ 。
②由图2可知硝酸钾在t2℃时的溶解度为_________ 。
(1)识别标签:如图为某天然矿泉水的标签。
| 水质主要成分(mg/L) K+:0.62~ 3.25 Na+:18.75 ~ 29.8 Ca2+:17.8 ~ 26.2 Cl-:14.2 ~ 30.8 硫酸根:41.6~70.2 碳酸氢根:184~261 |
②可以用
③若该瓶矿泉水为2L,根据标签中的信息,则至少含有钾离子
④写出由钙离子与氯离子构成的物质的化学式
(2)健康生活:防疫情,测体温。体温测量仪功不可没。
①传统型——体温计。因为汞是人体中的
②方便型——额温枪。某种额温枪的红外温度传感器所用材料含有钽酸锂(LiTaO3)。钽酸锂中锂元素(Li)的化合价为+1价,则钽元素(Ta)的化合价为
(3)节能减排:节能减排中“减排”的一个重要手段是合理利用二氧化碳。科学家在一定条件下将二氧化碳转化为甲烷,其反应的微观过程如下图所示。

①甲、乙、丙、丁四种物质中属于氧化物的是
②该反应的化学方程式是
③通过分析该反应的微观过程。对于化学变化,从微观角度可以获得的信息是
(4)资源利用:盐田法是海水制盐的方法之一,其流程如图1所示。

①图1中M是
②由图2可知硝酸钾在t2℃时的溶解度为
您最近一年使用:0次
【推荐3】海洋是个巨大的资源宝库。海水淡化、海水晒盐等对海洋资源的充分利用,体现了人类认识物质、改造物质的智慧。
(1)采用如图所示的膜分离法淡化海水,水分子可以通过淡化膜进入左侧的淡水池,从而得到淡水。下列说法中,不合理的是 (填选项序号之一)。

(2)采用盐田法晒盐,经日晒、风吹等,结晶池中会有氯化钠晶体析出,此时结晶池中的溶液为氯化钠的________ (填“饱和”或“不饱和”之一)溶液。该过程主要通过________ (选填“降温结晶”或“蒸发结晶”之一)使食盐析出。
(3)下图是粗盐在工业生产中的一种应用流程,请根据信息回答问题:
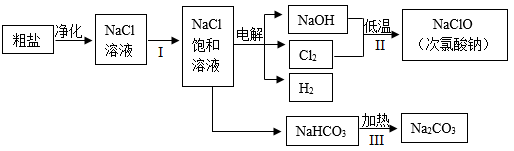
①除去粗盐中的难溶性杂质,可采用的操作是_________ (填选项序号A.蒸发 B.蒸馏 C.过滤D.溶解),该操作中玻璃棒的作用是______
②步骤 Ⅱ 中用烧碱低温制取次氯酸钠的反应原理为:Cl2+2NaOH=X+NaClO+H2O,则X的化学式是_____ ,NaClO中氯元素的化合价为_________ 。
③氯化钠溶液在通电情况下生成NaOH、Cl2和H2,写出其反应的化学方程式:_____________ 。
(4)海水中除了蕴含大量的钠元素和镁元素外,还含有大量的钾元素,NaCl和KNO3的溶解度曲线如图所示,试回答下列问题:
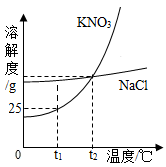
①在t2℃时,KNO3的溶解度_____ NaCl的溶解度(选填“大于”、“等于”或“小于”之一)。
②在t1℃时,KNO3饱和溶液的溶质质量分数是______ ,该温度下,将15g硝酸钾放入50g水中,可以得到 _______ g KNO3溶液。
③t1℃时分别将KNO3的饱和溶液及NaCl的饱和溶液升温到t2℃,此时KNO3溶质质量分数_________ (选填“大于”“小于”或“等于”之一)NaCl溶质质量分数。
(1)采用如图所示的膜分离法淡化海水,水分子可以通过淡化膜进入左侧的淡水池,从而得到淡水。下列说法中,不合理的是 (填选项序号之一)。

| A.膜分离法也是一种分离混合物的方法 |
| B.膜分离法较传统蒸馏法更节约能源 |
| C.加压后右侧海水中溶质质量分数增大 |
| D.加压后右侧海水的溶质质量增多 |
(3)下图是粗盐在工业生产中的一种应用流程,请根据信息回答问题:

①除去粗盐中的难溶性杂质,可采用的操作是
②步骤 Ⅱ 中用烧碱低温制取次氯酸钠的反应原理为:Cl2+2NaOH=X+NaClO+H2O,则X的化学式是
③氯化钠溶液在通电情况下生成NaOH、Cl2和H2,写出其反应的化学方程式:
(4)海水中除了蕴含大量的钠元素和镁元素外,还含有大量的钾元素,NaCl和KNO3的溶解度曲线如图所示,试回答下列问题:

①在t2℃时,KNO3的溶解度
②在t1℃时,KNO3饱和溶液的溶质质量分数是
③t1℃时分别将KNO3的饱和溶液及NaCl的饱和溶液升温到t2℃,此时KNO3溶质质量分数
您最近一年使用:0次
综合应用题
|
适中
(0.65)
【推荐1】下表是氯化铵在不同温度下的溶解度:
(1)从表中可知:随温度升高氯化铵的溶解度_____________ 。
(2)A烧杯是70℃时,溶剂为100g的氯化铵不饱和溶液,经过如下图的变化过程(在整个过程中不考虑水分的蒸发)。
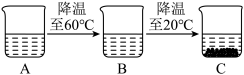
①C烧杯溶液中溶质的质量为_________ g。
②70℃时,将A烧杯中的溶液恒温蒸发10g溶剂后,析出ag固体,再继续恒温蒸发30g溶剂,则析出固体b g,则b g________ 3a g溶剂(填“<、≤、>、≥或=”)。
③配置一定溶质质量分数的氯化铵溶液的一些操作步骤见下图,正确的操作顺序是____ 。

| 温度(℃) | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 |
| 溶解度(g/100g水) | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 | 55.0 | 60.2 |
(2)A烧杯是70℃时,溶剂为100g的氯化铵不饱和溶液,经过如下图的变化过程(在整个过程中不考虑水分的蒸发)。

①C烧杯溶液中溶质的质量为
②70℃时,将A烧杯中的溶液恒温蒸发10g溶剂后,析出ag固体,再继续恒温蒸发30g溶剂,则析出固体b g,则b g
③配置一定溶质质量分数的氯化铵溶液的一些操作步骤见下图,正确的操作顺序是

您最近一年使用:0次
【推荐2】水是构成一切生物体的基本成分,是生命之源。
(1)验证水的组成。
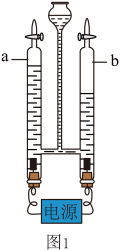

I、观察图1,b管连接的是电源______ (选填“正”或“负”)极,电解水的化学方程式是______ 。
II、分析图2,点燃氢气前,可选用______ 干燥氢气(填序号)。
A.生石灰 B.熟石灰 C.无水硫酸铜 D.硫酸铜晶体
“干燥氢气”的目的是______ 。
(2)水是一种常用的溶剂,不同物质在水中的溶解能力不同。
下表是NaCl、CaCl2的部分溶解度数据:
由上表可知,20℃时,NaCl的溶解度是______ g/100g水;60℃时,10g水中最多能溶解CaCl2______ g。
(3)某NaCl样品中混有少量CaCl2,可利用两物质溶解度的差异进行提纯。称取30g样品进行如下实验:
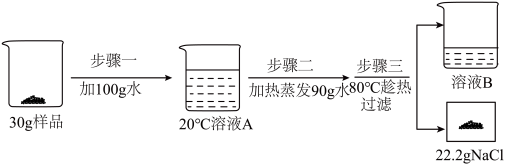
I、溶液A是该温度下NaCl的______ (填“饱和”或“不饱和”)溶液。
II、30g样品中含CaCl2的质量是______ g。
III、分析上述实验,说明步骤三趁热过滤的温度保持在60℃还是80℃更合适?请结合相关数据分析说明______
(1)验证水的组成。


I、观察图1,b管连接的是电源
II、分析图2,点燃氢气前,可选用
A.生石灰 B.熟石灰 C.无水硫酸铜 D.硫酸铜晶体
“干燥氢气”的目的是
(2)水是一种常用的溶剂,不同物质在水中的溶解能力不同。
下表是NaCl、CaCl2的部分溶解度数据:
| 温度(℃) | 20 | 40 | 60 | 80 | 100 |
| 溶解度(g/100g水) | NaCl | 36.0 | 36.6 | 37.1 | 38.0 |
| CaCl2 | 27.6 | 39.8 | 41.4 | 43.2 |
(3)某NaCl样品中混有少量CaCl2,可利用两物质溶解度的差异进行提纯。称取30g样品进行如下实验:

I、溶液A是该温度下NaCl的
II、30g样品中含CaCl2的质量是
III、分析上述实验,说明步骤三趁热过滤的温度保持在60℃还是80℃更合适?请结合相关数据分析说明
您最近一年使用:0次
【推荐3】我国化学家侯德榜创立的“侯氏制碱法”促进了世界制碱技术的发展,图1所示为其主要生产流程,图2是NH4CI和NaCl的溶解度曲线,请根据信息回答下列问题。

(1)操作a的名称是_________ ,生产流程中可循环利用的物质除水外还有_________ 。
(2)反应Ⅱ碳酸氢钠受热分解的化学反应方程式为_________ 。
(3)将20℃时NaCl的饱和溶液降温到t℃,该过程中发生改变的量是 。
(4)20℃时,将18gNaCl溶于水制成饱和溶液,需加入水的质量是_________ 。
(5)下列说法或操作不正确的是 (填字母序号);

(1)操作a的名称是
(2)反应Ⅱ碳酸氢钠受热分解的化学反应方程式为
(3)将20℃时NaCl的饱和溶液降温到t℃,该过程中发生改变的量是 。
| A.溶液质量 | B.溶质质量 |
| C.溶剂质量 | D.NaCl的溶解度 |
| E.溶质质量分数 | |
(5)下列说法或操作不正确的是 (填字母序号);
| A.配制(4)所需溶液时需要用到玻璃棒引流 |
| B.配制(4)所需溶液,量取水时,俯视方法读数,配制的氯化钠溶液中溶质的质量分数将偏大 |
| C.NaCl溶液中混有少量的NH4Cl,提纯NaCl的常用方法是降温结晶 |
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐1】第24届冬奥会于2022年2月4日在北京隆重举行,本届冬奥会体现了绿色办奥的理念。
(1)如图是以物质类别为横坐标、碳的化合价为纵坐标制成的碳元素“价类二维图”。回答下列问题:(已知:由金属离子和酸根离子构成的化合物称为盐)

①b点物质化学式______ 。
②写出由d转化为c化学方程式______ 。
(2)冬奥会利用废旧电子设备回收金、银来制作奖牌。从废旧电子粗产品中回收金、银的部分流程如下:

①操作I的名称是______ ,该操作用到玻璃仪器有玻璃棒、烧杯、______ 。
②写出步骤一的化学方程式______ 。(写其中一道即可)
③步骤二中加入硝酸银溶液的作用是______ 。
(1)如图是以物质类别为横坐标、碳的化合价为纵坐标制成的碳元素“价类二维图”。回答下列问题:(已知:由金属离子和酸根离子构成的化合物称为盐)

①b点物质化学式
②写出由d转化为c化学方程式
(2)冬奥会利用废旧电子设备回收金、银来制作奖牌。从废旧电子粗产品中回收金、银的部分流程如下:

①操作I的名称是
②写出步骤一的化学方程式
③步骤二中加入硝酸银溶液的作用是
您最近一年使用:0次
【推荐2】为测定氯化钠和碳酸钠固体混合物中氯化钠的质量分数,有以下两个实验方案:

(1)【方案1】
请问:①操作II的名称是_________
②X的化学式为_________ (写一种)
(2)【方案2】 通过测定样品和足量硫酸溶液反应产生气体的质量来计算样品中氯化钠的质量分数。
①若测得各物质的质量(g):样品质量为m1,所用硫酸溶液质量为m2,完全反应后混合溶液质量为m3,则生成气体的质量为___________ g。(用m1、m2、m3表示)
②请你再设计一种测定生成气体质量的方法,并注明需要测定哪些数据?____
【拓展提高】有人提出还有第三种方案:可用AgNO3溶液作为试剂,通过称量沉淀质量来确定氯化钠的质量?你认为是否可行,为什么?____

(1)【方案1】
请问:①操作II的名称是
②X的化学式为
(2)【方案2】 通过测定样品和足量硫酸溶液反应产生气体的质量来计算样品中氯化钠的质量分数。
①若测得各物质的质量(g):样品质量为m1,所用硫酸溶液质量为m2,完全反应后混合溶液质量为m3,则生成气体的质量为
②请你再设计一种测定生成气体质量的方法,并注明需要测定哪些数据?
【拓展提高】有人提出还有第三种方案:可用AgNO3溶液作为试剂,通过称量沉淀质量来确定氯化钠的质量?你认为是否可行,为什么?
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐3】化学就在我们身边,人类的衣食住行都离不开化学。请回答:
(1)外出时,佩戴口罩可以在一定程度上防止悬浮颗粒吸入鼻腔,其作用与_______ (填实验操作)类似。
(2)为了提高免疫力,妈妈为小强准备了下列食物:米饭、红烧肉、黄瓜,其中能为人体提供蛋白质的是______ 。
(3)居家消毒时,切勿将“84”消毒液与洁厕灵等强酸类清洗剂混合使用,因为两者相遇会发生如下反应 ,请写出物质R的化学式:
,请写出物质R的化学式:________ 。
(4)过氧乙酸(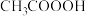 )的结构示意图为
)的结构示意图为 ,含有“过氧基”结构(如图方框部分)的物质都具有杀菌消毒作用。据此推测以下物质可用作杀菌消毒剂的为________。
,含有“过氧基”结构(如图方框部分)的物质都具有杀菌消毒作用。据此推测以下物质可用作杀菌消毒剂的为________。
(1)外出时,佩戴口罩可以在一定程度上防止悬浮颗粒吸入鼻腔,其作用与
(2)为了提高免疫力,妈妈为小强准备了下列食物:米饭、红烧肉、黄瓜,其中能为人体提供蛋白质的是
(3)居家消毒时,切勿将“84”消毒液与洁厕灵等强酸类清洗剂混合使用,因为两者相遇会发生如下反应
 ,请写出物质R的化学式:
,请写出物质R的化学式:(4)过氧乙酸(
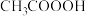 )的结构示意图为
)的结构示意图为 ,含有“过氧基”结构(如图方框部分)的物质都具有杀菌消毒作用。据此推测以下物质可用作杀菌消毒剂的为________。
,含有“过氧基”结构(如图方框部分)的物质都具有杀菌消毒作用。据此推测以下物质可用作杀菌消毒剂的为________。| A.H-O-H | B.O=C=O | C.H-O-O-H |
您最近一年使用:0次



