水是构成一切生物体的基本成分,是生命之源。
(1)验证水的组成。
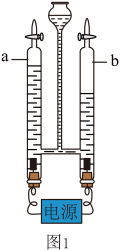

I、观察图1,b管连接的是电源______ (选填“正”或“负”)极,电解水的化学方程式是______ 。
II、分析图2,点燃氢气前,可选用______ 干燥氢气(填序号)。
A.生石灰 B.熟石灰 C.无水硫酸铜 D.硫酸铜晶体
“干燥氢气”的目的是______ 。
(2)水是一种常用的溶剂,不同物质在水中的溶解能力不同。
下表是NaCl、CaCl2的部分溶解度数据:
由上表可知,20℃时,NaCl的溶解度是______ g/100g水;60℃时,10g水中最多能溶解CaCl2______ g。
(3)某NaCl样品中混有少量CaCl2,可利用两物质溶解度的差异进行提纯。称取30g样品进行如下实验:
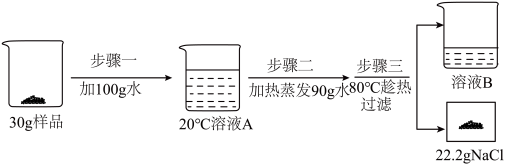
I、溶液A是该温度下NaCl的______ (填“饱和”或“不饱和”)溶液。
II、30g样品中含CaCl2的质量是______ g。
III、分析上述实验,说明步骤三趁热过滤的温度保持在60℃还是80℃更合适?请结合相关数据分析说明______
(1)验证水的组成。


I、观察图1,b管连接的是电源
II、分析图2,点燃氢气前,可选用
A.生石灰 B.熟石灰 C.无水硫酸铜 D.硫酸铜晶体
“干燥氢气”的目的是
(2)水是一种常用的溶剂,不同物质在水中的溶解能力不同。
下表是NaCl、CaCl2的部分溶解度数据:
| 温度(℃) | 20 | 40 | 60 | 80 | 100 |
| 溶解度(g/100g水) | NaCl | 36.0 | 36.6 | 37.1 | 38.0 |
| CaCl2 | 27.6 | 39.8 | 41.4 | 43.2 |
(3)某NaCl样品中混有少量CaCl2,可利用两物质溶解度的差异进行提纯。称取30g样品进行如下实验:

I、溶液A是该温度下NaCl的
II、30g样品中含CaCl2的质量是
III、分析上述实验,说明步骤三趁热过滤的温度保持在60℃还是80℃更合适?请结合相关数据分析说明
2023·上海闵行·一模 查看更多[4]
2023年上海市闵行区中考一模化学试题(已下线)第三章 走进溶液世界(单元测试)-2023-2024学年九年级化学第一学期同步精品课堂(沪教版·上海)(已下线)期末测试卷02(一模)-2023-2024学年九年级化学上学期期中期末挑战满分冲刺卷(沪教版·上海)(已下线)2024年中考风向标-上海-物质的分离与提纯及粗盐的提纯
更新时间:2023-04-01 21:03:22
|
相似题推荐
【推荐1】大型纪录片《水问》向人们讲述了水是万物之源,是宝贵的自然资源。
(一)了解水的组成
(1)如图是电解水的实验装置示意图,图中a连接电源的___________ (填“正极”或“负极”),该反应的符号表达式为 ___________ ,该实验说明水是由 ___________ 组成的。

(2)实验时常在水中加入硫酸钠或氢氧化钠,目的是___________ 。
(3)下列关于电解水的说法中正确的是 ___________(填序号)。
(二)水的净化
小林同学收集到一瓶浑浊的河水,他要模拟自来水厂的净水过程,最终制成能用于进行化学实验的水,其净水过程如图所示。请回答以下问题:

(4)A物质可以是明矾,其作用是___________ ,操作①的名称是 ___________ ,进行该操作用到的玻璃棒的作用是 ___________ 。
(5)操作②中使用的物质是___________ ,这是利用了该物质的吸附性除去臭味和一些可溶性的杂质。操作③是净化程度最高的净化水的方法,该操作的名称是 ___________ 。
(6)向制得的实验室用水中加入肥皂水,振荡,出现的现象是___________ ,说明属于软水。
(一)了解水的组成
(1)如图是电解水的实验装置示意图,图中a连接电源的

(2)实验时常在水中加入硫酸钠或氢氧化钠,目的是
(3)下列关于电解水的说法中正确的是 ___________(填序号)。
| A.水分子发生了改变 |
| B.氢原子和氧原子没有发生变化 |
| C.水分子是化学变化中最小的微粒 |
| D.该反应为分解反应 |
| E.化学变化的实质是分子分裂成原子,原子重新组合成新的分子 |
(二)水的净化
小林同学收集到一瓶浑浊的河水,他要模拟自来水厂的净水过程,最终制成能用于进行化学实验的水,其净水过程如图所示。请回答以下问题:

(4)A物质可以是明矾,其作用是
(5)操作②中使用的物质是
(6)向制得的实验室用水中加入肥皂水,振荡,出现的现象是
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐2】为探究水的组成及变化,某小同学设计如图装置进行电解水实验,先在电解器玻璃管里加满水(含少量NaOH),再接通直流电源。已知:水中加入的NaOH只起增强导电性作用,本身不参与反应。回答下列问题:
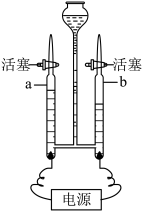
(1)a管连接的是电源的____________ 极,a、b两支玻璃管中生成气体的体积比约为_____________ 。
(2)切断电源后,用燃着的木条在a玻璃管尖嘴口检验产生的气体,观察到的现象是_________ 。
(3)若已知a管收集到气体质量为0.8克,请计算b管产生气体的质量,请写出计算过程。

(1)a管连接的是电源的
(2)切断电源后,用燃着的木条在a玻璃管尖嘴口检验产生的气体,观察到的现象是
(3)若已知a管收集到气体质量为0.8克,请计算b管产生气体的质量,请写出计算过程。
您最近一年使用:0次
综合应用题
|
适中
(0.65)
【推荐3】某研究小组同学以水为主题,进行以下两个主题的研究:
I水的净化:同学们在黄海边旅游时,用瓶装了些海水带回实验室,仿照自来水厂的净水过程,按照如图流程进行实验制取蒸馏水。请回答下列问题。
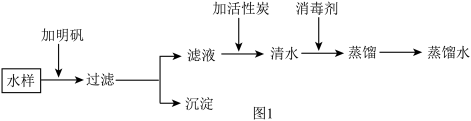
(1)海水因含大量氯化钠而略带咸味,氯化钠由_________ 构成(填粒子符号)。.
(2)下列净化水的单一操作中,相对净化程度最高的是_________ (填字母)
a.静置沉淀 b.过滤 c.加入活性炭 d.蒸馏
(3)向滤液中加入活性炭,利用其具有_________ 性,除去水样中的色素和异味。
(4)二氧化氯是一种常用的消毒剂,请用化学用语表示二氧化氯中氯元素的化合价_________ 。
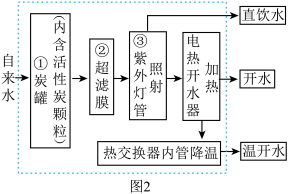
(5)研究过程中,同学们查阅资料时发现,目前许多旅游景点安装了直饮水机,其工作流程如图所示。③中紫外灯管照射的作用是_________ , 超滤膜的作用相当于实验室的_________ (填操作名称)。
II 水的变化:宏观、微观之间存在必然联系,请根据下图水的两种变化和微观示意图回答问题。

(1)如图3属于_________ 变化,从微观结构分析,该变化的特点是_________ 。
(2)如图4电解水实验中,小明推测“a试管内产生的是氢气,b管内产生的是氧气。”这属于科学探究中的_________ (填序号) 环节,还需要_________ 来进行验证。
a.提出问题 b.猜想与假设 c.设计并进行实验 d.表达与交流
(3)如图5对应于如图中_________ (填“甲”或“乙”)变化,该变化的文字表达式为_________ 。
(4)关于电解水实验的下列说法中正确的是_________ 。
a.水是由氢气和氧气组成的 b.生成氧气中氧分子化学性质与空气中氧分子化学性质相同
c.分子在化学变化中可以再分 d.分子是化学变化中的最小粒子
I水的净化:同学们在黄海边旅游时,用瓶装了些海水带回实验室,仿照自来水厂的净水过程,按照如图流程进行实验制取蒸馏水。请回答下列问题。


(1)海水因含大量氯化钠而略带咸味,氯化钠由
(2)下列净化水的单一操作中,相对净化程度最高的是
a.静置沉淀 b.过滤 c.加入活性炭 d.蒸馏
(3)向滤液中加入活性炭,利用其具有
(4)二氧化氯是一种常用的消毒剂,请用化学用语表示二氧化氯中氯元素的化合价
(5)研究过程中,同学们查阅资料时发现,目前许多旅游景点安装了直饮水机,其工作流程如图所示。③中紫外灯管照射的作用是
II 水的变化:宏观、微观之间存在必然联系,请根据下图水的两种变化和微观示意图回答问题。

(1)如图3属于
(2)如图4电解水实验中,小明推测“a试管内产生的是氢气,b管内产生的是氧气。”这属于科学探究中的
a.提出问题 b.猜想与假设 c.设计并进行实验 d.表达与交流
(3)如图5对应于如图中
(4)关于电解水实验的下列说法中正确的是
a.水是由氢气和氧气组成的 b.生成氧气中氧分子化学性质与空气中氧分子化学性质相同
c.分子在化学变化中可以再分 d.分子是化学变化中的最小粒子
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐1】《天工开物》中有“煤饼烧石成灰”的记载(“石”指石灰石),石灰石是重要的化工原料。某化学兴趣小组围绕石灰石进行了以下探究。
Ⅰ、石灰石分解的探究
【实验1】如图所示,利用煤气灯(煤气的主要成分是CO)煅烧石灰石(煅烧时杂质不发生变化)。

(1)同学们煅烧石灰石时,在火焰上方罩一个涂有澄清石灰水的烧杯,发现石灰水变浑浊,产生浑浊的化学方程式为______ 。根据上述现象能否推断煅烧石灰石产生二氧化碳?并请说明理由______ 。
(2)用煅烧后的固体继续做如下图甲所示的实验。

①继续向试管A上层清液中逐滴滴加稀盐酸,至红色恰好褪去,轻轻晃动试管A,溶液自下而上又变为红色。解释出现上述现象的原因______ 。
②请设计实验证验实验1中的石灰石是部分发生分解:
【实验2】如图乙,取少量碳酸钙粉末于试管B,加入2mL水,振荡,制成碳酸钙悬浊液,滴加2滴无色酚酞试液,酚酞试液变红。加热后,溶液红色变浅。经测定发现液体的pH变小。另一组同学测得在常温下四种混合体系的pH如下表所示。
(3)实验证明,碳酸钙悬浊液中形成了碳酸钙的______ (填“饱和”或“不饱和”)使溶液。
(4)碳酸钙的溶解度受温度影响的情况是______ 。
(5)碳酸钙悬浊液使酚酞变红与______ (填微粒符号)有关,理由是______ 。
Ⅱ、石灰石用途的探究
(6)工业用石灰石浆吸收废气中的二氧化硫,主要的反应为: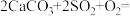
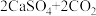 。请回答下列问题:
。请回答下列问题:
①硫元素的化合价在反应前后的变化为______ 。
②按上述方法处理2000吨废气中的二氧化硫,至少需要含5t碳酸钙的石灰石桨参加反应。则废气中二氧化硫的质量分数。______
(7)石灰石是高炉炼铁的原料之一。石灰石能除去铁矿石中的SiO2,同时能提高单位时间内生铁的产率。分析加入石灰石能提高生铁产率的原因可能是:______ 。
Ⅰ、石灰石分解的探究
【实验1】如图所示,利用煤气灯(煤气的主要成分是CO)煅烧石灰石(煅烧时杂质不发生变化)。

(1)同学们煅烧石灰石时,在火焰上方罩一个涂有澄清石灰水的烧杯,发现石灰水变浑浊,产生浑浊的化学方程式为
(2)用煅烧后的固体继续做如下图甲所示的实验。

①继续向试管A上层清液中逐滴滴加稀盐酸,至红色恰好褪去,轻轻晃动试管A,溶液自下而上又变为红色。解释出现上述现象的原因
②请设计实验证验实验1中的石灰石是部分发生分解:
实验操作 | 实验现象 | 实验结论 |
实验1中的石灰石部分分解 |
【实验2】如图乙,取少量碳酸钙粉末于试管B,加入2mL水,振荡,制成碳酸钙悬浊液,滴加2滴无色酚酞试液,酚酞试液变红。加热后,溶液红色变浅。经测定发现液体的pH变小。另一组同学测得在常温下四种混合体系的pH如下表所示。
混合体系 | ①Na2CO3溶液 | ②NaCl溶液 | 溶液CaCl2 | ④CaCO3悬浊液 |
pH | 11.6 | 7.0 | 7.0 | 10.1 |
(4)碳酸钙的溶解度受温度影响的情况是
(5)碳酸钙悬浊液使酚酞变红与
Ⅱ、石灰石用途的探究
(6)工业用石灰石浆吸收废气中的二氧化硫,主要的反应为:
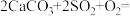
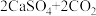 。请回答下列问题:
。请回答下列问题:①硫元素的化合价在反应前后的变化为
②按上述方法处理2000吨废气中的二氧化硫,至少需要含5t碳酸钙的石灰石桨参加反应。则废气中二氧化硫的质量分数。
(7)石灰石是高炉炼铁的原料之一。石灰石能除去铁矿石中的SiO2,同时能提高单位时间内生铁的产率。分析加入石灰石能提高生铁产率的原因可能是:
您最近一年使用:0次
综合应用题
|
适中
(0.65)
名校
解题方法
【推荐2】定量研究既是化学的重要思想,也是研究化学变化的重要方法。“青附”学习小组走进实验室,从定量角度探究化学变化、应用化学知识。
(1)“青附”学习小组想用如图装置探究质量守恒定律,请回答下列问题。
①确定研究对象:可以选择的化学反应是___________ 。(填字母)
A.盐酸和大理石反应,生成氯化钙、水和二氧化碳
B.氢氧化钠溶液和硫酸铜溶液反应,生成硫酸钠和氢氧化铜
②进行实验:反应前后天平指针不发生偏转。
③得出结论:参加化学反应的各物质的质量总和,等于反应后生成的各物质的质量总和。
④迁移应用:下列现象能用质量守恒定律解释的是___________ (填字母)。
A.镁条燃烧时,生成的白色粉末的质量大于镁条质量
B.氢气燃烧时,参加反应的氢气和氧气的体积大于生成水的体积
C.水结冰前后质量保持不变
⑤实质探究:质量守恒定律成立的微观原因是:___________ 。
(2)“青附”学习小组欲配制50g溶质质量分数为10%的氯化钠溶液,按如图所示步骤进行操作。

步聚①计算:需氯化钠___________ g,水___________ mL(室温时,水的密度约为1.0g/mL)
步骤②___________ (写步骤名称),调节天平平衡后称取所需的氯化钠固体时,发现托盘天平的指针偏左,此时应___________ (填字母)。
A.调节天平平衡螺母 B.增加适量氯化钠
C.增加砝码 D.减少适量氯化钠
步骤③溶解:用量筒量取所需的水,倒入盛有NaC1固体的烧杯中,用玻璃棒搅拌,搅拌的目的是___________ 。这样得到的溶液即是50g溶质质量分数为10%的NaC1溶液。
步骤④装瓶存放:配好的溶液在装入试剂瓶时不小心洒出少许,则其溶质质量分数___________ (填“变大”“变小”“不变”)。
(3)“青附”学习小组的同学分别继续按照下表的数据配制了A、B、C、D四组溶液,请分析并回答下列问题。
a.上述四组溶液属于饱和溶液的是___________ 。(填字母)
b.取等质量的氯化钠和硝酸钾固体各mg,按照如图进行实验。
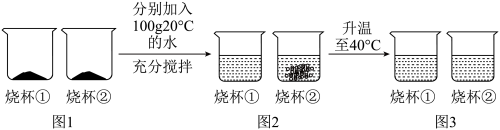
m的取值范围是___________ ,图1烧杯①中盛放的物质是___________ 。(填化学式)

(1)“青附”学习小组想用如图装置探究质量守恒定律,请回答下列问题。
①确定研究对象:可以选择的化学反应是
A.盐酸和大理石反应,生成氯化钙、水和二氧化碳
B.氢氧化钠溶液和硫酸铜溶液反应,生成硫酸钠和氢氧化铜
②进行实验:反应前后天平指针不发生偏转。
③得出结论:参加化学反应的各物质的质量总和,等于反应后生成的各物质的质量总和。
④迁移应用:下列现象能用质量守恒定律解释的是
A.镁条燃烧时,生成的白色粉末的质量大于镁条质量
B.氢气燃烧时,参加反应的氢气和氧气的体积大于生成水的体积
C.水结冰前后质量保持不变
⑤实质探究:质量守恒定律成立的微观原因是:
(2)“青附”学习小组欲配制50g溶质质量分数为10%的氯化钠溶液,按如图所示步骤进行操作。

步聚①计算:需氯化钠
步骤②
A.调节天平平衡螺母 B.增加适量氯化钠
C.增加砝码 D.减少适量氯化钠
步骤③溶解:用量筒量取所需的水,倒入盛有NaC1固体的烧杯中,用玻璃棒搅拌,搅拌的目的是
步骤④装瓶存放:配好的溶液在装入试剂瓶时不小心洒出少许,则其溶质质量分数
(3)“青附”学习小组的同学分别继续按照下表的数据配制了A、B、C、D四组溶液,请分析并回答下列问题。
| 序号 | 温度/℃ | 水的质量/g | 加入的固体及质量g | 所得溶液的质量/g |
| A | 20 | 50 | 硝酸钾20 | 65.8 |
| B | 40 | 100 | 硝酸钾65 | 163.9 |
| C | 20 | 100 | 氯化钠40 | 136.0 |
| D | 40 | 100 | 氯化钠40 | 136.6 |
b.取等质量的氯化钠和硝酸钾固体各mg,按照如图进行实验。

m的取值范围是
您最近一年使用:0次
【推荐3】水在化学实验、生产与生活中的作用不可忽视。
(1)下图三个实验中分别用到了水。

图A铁丝在氧气中燃烧 图B探究燃烧的条件 图C探究二氧化碳的性质
①图A中水的作用是_______________ 。
②图B中水的作用是提供热量和______________ 。
③图C中水的作用是______________ 。
(2)农业上常用16%的氯化钠溶液选种,1000g该浓度的氯化钠溶液中含有溶质的质量为_____ g,若配制该溶液时,将量取好的水洒落容器外,则所配溶液的溶质质量分数_______ (填“偏大”“偏小”或“不变”)。
(3)下表是氯化钠和硝酸钾两种物质在不同温度时的溶解度。
①40℃时氯化钠和硝酸钾两种物质中溶解度较大的是_______ 。
②若氯化钠中混有少量硝酸钾,提纯氯化钠的方法是_______ 。
③20℃时,按如图进行操作。乙中的溶液为_______ (填“饱和”或“不饱和”)溶液,丙中未溶解的固体质量为_______ g。
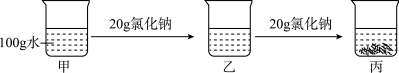
(1)下图三个实验中分别用到了水。

图A铁丝在氧气中燃烧 图B探究燃烧的条件 图C探究二氧化碳的性质
①图A中水的作用是
②图B中水的作用是提供热量和
③图C中水的作用是
(2)农业上常用16%的氯化钠溶液选种,1000g该浓度的氯化钠溶液中含有溶质的质量为
(3)下表是氯化钠和硝酸钾两种物质在不同温度时的溶解度。
| 温度/℃ | 20 | 30 | 40 | 50 | 60 | |
| 溶解度/g | NaCl | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 |
| KNO3 | 31.6 | 45.8 | 63.9 | 85.5 | 110.0 | |
②若氯化钠中混有少量硝酸钾,提纯氯化钠的方法是
③20℃时,按如图进行操作。乙中的溶液为

您最近一年使用:0次
【推荐1】如图是A、B、C三种固体物质的溶解度曲线,请回答下列问题:
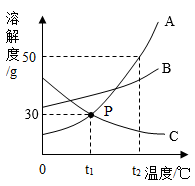
(1)t2℃时若将等质量的A、B、C三种物质加入100g水中,只有一种物质形成了饱和溶液,则该物质是____________ 。
(2)要使A、B、C的不饱和溶液变成饱和溶液,下列措施一定能达到目的的是____________ (填序号)。
①升高温度 ②加溶质 ③恒温蒸发溶剂 ④加溶剂
(3)将t1℃三种物质的饱和溶液升温至t2℃,所得溶液溶质的质量分数由大到小的排列顺序是____________ (填字母)。
(4)下列说法正确的是____________ (填序号)。
①t1℃时,A和C的饱和溶液溶质的质量分数都为30%
②t2℃时,A溶液比B溶液的溶质质量分数大
③t2℃时,等质量的A、B、C三种物质的饱和溶液中,A物质的溶液中溶剂的量最少
④t2℃时,30gA物质加入到50g水中不断搅拌形成溶液,该溶液的溶质质量分数是37.5%
⑤分别将A、B两物质的饱和溶液由t2℃降至t1℃时,析出晶体质量较多的是A
(5)要配制36.8g溶质质量分数为9.8%的稀硫酸,需要溶质质量分数为98%的浓硫酸(密度为1.84g/cm3)____________ mL;配制过程中用到的玻璃仪器有烧杯、玻璃棒、胶头滴管和____________ 。

(1)t2℃时若将等质量的A、B、C三种物质加入100g水中,只有一种物质形成了饱和溶液,则该物质是
(2)要使A、B、C的不饱和溶液变成饱和溶液,下列措施一定能达到目的的是
①升高温度 ②加溶质 ③恒温蒸发溶剂 ④加溶剂
(3)将t1℃三种物质的饱和溶液升温至t2℃,所得溶液溶质的质量分数由大到小的排列顺序是
(4)下列说法正确的是
①t1℃时,A和C的饱和溶液溶质的质量分数都为30%
②t2℃时,A溶液比B溶液的溶质质量分数大
③t2℃时,等质量的A、B、C三种物质的饱和溶液中,A物质的溶液中溶剂的量最少
④t2℃时,30gA物质加入到50g水中不断搅拌形成溶液,该溶液的溶质质量分数是37.5%
⑤分别将A、B两物质的饱和溶液由t2℃降至t1℃时,析出晶体质量较多的是A
(5)要配制36.8g溶质质量分数为9.8%的稀硫酸,需要溶质质量分数为98%的浓硫酸(密度为1.84g/cm3)
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐2】已知M、N两种固体物质的溶解度曲线如图所示。据图回答问题:
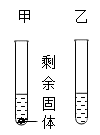
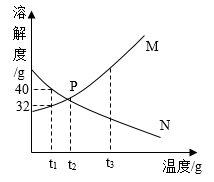
(1)在t1℃甲、乙两只试管中各盛有50g水,分别取M、N两物质20g溶解于试管中,如图,则甲试管里溶解的是物质____ (M、N),若将温度升高至t3℃,则乙试管中的现象是___ ,甲试管中溶液的溶质质量分数是___ (保留小数点后一位),若将此溶液浓缩成40%的溶液,则需蒸发掉__ 水。
(2)若将t 3℃时M、N两物质的等质量的饱和溶液降温至t2℃,则溶液的质量由大到小顺序是____


(1)在t1℃甲、乙两只试管中各盛有50g水,分别取M、N两物质20g溶解于试管中,如图,则甲试管里溶解的是物质
(2)若将t 3℃时M、N两物质的等质量的饱和溶液降温至t2℃,则溶液的质量由大到小顺序是
您最近一年使用:0次
【推荐3】硝酸钾是重要的工业原料。下表是硝酸钾和氯化钠的部分溶解度数据:
(1)农业生产中常将硝酸钾用作______ 。
(2)20℃时,氯化钠的溶解度为______ 。
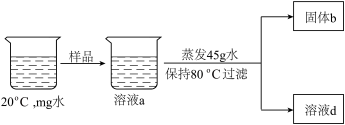
(3)工业生产的硝酸钾往往含有一定量的氯化钠。20℃时,取15g硝酸钾(含杂质氯化钠)样品,进行以下实验:______ g,取用该水量的理由是______ 。若得到固体b的质量为0.6g,该固体是______ (填写物质名称),样品中所含杂质氯化钠的质量是______ g。溶液a和溶液d中硝酸钾的质量是否相等并阐述你的理由。______ 。
| 温度(℃) | 0 | 20 | 40 | 60 | 80 | |
| 溶解度(g/100g水) | 氯化钠 | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 |
| 硝酸钾 | 13.3 | 31.6 | 63.9 | 110.0 | 169.0 | |
(1)农业生产中常将硝酸钾用作
(2)20℃时,氯化钠的溶解度为
(3)工业生产的硝酸钾往往含有一定量的氯化钠。20℃时,取15g硝酸钾(含杂质氯化钠)样品,进行以下实验:
您最近一年使用:0次
【推荐1】水是人类赖以生存和发展不可缺少的重要物质资源之一,请你用水的知识回答下列问题:
(1)下列物质属于纯净物的是___________(填字母)。
(2)3月22日是“世界水日”,自来水厂净水过程中不涉及的步骤是___________(填字母)。
(3)如图是KNO3和NH4Cl的溶解度曲线,根据图示填空
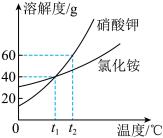
①将NH4Cl的不饱和溶液变成饱和溶液,方法有___________ (填一条即可)。
②t2℃时,KNO3饱和溶液中溶质的质量分数是___________ 。
③t2℃时,分别将200g KNO3饱和溶液和200gNH4Cl饱和溶液蒸发10g水,再恢复到t2℃后过滤,所得溶液质量较大的是___________ (填“KNO3”或“NH4Cl”)溶液。
(4)某小组称取4.90g氯酸钾和1.50g二氧化锰混合后进行制取氧气,收集一定量氧气后结束实验,为回收剩余固体中的二氧化锰,进行如下实验。
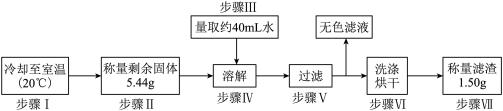
(20℃时氯酸钾、氯化钾的溶解度分别为7g、34g;假设溶液中两种物质的溶解度相互无影响,此时水的密度为1g/ml)
①5.44g剩余固体中含有的氯酸钾质量为___________ g。
②步骤Ⅲ中水量约为40mL而不是30mL的原因___________ 。
(1)下列物质属于纯净物的是___________(填字母)。
| A.海水 | B.冰水混合物 | C.矿泉水 | D.自来水 |
| A.沉淀 | B.蒸馏 | C.吸附 | D.消毒 |

①将NH4Cl的不饱和溶液变成饱和溶液,方法有
②t2℃时,KNO3饱和溶液中溶质的质量分数是
③t2℃时,分别将200g KNO3饱和溶液和200gNH4Cl饱和溶液蒸发10g水,再恢复到t2℃后过滤,所得溶液质量较大的是
(4)某小组称取4.90g氯酸钾和1.50g二氧化锰混合后进行制取氧气,收集一定量氧气后结束实验,为回收剩余固体中的二氧化锰,进行如下实验。

(20℃时氯酸钾、氯化钾的溶解度分别为7g、34g;假设溶液中两种物质的溶解度相互无影响,此时水的密度为1g/ml)
①5.44g剩余固体中含有的氯酸钾质量为
②步骤Ⅲ中水量约为40mL而不是30mL的原因
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐2】已知M、N两种固体物质的溶解度曲线如图所示。据图回答问题:


(1)在t1℃甲、乙两只试管中各盛有50g水,分别取M、N两物质20g溶解于试管中,如图,则甲试管里溶解的是物质____ (M、N),若将温度升高至t3℃,则乙试管中的现象是___ ,甲试管中溶液的溶质质量分数是___ (保留小数点后一位),若将此溶液浓缩成40%的溶液,则需蒸发掉__ 水。
(2)若将t 3℃时M、N两物质的等质量的饱和溶液降温至t2℃,则溶液的质量由大到小顺序是____


(1)在t1℃甲、乙两只试管中各盛有50g水,分别取M、N两物质20g溶解于试管中,如图,则甲试管里溶解的是物质
(2)若将t 3℃时M、N两物质的等质量的饱和溶液降温至t2℃,则溶液的质量由大到小顺序是
您最近一年使用:0次
综合应用题
|
适中
(0.65)
【推荐3】下表是氯化铵在不同温度下的溶解度:
(1)从表中可知:随温度升高氯化铵的溶解度_____________ 。
(2)A烧杯是70℃时,溶剂为100g的氯化铵不饱和溶液,经过如下图的变化过程(在整个过程中不考虑水分的蒸发)。
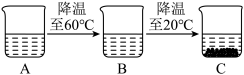
①C烧杯溶液中溶质的质量为_________ g。
②70℃时,将A烧杯中的溶液恒温蒸发10g溶剂后,析出ag固体,再继续恒温蒸发30g溶剂,则析出固体b g,则b g________ 3a g溶剂(填“<、≤、>、≥或=”)。
③配置一定溶质质量分数的氯化铵溶液的一些操作步骤见下图,正确的操作顺序是____ 。

| 温度(℃) | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 |
| 溶解度(g/100g水) | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 | 55.0 | 60.2 |
(2)A烧杯是70℃时,溶剂为100g的氯化铵不饱和溶液,经过如下图的变化过程(在整个过程中不考虑水分的蒸发)。

①C烧杯溶液中溶质的质量为
②70℃时,将A烧杯中的溶液恒温蒸发10g溶剂后,析出ag固体,再继续恒温蒸发30g溶剂,则析出固体b g,则b g
③配置一定溶质质量分数的氯化铵溶液的一些操作步骤见下图,正确的操作顺序是

您最近一年使用:0次



