已知M、N两种固体物质的溶解度曲线如图所示。据图回答问题:
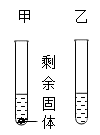
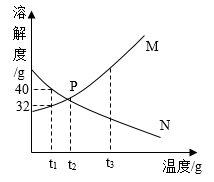
(1)在t1℃甲、乙两只试管中各盛有50g水,分别取M、N两物质20g溶解于试管中,如图,则甲试管里溶解的是物质____ (M、N),若将温度升高至t3℃,则乙试管中的现象是___ ,甲试管中溶液的溶质质量分数是___ (保留小数点后一位),若将此溶液浓缩成40%的溶液,则需蒸发掉__ 水。
(2)若将t 3℃时M、N两物质的等质量的饱和溶液降温至t2℃,则溶液的质量由大到小顺序是____


(1)在t1℃甲、乙两只试管中各盛有50g水,分别取M、N两物质20g溶解于试管中,如图,则甲试管里溶解的是物质
(2)若将t 3℃时M、N两物质的等质量的饱和溶液降温至t2℃,则溶液的质量由大到小顺序是
更新时间:2020/07/14 10:30:52
|
相似题推荐
综合应用题
|
适中
(0.65)
【推荐1】学习《海水“制碱”》的知识后,小明在实验室中进行了如下探究活动,请你和小明一起完成下面的实验探究活动。
(1)探究碳酸钠的溶解性:在编号为 A、B、C、D 的四个烧杯中各加入室温下的水 100g,并分别加入取自实验室的碳酸钠固体,搅拌至充分溶解,实验数据记录如下表:
分析上述数据,烧杯编号为_________ 中的溶液是饱和溶液。
(2)探究食用纯碱的纯度:小明把家中厨房里的食用纯碱(主要成分是Na2CO3)带到实验室,他称取食用纯碱12.0g放入烧杯中,加入200g水使其完全溶解。现将150g一定浓度的CaCl2溶液逐滴滴入烧杯中,测得滴加氯化钙溶液的质量与生成沉淀的质量关系如下表:
①m 的数值是______ 。
②计算纯碱样品中碳酸钠的质量分数______ (写出计算过程,计算结果保留一位小数)。
③滴加氯化钙溶液过量的目的是______ 。
(1)探究碳酸钠的溶解性:在编号为 A、B、C、D 的四个烧杯中各加入室温下的水 100g,并分别加入取自实验室的碳酸钠固体,搅拌至充分溶解,实验数据记录如下表:
| 烧杯编号 | A | B | C | D |
| 水的质量/g | 100 | 100 | 100 | 100 |
| 加入 Na2CO3 的质量/g | 30 | 35 | 40 | 50 |
| 溶液的质量/g | 130 | 135 | 140 | 140 |
分析上述数据,烧杯编号为
(2)探究食用纯碱的纯度:小明把家中厨房里的食用纯碱(主要成分是Na2CO3)带到实验室,他称取食用纯碱12.0g放入烧杯中,加入200g水使其完全溶解。现将150g一定浓度的CaCl2溶液逐滴滴入烧杯中,测得滴加氯化钙溶液的质量与生成沉淀的质量关系如下表:
| CaCl2 溶液的质量/g | 25 | 50 | 75 | 100 | 125 | 150 |
| 沉淀的质量/g | 2 | 4 | m | 8 | 10 | 10 |
①m 的数值是
②计算纯碱样品中碳酸钠的质量分数
③滴加氯化钙溶液过量的目的是
您最近一年使用:0次
【推荐2】水是构成一切生物体的基本成分,是生命之源。
(1)验证水的组成。
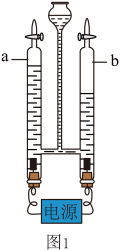

I、观察图1,b管连接的是电源______ (选填“正”或“负”)极,电解水的化学方程式是______ 。
II、分析图2,点燃氢气前,可选用______ 干燥氢气(填序号)。
A.生石灰 B.熟石灰 C.无水硫酸铜 D.硫酸铜晶体
“干燥氢气”的目的是______ 。
(2)水是一种常用的溶剂,不同物质在水中的溶解能力不同。
下表是NaCl、CaCl2的部分溶解度数据:
由上表可知,20℃时,NaCl的溶解度是______ g/100g水;60℃时,10g水中最多能溶解CaCl2______ g。
(3)某NaCl样品中混有少量CaCl2,可利用两物质溶解度的差异进行提纯。称取30g样品进行如下实验:
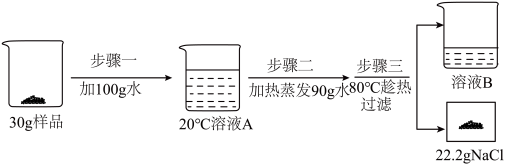
I、溶液A是该温度下NaCl的______ (填“饱和”或“不饱和”)溶液。
II、30g样品中含CaCl2的质量是______ g。
III、分析上述实验,说明步骤三趁热过滤的温度保持在60℃还是80℃更合适?请结合相关数据分析说明______
(1)验证水的组成。


I、观察图1,b管连接的是电源
II、分析图2,点燃氢气前,可选用
A.生石灰 B.熟石灰 C.无水硫酸铜 D.硫酸铜晶体
“干燥氢气”的目的是
(2)水是一种常用的溶剂,不同物质在水中的溶解能力不同。
下表是NaCl、CaCl2的部分溶解度数据:
| 温度(℃) | 20 | 40 | 60 | 80 | 100 |
| 溶解度(g/100g水) | NaCl | 36.0 | 36.6 | 37.1 | 38.0 |
| CaCl2 | 27.6 | 39.8 | 41.4 | 43.2 |
(3)某NaCl样品中混有少量CaCl2,可利用两物质溶解度的差异进行提纯。称取30g样品进行如下实验:

I、溶液A是该温度下NaCl的
II、30g样品中含CaCl2的质量是
III、分析上述实验,说明步骤三趁热过滤的温度保持在60℃还是80℃更合适?请结合相关数据分析说明
您最近一年使用:0次
综合应用题
|
适中
(0.65)
名校
【推荐3】我国古代纺织业常将草木灰(主要成分K2CO3)和生石灰在水中混合,用上层清液漂白织物。
【资料】①K2CO3 + Ca(OH)2 = CaCO3↓ + 2KOH
②Ca(OH)2、K2CO3 和 KOH 的部分溶解度如下表:
(1)20℃时,100 g 水中最多可溶解 K2CO3 的质量是__________ g,溶质的质量分数为 50% 的 KOH 溶液属于 ___________ 溶液(填“饱和”或“不饱和”)。
(2)某温度时,向一定量的饱和氢氧化钙溶液中加入少量生石灰,恢复到原温度,某些量随时间变化的关系如图所示。则纵坐标可能表示的是____________ (填序号)
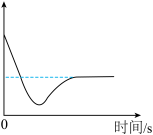
a溶质的质量 b溶质的质量分数 c 氢氧化钙的溶解度 d溶剂的质量 e溶液的质量
(3)20℃时,将 1.38 g K2CO3 固体放入 100 g 水中,并加入一定量的氢氧化钙,搅拌使其充分反应,恢复到原温度,过滤,得到质量为 1.5 g 的固体。所得滤液中的溶质是____________ ,加入氢氧化钙的质量是_________ g。
(4)将纯净的氯化钠配制成溶液。20℃时,向 4 个盛有 200 g 水的烧杯中,分别加入一定质量的氯化钠并充分溶解。4 组实验数据如下:
若将②中得到的溶液稀释成质量分数为 0.9%的生理盐水,需加水的质量是________ g。关于上述实验的叙述正确的是__________ (填序号)。
a①②所得溶液是不饱和溶液
b③④所得溶液中,溶质的质量分数相等
c20℃时,200 g 水中最多溶解氯化钠的质量为 72 g
d20℃时,将④继续恒温蒸发 100 g 水,过滤,得到质量为 36 g 的固体
【资料】①K2CO3 + Ca(OH)2 = CaCO3↓ + 2KOH
②Ca(OH)2、K2CO3 和 KOH 的部分溶解度如下表:
| 温度/℃ | 0 | 10 | 20 | 30 | 50 | |
| 溶解度/g | Ca(OH)2 | 0.18 | 0.17 | 0.16 | 0.15 | 0.14 |
| K2CO3 | 107 | 109 | 110 | 114 | 121 | |
| KOH | 97 | 103 | 112 | 126 | 140 | |
(2)某温度时,向一定量的饱和氢氧化钙溶液中加入少量生石灰,恢复到原温度,某些量随时间变化的关系如图所示。则纵坐标可能表示的是

a溶质的质量 b溶质的质量分数 c 氢氧化钙的溶解度 d溶剂的质量 e溶液的质量
(3)20℃时,将 1.38 g K2CO3 固体放入 100 g 水中,并加入一定量的氢氧化钙,搅拌使其充分反应,恢复到原温度,过滤,得到质量为 1.5 g 的固体。所得滤液中的溶质是
(4)将纯净的氯化钠配制成溶液。20℃时,向 4 个盛有 200 g 水的烧杯中,分别加入一定质量的氯化钠并充分溶解。4 组实验数据如下:
| 实验序号 | ① | ② | ③ | ④ |
| 加入氯化钠的质量/g | 9 | 36 | 81 | 90 |
| 溶液质量/g | 209 | 236 | 272 | 272 |
a①②所得溶液是不饱和溶液
b③④所得溶液中,溶质的质量分数相等
c20℃时,200 g 水中最多溶解氯化钠的质量为 72 g
d20℃时,将④继续恒温蒸发 100 g 水,过滤,得到质量为 36 g 的固体
您最近一年使用:0次
【推荐1】人类的生存发展离不开水。
(1)自然界中的水主要以___________ (填“纯净物”或“混合物”)的形式存在。
(2)生活中将硬水软化最常用的方法是___________ 。
(3)水是常用的溶剂,下列物质放入水中,能形成无色无气味溶液的是___________ 。
A 酒精 B 硫酸铁 C 氯化钠 D 氢氧化镁
(4)意外火灾会对生命财产带来损害,下列火灾不能用水熄灭的是___________ 。
A 油锅着火 B 森林失火 C 棉花着火 D 电器着火
(5)水的存在有利有弊。保存干果时尽可能避免有水存在,以防发生霉变。因此常在食品袋内放一包干燥剂,其主要成分为氧化钙。试写出氧化钙去除水分的化学方程式___________ 。
(6)不同的物质在水中溶解能力有所差异。下图为甲、乙、丙三种物质的溶解度曲线。结合图示回答下列问题。
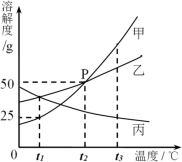
① 交点P的意义为___________ 。
② 在不改变溶剂的前提下,使丙的饱和溶液转变为不饱和溶液的方法为___________ 。
③t1℃时15 g甲的饱和溶液中溶质质量分数为___________ 。
④ 甲、乙、丙三种物质的饱和溶液溶质质量分数由大到小的顺序为丙>乙>甲时,温度t的范围为___________ 。
(1)自然界中的水主要以
(2)生活中将硬水软化最常用的方法是
(3)水是常用的溶剂,下列物质放入水中,能形成无色无气味溶液的是
A 酒精 B 硫酸铁 C 氯化钠 D 氢氧化镁
(4)意外火灾会对生命财产带来损害,下列火灾不能用水熄灭的是
A 油锅着火 B 森林失火 C 棉花着火 D 电器着火
(5)水的存在有利有弊。保存干果时尽可能避免有水存在,以防发生霉变。因此常在食品袋内放一包干燥剂,其主要成分为氧化钙。试写出氧化钙去除水分的化学方程式
(6)不同的物质在水中溶解能力有所差异。下图为甲、乙、丙三种物质的溶解度曲线。结合图示回答下列问题。

① 交点P的意义为
② 在不改变溶剂的前提下,使丙的饱和溶液转变为不饱和溶液的方法为
③t1℃时15 g甲的饱和溶液中溶质质量分数为
④ 甲、乙、丙三种物质的饱和溶液溶质质量分数由大到小的顺序为丙>乙>甲时,温度t的范围为
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐2】化学是一门自然科学,其特征是研究物质和创造物质。
(1)硅是太阳能电池和电脑芯片不可缺少的材料。人们利用石英砂(主要成分是二氧化硅)制得高纯硅。生产高纯硅的流程示意图如下:
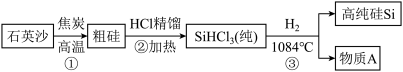
①制备粗硅的反应为:SiO2+2C Si+2CO↑,该反应属于
Si+2CO↑,该反应属于_______ 反应(选填“分解”“化合”“置换”“复分解”之一),其中生成物CO中碳元素的化合价为_______ 。
②制备过程中用到H2,可以用_______ (选填“锌”“铜”“碳”“水”之一)与稀盐酸反应生成。
③物质A通常状况下为无色有刺激性气味的气体,溶于水形成盐酸,试写出物质A的化学式____ 。
(2)海洋是生命的摇篮,海水不仅是宝贵的水资源,而且蕴藏着丰富的化学资源。从海水中取得淡水的过程称为“海水淡化”。 现在所用的海水淡化方法主要分为蒸馏法(热法)和膜法两大类。如图所示,对淡化膜右侧的海水加压,水分子可以透过淡化膜进入左侧淡水池,而海水中有些溶质离子不能通过淡化膜,从而得到淡水。
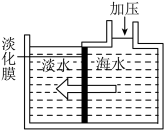
①将少量加压后的右侧海水置于表面皿中,用酒精灯加热,水分蒸干后,可在表面皿上观察到的现象是___ 。
②下列对加压后右侧海水成分变化情况的分析中,正确的是_______ (填选项)。
A 溶质质量增加 B 溶剂质量减少 C 溶液质量不变 D 溶质质量分数减小
③氨碱法制纯碱是先通过化学反应生成NaHCO3和NH4Cl,NaHCO3结晶析出,再加热NaHCO3制得纯碱。根据NaHCO3和NH4Cl的溶解度曲线回答下列问题:
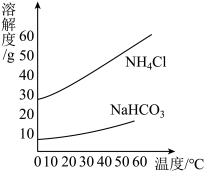
a 40℃时,NH4Cl的溶解度_______ NaHCO3的溶解度(选填“大于”“小于”“等于”之一)。
b 把30℃时NH4Cl的饱和溶液升温到50℃后所得溶液是此温度下NH4Cl的_______ 溶液(选填“饱和”或“不饱和”之一)。
c 20℃时,将30gNaHCO3固体置于100g水中,形成的溶液是此温度下NaHCO3的_______ 溶液(选填“饱和”或“不饱和”之一)。
d 在50℃时将等质量的NaHCO3和NH4Cl饱和溶液同时降温到20℃,_______ 析出晶体质量较多(填化学式)。
(1)硅是太阳能电池和电脑芯片不可缺少的材料。人们利用石英砂(主要成分是二氧化硅)制得高纯硅。生产高纯硅的流程示意图如下:

①制备粗硅的反应为:SiO2+2C
 Si+2CO↑,该反应属于
Si+2CO↑,该反应属于②制备过程中用到H2,可以用
③物质A通常状况下为无色有刺激性气味的气体,溶于水形成盐酸,试写出物质A的化学式
(2)海洋是生命的摇篮,海水不仅是宝贵的水资源,而且蕴藏着丰富的化学资源。从海水中取得淡水的过程称为“海水淡化”。 现在所用的海水淡化方法主要分为蒸馏法(热法)和膜法两大类。如图所示,对淡化膜右侧的海水加压,水分子可以透过淡化膜进入左侧淡水池,而海水中有些溶质离子不能通过淡化膜,从而得到淡水。

①将少量加压后的右侧海水置于表面皿中,用酒精灯加热,水分蒸干后,可在表面皿上观察到的现象是
②下列对加压后右侧海水成分变化情况的分析中,正确的是
A 溶质质量增加 B 溶剂质量减少 C 溶液质量不变 D 溶质质量分数减小
③氨碱法制纯碱是先通过化学反应生成NaHCO3和NH4Cl,NaHCO3结晶析出,再加热NaHCO3制得纯碱。根据NaHCO3和NH4Cl的溶解度曲线回答下列问题:

a 40℃时,NH4Cl的溶解度
b 把30℃时NH4Cl的饱和溶液升温到50℃后所得溶液是此温度下NH4Cl的
c 20℃时,将30gNaHCO3固体置于100g水中,形成的溶液是此温度下NaHCO3的
d 在50℃时将等质量的NaHCO3和NH4Cl饱和溶液同时降温到20℃,
您最近一年使用:0次
【推荐3】水是生命之源,人类的生产生活中离不开水。
(1)某自来水生产的一般过程如下图所示:

①明矾是一种常用的混凝剂,其作用是_______ 。
②氯气可用作自来水的消毒剂,实验室制取氯气的化学方程式为:MnO2+4HCl(浓) MnCl2+Cl2↑+2X,X的化学式为
MnCl2+Cl2↑+2X,X的化学式为_______ 。
③该生产过程_______ (填“能”或“不能”)将硬水转化成软水。
(2)如图是甲乙两种固体的溶解度曲线。

①40℃时,100g水最多能溶解_______ g甲。
②20℃时,将20g乙加到50g水中,充分溶解,溶液的溶质质量分数为_______ (只列式,不计算)。
③若甲中混有少量的乙,欲提纯甲,可采用的方法是_______ (填“蒸发结晶”或“降温结晶”)。
(1)某自来水生产的一般过程如下图所示:

①明矾是一种常用的混凝剂,其作用是
②氯气可用作自来水的消毒剂,实验室制取氯气的化学方程式为:MnO2+4HCl(浓)
 MnCl2+Cl2↑+2X,X的化学式为
MnCl2+Cl2↑+2X,X的化学式为③该生产过程
(2)如图是甲乙两种固体的溶解度曲线。

①40℃时,100g水最多能溶解
②20℃时,将20g乙加到50g水中,充分溶解,溶液的溶质质量分数为
③若甲中混有少量的乙,欲提纯甲,可采用的方法是
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐1】水是生命之源,是人类生产、生活中不可缺少的重要物质。
(1)生活中使用活性炭净化水,利用了活性炭的___________ 性。
(2)水常用作物质溶解的溶剂。___________ 。
②10℃时,将等质量的KNO3、NaCl固体分别加入到盛有100g水的两个烧杯中,搅拌,充分溶解,现象如图2所示。烧杯中一定是饱和溶液的是___________ (填“KNO3”或“NaCl”)溶液。
③Ca(OH)2溶解度曲线如图3所示,欲将A点对应的Ca(OH)2溶液溶质质量分数增大,下列三种方法中可采取的方法是___________ 。
A.升高温度 B.恒温蒸发水 C.降温后添加溶质
(1)生活中使用活性炭净化水,利用了活性炭的
(2)水常用作物质溶解的溶剂。
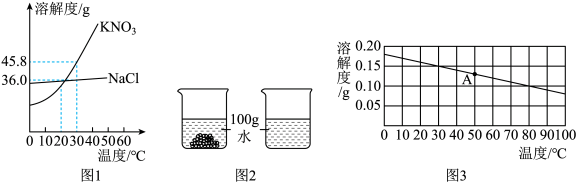
②10℃时,将等质量的KNO3、NaCl固体分别加入到盛有100g水的两个烧杯中,搅拌,充分溶解,现象如图2所示。烧杯中一定是饱和溶液的是
③Ca(OH)2溶解度曲线如图3所示,欲将A点对应的Ca(OH)2溶液溶质质量分数增大,下列三种方法中可采取的方法是
A.升高温度 B.恒温蒸发水 C.降温后添加溶质
您最近一年使用:0次
综合应用题
|
适中
(0.65)
【推荐2】t1 ℃时,将等质量的硝酸钾和氯化钾分别加入到各盛有100 g水的两个烧杯中,充分搅拌后现象如图1所示,硝酸钾和氯化钾的溶解度曲线如图2所示。完成下列各题。
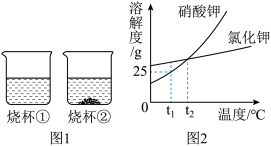
(1)烧杯①的溶液是________(填溶质的化学式)的溶液
(2)t1 ℃时,20g硝酸钾放入50g水中,所得溶液为_________(“饱和”或“不饱和”)溶液。
(3)若将烧杯①和烧杯②的溶液都升温到t2 ℃,则两烧杯中溶液的溶质质量分数的大小关系为烧杯①溶液的浓度 _____ (选填“大于”、“小于”、“等于”或“无法比较”)烧杯②溶液的浓度。
(4)t1 ℃时,若将125g硝酸钾的饱和溶液稀释至溶质质量分数为10%,需加水的质量为____ g 。

(1)烧杯①的溶液是________(填溶质的化学式)的溶液
(2)t1 ℃时,20g硝酸钾放入50g水中,所得溶液为_________(“饱和”或“不饱和”)溶液。
(3)若将烧杯①和烧杯②的溶液都升温到t2 ℃,则两烧杯中溶液的溶质质量分数的大小关系为烧杯①溶液的浓度 _____ (选填“大于”、“小于”、“等于”或“无法比较”)烧杯②溶液的浓度。
(4)t1 ℃时,若将125g硝酸钾的饱和溶液稀释至溶质质量分数为10%,需加水的质量为____ g 。
您最近一年使用:0次
【推荐3】红色经典影片《闪闪的红星》中有一段儿童团员潘冬子给红军送食盐的故事。潘冬子开始把食盐装在竹筒中,打算扮作上山砍柴的人将食盐送给红军,途中发现敌人盘查严格,潘冬子急中生智跑到河边,把竹筒里的食盐全部溶成食盐水,再用棉袄吸收,最终顺利地将食盐送给了红军。______ (写符号)构成。
(2)从食盐水中重新得到食盐固体,需进行的操作名称是______ 。
(3)氯化钠的溶解度曲线如图1,假设潘冬子的竹筒中有 氯化钠,
氯化钠, 时最少需用
时最少需用______ g水溶解。
(4)生理盐水是 的氯化钠溶液,市售生理盐水标签如图2,则配制
的氯化钠溶液,市售生理盐水标签如图2,则配制 生理盐水需要氯化钠
生理盐水需要氯化钠______ g。
(5)氯化钠具有广泛的应用。实验室配制 溶质质量分数为
溶质质量分数为 的氯化钠溶液。
的氯化钠溶液。
①用已调节平衡的托盘天平称取氯化钠时,发现指针偏左,接下来的操作是______ 。(填序号)
A.添加氯化钠 B.减少氯化钠 C.调节平衡螺母 D.添加砝码
②在量取水体积时,若仰视读数,则导致氯化钠溶液的溶质质量分数是______ (填“ ”、“
”、“ ”、“
”、“ ”)
”) 。
。
③若用溶质质量分数为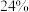 的
的 溶液和蒸馏水来配制该
溶液和蒸馏水来配制该 溶液,则所需
溶液,则所需 的
的 溶液与蒸馏水的质量比为
溶液与蒸馏水的质量比为______ 。
(6)食盐也是重要的工业原料,将饱和食盐水通电后,正负电极上会产生大量气泡,产生的气体经化合后溶于水,可得重要化工原料盐酸,向电解后的溶液中滴入酚酞试液后会变红。写出电解饱和食盐水反应的化学方程式为______ 。


(2)从食盐水中重新得到食盐固体,需进行的操作名称是
(3)氯化钠的溶解度曲线如图1,假设潘冬子的竹筒中有
 氯化钠,
氯化钠, 时最少需用
时最少需用(4)生理盐水是
 的氯化钠溶液,市售生理盐水标签如图2,则配制
的氯化钠溶液,市售生理盐水标签如图2,则配制 生理盐水需要氯化钠
生理盐水需要氯化钠(5)氯化钠具有广泛的应用。实验室配制
 溶质质量分数为
溶质质量分数为 的氯化钠溶液。
的氯化钠溶液。①用已调节平衡的托盘天平称取氯化钠时,发现指针偏左,接下来的操作是
A.添加氯化钠 B.减少氯化钠 C.调节平衡螺母 D.添加砝码
②在量取水体积时,若仰视读数,则导致氯化钠溶液的溶质质量分数是
 ”、“
”、“ ”、“
”、“ ”)
”) 。
。③若用溶质质量分数为
 的
的 溶液和蒸馏水来配制该
溶液和蒸馏水来配制该 溶液,则所需
溶液,则所需 的
的 溶液与蒸馏水的质量比为
溶液与蒸馏水的质量比为(6)食盐也是重要的工业原料,将饱和食盐水通电后,正负电极上会产生大量气泡,产生的气体经化合后溶于水,可得重要化工原料盐酸,向电解后的溶液中滴入酚酞试液后会变红。写出电解饱和食盐水反应的化学方程式为
您最近一年使用:0次
【推荐1】化学在农业、工业、科技、生活、生产中发挥着越来越重要的作用
(1)小东发现家里物品涉及很多化学知识,可以完成很多有趣的化学实验:请你与他一起探究家庭里的化学实验
①绿植所用的“无土栽培”营养液配方中含有下列物质,其中能促进植物茎、叶生长茂盛,叶色浓绿的是_____ (填字母,下同)。其中属于复合肥的是_____ 。
a. b.
b. c.
c. d.
d.
②洁厕灵的主要成分是稀盐酸,厨房清洁剂的主要成分是氢氧化钠溶液,洁厕灵与厨房清洁剂混合,主要反应的化学方程式为_____ 。
③腌制皮蛋的原料配方是少量 、
、 和过量
和过量 的固体混合物。将一定量的腌制皮蛋原料放于烧杯中,加入足量的蒸馏水,充分反应,所涉及的反应中有化合反应和
的固体混合物。将一定量的腌制皮蛋原料放于烧杯中,加入足量的蒸馏水,充分反应,所涉及的反应中有化合反应和_____ 反应(填写基本反应类型)
④生活中既可作食品调味剂,又能用于清洗热水瓶内水垢【主要成分 和
和 】的是
】的是_____ 。若改用稀盐酸来代替该物质,请写出稀盐酸除水垢中发生中和反应的化学方程式_____ ;该反应属于_____ 反应。(填“吸热”或“放热”)
(2)溶液与人类生产、生活密切相关。
①把少量下列物质分别放入水中,充分搅拌,能得到溶液的是_____ (填序号,下同)
A.硝酸钾 B.植物油 C.面粉 D.碳酸钙
②在盛有水的烧杯中加入以下某种物质,形成溶液过程中,温度降低,这种物质是_____ 。
A.氯化钠 B.硝酸铵 C.氢氧化钠
③ 时,根据某固体物质在不同质量的水中达到饱和状态时所溶解的质量,绘制成如图所示图像。
时,根据某固体物质在不同质量的水中达到饱和状态时所溶解的质量,绘制成如图所示图像。 时,该固体物质的溶解度为
时,该固体物质的溶解度为_____ 克。
(III)C点所对应的溶液是_____ (填“饱和”或“不饱和”)溶液。
(III)图中A、B、C、D四点对应的溶液溶质质量分数大小关系为_____ (用含A、B、C、D的关系式表达)。
(1)小东发现家里物品涉及很多化学知识,可以完成很多有趣的化学实验:请你与他一起探究家庭里的化学实验
①绿植所用的“无土栽培”营养液配方中含有下列物质,其中能促进植物茎、叶生长茂盛,叶色浓绿的是
a.
 b.
b. c.
c. d.
d.
②洁厕灵的主要成分是稀盐酸,厨房清洁剂的主要成分是氢氧化钠溶液,洁厕灵与厨房清洁剂混合,主要反应的化学方程式为
③腌制皮蛋的原料配方是少量
 、
、 和过量
和过量 的固体混合物。将一定量的腌制皮蛋原料放于烧杯中,加入足量的蒸馏水,充分反应,所涉及的反应中有化合反应和
的固体混合物。将一定量的腌制皮蛋原料放于烧杯中,加入足量的蒸馏水,充分反应,所涉及的反应中有化合反应和④生活中既可作食品调味剂,又能用于清洗热水瓶内水垢【主要成分
 和
和 】的是
】的是(2)溶液与人类生产、生活密切相关。
①把少量下列物质分别放入水中,充分搅拌,能得到溶液的是
A.硝酸钾 B.植物油 C.面粉 D.碳酸钙
②在盛有水的烧杯中加入以下某种物质,形成溶液过程中,温度降低,这种物质是
A.氯化钠 B.硝酸铵 C.氢氧化钠
③
 时,根据某固体物质在不同质量的水中达到饱和状态时所溶解的质量,绘制成如图所示图像。
时,根据某固体物质在不同质量的水中达到饱和状态时所溶解的质量,绘制成如图所示图像。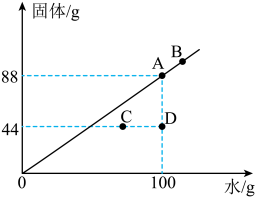
 时,该固体物质的溶解度为
时,该固体物质的溶解度为(III)C点所对应的溶液是
(III)图中A、B、C、D四点对应的溶液溶质质量分数大小关系为
您最近一年使用:0次
【推荐2】2021年3月15日,习近平总书记在会议上提出:
“要把碳达峰,碳中和纳入生态文明建设整体布局。”“碳达峰”就是我们国家承诺在2030年前,二氧化碳的排放不再增长,达到峰值之后再慢慢减下去:而到2060年,针对排放的二氧化碳,要采取植树、节能减排等各种方式全部抵消按,这就是“碳中和”。
①实现“碳中和”,需要通过能源结构的调整和替代实现。
②能源的清洁低碳化,是“十四五”碳达峰部署的重点工作。页岩气是蕴藏于页岩层可供开采的天然气资源,其成分以甲烷为主,是一种清洁、高效的能源资源和化工原料,主要用于居民燃气、城市供热、发电、汽车燃料和化工生产等。
请写出甲烷在空气中完全燃烧的化学反应方程式:______ ,该反应属于______ 反应。(选填“化合”、“分解”、“氧化”或“复分解”之一)
②完善能源双控制度,构建以新能源为主体的新型电力系统。下列选项中,不属于新能源的是______ (填序号)。
A.氢能B.风能C.太阳能D.石油
③氢氧燃料电池汽车替代传统能源汽车,可有效减少碳排放。氢氧燃料电池供电的过程中,______ 能转化为电能。
④实现碳达峰,碳中和是一场硬仗,需要每个人的努力与践行。下列做法中,不符合“低碳生活”的是______ (填序号)。
A.骑行共享单车,倡导绿色出行B.践行光盘行动,杜绝铺张浪费
C.旧衣焚烧掩埋,加快生产销售D.选用节能家电,减少能源消耗
(2)推进碳达峰、碳中和,需要科学技术发挥核心作用。工业生产中,关键工艺流程的低碳化改造十分重要。早在二十世纪初,我国著名化学家侯德榜先生创立了侯氏制碱法,优化并促进了世界制碱技术的发展。
如图所示为Na2CO3和NH4Cl两种物质的溶解度曲线。试回答下列问题:
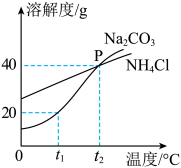
①由图可知,t1℃时,两者中溶解度较大的物质是______ 。
②t2℃时, NH4Cl饱和溶液的溶质质量分数______ Na2CO3饱和溶液的溶质质量分数。(选填“大于”、“小于”或“等于”)
③t1℃时,25g水中加入10 g Na2CO3固体,经充分搅拌后,所得溶液的质量为______ g。
④t2℃时,将等质量的NH4Cl饱和溶液和Na2CO3饱和溶液均降温至t1℃,析出晶体较多的是______ 。
“要把碳达峰,碳中和纳入生态文明建设整体布局。”“碳达峰”就是我们国家承诺在2030年前,二氧化碳的排放不再增长,达到峰值之后再慢慢减下去:而到2060年,针对排放的二氧化碳,要采取植树、节能减排等各种方式全部抵消按,这就是“碳中和”。

①实现“碳中和”,需要通过能源结构的调整和替代实现。
②能源的清洁低碳化,是“十四五”碳达峰部署的重点工作。页岩气是蕴藏于页岩层可供开采的天然气资源,其成分以甲烷为主,是一种清洁、高效的能源资源和化工原料,主要用于居民燃气、城市供热、发电、汽车燃料和化工生产等。
请写出甲烷在空气中完全燃烧的化学反应方程式:
②完善能源双控制度,构建以新能源为主体的新型电力系统。下列选项中,不属于新能源的是
A.氢能B.风能C.太阳能D.石油
③氢氧燃料电池汽车替代传统能源汽车,可有效减少碳排放。氢氧燃料电池供电的过程中,
④实现碳达峰,碳中和是一场硬仗,需要每个人的努力与践行。下列做法中,不符合“低碳生活”的是
A.骑行共享单车,倡导绿色出行B.践行光盘行动,杜绝铺张浪费
C.旧衣焚烧掩埋,加快生产销售D.选用节能家电,减少能源消耗
(2)推进碳达峰、碳中和,需要科学技术发挥核心作用。工业生产中,关键工艺流程的低碳化改造十分重要。早在二十世纪初,我国著名化学家侯德榜先生创立了侯氏制碱法,优化并促进了世界制碱技术的发展。
如图所示为Na2CO3和NH4Cl两种物质的溶解度曲线。试回答下列问题:

①由图可知,t1℃时,两者中溶解度较大的物质是
②t2℃时, NH4Cl饱和溶液的溶质质量分数
③t1℃时,25g水中加入10 g Na2CO3固体,经充分搅拌后,所得溶液的质量为
④t2℃时,将等质量的NH4Cl饱和溶液和Na2CO3饱和溶液均降温至t1℃,析出晶体较多的是
您最近一年使用:0次
【推荐3】某化学兴趣小组以“生命之源——水”为主题开展项目式学习。
任务一:掌握水的净化方法
(1)同学们从如泰运河取回水样,用自制净水器处理,净水器中的活性炭对水样中的异味和色素有___ 作用,所得的水____ (填“是”或“不是”)纯水。
(2)向处理后的水样中加入肥皂水,振荡,观察到泡沫较少,白色垢状物较多,则该水样属于____ (填“硬水”或“软水”)。生活中常用____ 的方法降低水的硬度。
(3)节约用水是我们的责任和义务,请写一条日常生活中的节水措施____ 。
任务二:探究水的组成
(4)1800年英国化学家尼科尔森利用伏打电池对水进行通电,发现两极上都有气体逸出。实验室常用如图装置进行模拟,则管a与管b中产生气体的体积比约为____ 。该实验可得出水是由____ 组成的。
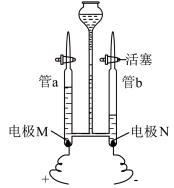
(5)电解水时,为增强水的导电性,通常加入少量NaOH,其溶解后可产生自由移动的阴离子是____ (填符号)。
任务三:探究水蒸气与镁粉的反应
(6)实验装置如图所示(部分夹持仪器省略),为了防止玻璃管中原有空气对实验的干扰,实验开始时,应先点燃____ (选填“A”或“B”)处酒精灯。
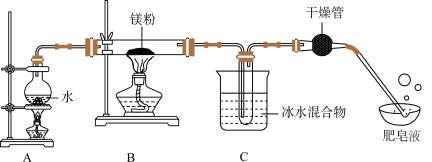
(7)肥皂液中产生了能上升到空中的肥皂泡,用燃着的木条靠近肥皂泡,有爆鸣声。B处玻璃管内生成了白色固体Mg(OH)2。写出B处玻璃管内发生反应的化学方程式____ 。
任务四:了解水的用途
(8)水是最常用的溶剂。20℃时,根据某固体物质在不同质量的水中达到饱和状态时所溶解的质量,绘制成如图所示图像。
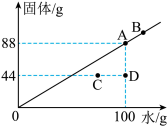
①20℃时,该固体物质的溶解度为____ g。
②C点所对应的溶液是____ (填“饱和”或“不饱和”)溶液。
③图中A、B、C、D四点所对应的溶液溶质质量分数大小关系为____ (用含A、B、C、D的关系式表示)
任务一:掌握水的净化方法
(1)同学们从如泰运河取回水样,用自制净水器处理,净水器中的活性炭对水样中的异味和色素有
(2)向处理后的水样中加入肥皂水,振荡,观察到泡沫较少,白色垢状物较多,则该水样属于
(3)节约用水是我们的责任和义务,请写一条日常生活中的节水措施
任务二:探究水的组成
(4)1800年英国化学家尼科尔森利用伏打电池对水进行通电,发现两极上都有气体逸出。实验室常用如图装置进行模拟,则管a与管b中产生气体的体积比约为

(5)电解水时,为增强水的导电性,通常加入少量NaOH,其溶解后可产生自由移动的阴离子是
任务三:探究水蒸气与镁粉的反应
(6)实验装置如图所示(部分夹持仪器省略),为了防止玻璃管中原有空气对实验的干扰,实验开始时,应先点燃

(7)肥皂液中产生了能上升到空中的肥皂泡,用燃着的木条靠近肥皂泡,有爆鸣声。B处玻璃管内生成了白色固体Mg(OH)2。写出B处玻璃管内发生反应的化学方程式
任务四:了解水的用途
(8)水是最常用的溶剂。20℃时,根据某固体物质在不同质量的水中达到饱和状态时所溶解的质量,绘制成如图所示图像。

①20℃时,该固体物质的溶解度为
②C点所对应的溶液是
③图中A、B、C、D四点所对应的溶液溶质质量分数大小关系为
您最近一年使用:0次



