硝酸钾是重要的工业原料。下表是硝酸钾和氯化钠的部分溶解度数据:
(1)农业生产中常将硝酸钾用作______ 。
(2)20℃时,氯化钠的溶解度为______ 。
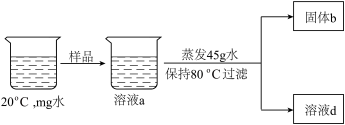
(3)工业生产的硝酸钾往往含有一定量的氯化钠。20℃时,取15g硝酸钾(含杂质氯化钠)样品,进行以下实验:______ g,取用该水量的理由是______ 。若得到固体b的质量为0.6g,该固体是______ (填写物质名称),样品中所含杂质氯化钠的质量是______ g。溶液a和溶液d中硝酸钾的质量是否相等并阐述你的理由。______ 。
| 温度(℃) | 0 | 20 | 40 | 60 | 80 | |
| 溶解度(g/100g水) | 氯化钠 | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 |
| 硝酸钾 | 13.3 | 31.6 | 63.9 | 110.0 | 169.0 | |
(1)农业生产中常将硝酸钾用作
(2)20℃时,氯化钠的溶解度为
(3)工业生产的硝酸钾往往含有一定量的氯化钠。20℃时,取15g硝酸钾(含杂质氯化钠)样品,进行以下实验:
2024·上海普陀·二模 查看更多[2]
更新时间:2024-04-16 10:41:55
|
相似题推荐
综合应用题
|
适中
(0.65)
解题方法
【推荐1】硫酸生产过程中会产生大量有害的二氧化硫废气和烟尘,为了变废为宝,某硫酸厂的环保车间设计了如下的工艺流程,采用物质循环利用的方法将二氧化硫转化为无毒的二氧化碳,其中,反应罐中发生的化学反应为:4Na2S+8SO2 8S↓+4Na2SO4分析流程,解决下列问题:
8S↓+4Na2SO4分析流程,解决下列问题:

(1)吸收塔中加水是为了加快溶解速率,要进行的操作是___________ 。
(2)结晶釜中结晶的方法是___________ 。
(3)写出煅烧窑中发生反应的化学方程式___________ 。
(4)该车间得到的产品是___________ 和___________ 。
(5)该流程中可循环利用的物质是___________ 。
 8S↓+4Na2SO4分析流程,解决下列问题:
8S↓+4Na2SO4分析流程,解决下列问题:
(1)吸收塔中加水是为了加快溶解速率,要进行的操作是
(2)结晶釜中结晶的方法是
(3)写出煅烧窑中发生反应的化学方程式
(4)该车间得到的产品是
(5)该流程中可循环利用的物质是
您最近一年使用:0次
综合应用题
|
适中
(0.65)
名校
【推荐2】NaCl在生产和生活中具有广泛的用途,是一种重要的资源。通过晾晒海水可以得到粗盐和母液(又叫苦卤)。下图为母液中最主要的四种盐(NaCl、KCl、MgCl2、MgSO4)的溶解度曲线图。回答下列问题:

(1)①90℃时,四种盐中MgCl2的溶解度最大,则表示MgCl2溶解度曲线的是_________ 。(填“A”或“B”)此时饱和MgCl2溶液的质量分数为_______
(请写出计算表达式即可)
②四种盐中溶解度受温度变化的影响最小的是_____________ 。 (填化学式)
(2)60℃时,若母液中的NaCl、KCl、MgCl2、MgSO4都已达到饱和,为了获得较纯净的MgSO4晶体,可采用的最好方法是_______________ 。
(3)工业上常通过加入碱溶液与母液中的Mg2+反应来制取Mg(OH)2沉淀。为了探究获得较高Mg2+沉淀率的反应条件,进行下列对比实验(每组实验取250mL母液)
①本实验研究了哪些因素对Mg2+的沉淀率的影响_______
②实验a和b对比,可得到的结论是_______
③表格中x的数值可能为__________ (填字母)。
A 95.8 B 92.1 C 97.2 D 93.1

(1)①90℃时,四种盐中MgCl2的溶解度最大,则表示MgCl2溶解度曲线的是
(请写出计算表达式即可)
②四种盐中溶解度受温度变化的影响最小的是
(2)60℃时,若母液中的NaCl、KCl、MgCl2、MgSO4都已达到饱和,为了获得较纯净的MgSO4晶体,可采用的最好方法是
(3)工业上常通过加入碱溶液与母液中的Mg2+反应来制取Mg(OH)2沉淀。为了探究获得较高Mg2+沉淀率的反应条件,进行下列对比实验(每组实验取250mL母液)
| 实验序号 | 反应温度/℃ | 反应时间/min | 反应pH值 | Mg2+的沉淀率/% |
| a | 40 | 60 | 10 | 90.1 |
| b | 40 | 60 | 12 | 92.7 |
| c | 40 | 90 | 12 | 93.6 |
| d | 50 | 60 | 12 | 96.4 |
| e | 50 | 90 | 12 | X |
①本实验研究了哪些因素对Mg2+的沉淀率的影响
②实验a和b对比,可得到的结论是
③表格中x的数值可能为
A 95.8 B 92.1 C 97.2 D 93.1
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐3】驰行中的化学——跑出发展“加速度”
Ⅰ、2022年我国燃油汽车年产量达2702.1万辆,其使用的燃料主要是汽油或柴油。
(1)石油炼制可得到汽油和柴油。除石油外,人们常用的化石燃料还有天然气和______ 。
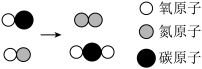
(2)燃油汽车排气系统中安装的“三元催化器”能将尾气中的有害气体转化成无毒气体,反应的微观示意图如下、下列说法错误的是______(填标号)。
Ⅱ、近年来我国大力推广新能源汽车,2022年我国新能源汽车年产量达705.8万辆。新能源汽车常用锂电池供电,碳酸锂( )是制备锂电池的重要原料。工业上以锂辉石(主要成分为
)是制备锂电池的重要原料。工业上以锂辉石(主要成分为 )为原料制取碳酸锂,其主要工艺流程如下图所示:
)为原料制取碳酸锂,其主要工艺流程如下图所示:
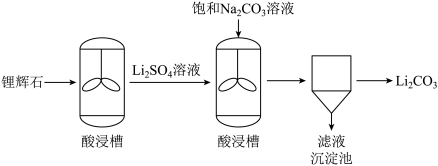
(3)酸浸槽中加入的酸是______ 。
(4)反应器中发生反应的化学方程式为______ 。
(5)下表为Li2SO4和Na2SO4在不同温度下的溶解度
①20°C时,在50g水中加入18gLi2SO4,形成溶液的质量为______ g;
②若Na2SO4中混有少量Li2SO4,要得到较纯净的Na2SO4,可采用______ 的方法(填“过滤”或“冷却热饱和溶液”)。
Ⅰ、2022年我国燃油汽车年产量达2702.1万辆,其使用的燃料主要是汽油或柴油。
(1)石油炼制可得到汽油和柴油。除石油外,人们常用的化石燃料还有天然气和
(2)燃油汽车排气系统中安装的“三元催化器”能将尾气中的有害气体转化成无毒气体,反应的微观示意图如下、下列说法错误的是______(填标号)。

| A.反应前后原子个数没有发生改变 |
| B.反应前后分子个数没有发生改变 |
| C.反应前后各元素化合价均未发生改变 |
| D.参加反应的两种物质的质量比为14:15 |
Ⅱ、近年来我国大力推广新能源汽车,2022年我国新能源汽车年产量达705.8万辆。新能源汽车常用锂电池供电,碳酸锂(
 )是制备锂电池的重要原料。工业上以锂辉石(主要成分为
)是制备锂电池的重要原料。工业上以锂辉石(主要成分为 )为原料制取碳酸锂,其主要工艺流程如下图所示:
)为原料制取碳酸锂,其主要工艺流程如下图所示:
(3)酸浸槽中加入的酸是
(4)反应器中发生反应的化学方程式为
(5)下表为Li2SO4和Na2SO4在不同温度下的溶解度
温度/℃ | 0 | 10 | 20 | 30 | 40 | |
溶解度/g | Li2SO4 | 36.1 | 35.4 | 34.8 | 34.3 | 33.9 |
Na2SO4 | 4.9 | 9.1 | 19.5 | 40.8 | 48.8 | |
②若Na2SO4中混有少量Li2SO4,要得到较纯净的Na2SO4,可采用
您最近一年使用:0次
【推荐1】氯化铵( )是农业生产中的一种肥料。兴趣小组的同学开展了有关氯化铵项目的研究。
)是农业生产中的一种肥料。兴趣小组的同学开展了有关氯化铵项目的研究。
项目一:氯化铵的性质
(1)氯化铵是一种白色固体粉末,描述的是氯化铵的_____ (填“物理”或“化学”)性质。
(2)鉴别尿素[ ]和氯化铵
]和氯化铵_____ (填“能”或“不能”)用加熟石灰研磨的方法。
项目二:氯化铵的制备
(3)如图,两集气瓶中分别装满氨气 和氯化氢
和氯化氢 气体,抽去两集气瓶之间的玻璃片,二者接触后产生大量白烟。白烟是氯化铵固体小颗粒。
气体,抽去两集气瓶之间的玻璃片,二者接触后产生大量白烟。白烟是氯化铵固体小颗粒。
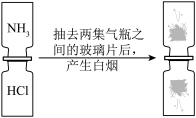
该实验可以说明分子在_____ 。
项目三:氯化铵的用途
(4)用氯化铵固体配制无土栽培营养液。 时,取
时,取 固体放入100g水中充分溶解,得到的甲溶液按如图所示进行操作:
固体放入100g水中充分溶解,得到的甲溶液按如图所示进行操作:

①甲、乙溶液的溶质质量分数大小关系为_____ 。丙溶液是_____ (填“饱和”或“不饱和”)溶液。
② 时
时 的溶解度为
的溶解度为_____ g。
 )是农业生产中的一种肥料。兴趣小组的同学开展了有关氯化铵项目的研究。
)是农业生产中的一种肥料。兴趣小组的同学开展了有关氯化铵项目的研究。项目一:氯化铵的性质
(1)氯化铵是一种白色固体粉末,描述的是氯化铵的
(2)鉴别尿素[
 ]和氯化铵
]和氯化铵项目二:氯化铵的制备
(3)如图,两集气瓶中分别装满氨气
 和氯化氢
和氯化氢 气体,抽去两集气瓶之间的玻璃片,二者接触后产生大量白烟。白烟是氯化铵固体小颗粒。
气体,抽去两集气瓶之间的玻璃片,二者接触后产生大量白烟。白烟是氯化铵固体小颗粒。
该实验可以说明分子在
项目三:氯化铵的用途
(4)用氯化铵固体配制无土栽培营养液。
 时,取
时,取 固体放入100g水中充分溶解,得到的甲溶液按如图所示进行操作:
固体放入100g水中充分溶解,得到的甲溶液按如图所示进行操作:
①甲、乙溶液的溶质质量分数大小关系为
②
 时
时 的溶解度为
的溶解度为
您最近一年使用:0次
【推荐2】不同温度下,碳酸钠和碳酸氢钠的溶解度如表所示
(1)碳酸氢钠俗称__________ 。
(2)服用碳酸氢钠治疗胃酸过多时,胃液的pH__ (填“增大”、“减小”或“不变”),发生反应的化学方程式是__________ 。
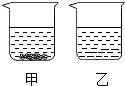
(3)为区分碳酸钠和碳酸氢钠两种白色固体.在20℃时,各盛有50mL水的甲、乙两烧杯中,分别加入等质量的碳酸钠和碳酸氢钠固体,充分溶解后,现象如图所示.乙烧杯中加入的物质是_____ (填化学式),加入的质量m的范围为:________ 。
| 温度/℃ | 0 | 20 | 40 | 60 |
| 碳酸钠 | 7.0 | 21.8 | 48.8 | 46.4 |
| 碳酸氢钠 | 6.9 | 9.6 | 12.7 | 16.4 |
(1)碳酸氢钠俗称
(2)服用碳酸氢钠治疗胃酸过多时,胃液的pH
(3)为区分碳酸钠和碳酸氢钠两种白色固体.在20℃时,各盛有50mL水的甲、乙两烧杯中,分别加入等质量的碳酸钠和碳酸氢钠固体,充分溶解后,现象如图所示.乙烧杯中加入的物质是

您最近一年使用:0次
综合应用题
|
适中
(0.65)
【推荐3】水和溶液与我们的生活息息相关。
(1)将厨房中的下列物质:胡椒、花生油、面粉、白糖分别放入水中,能形成溶液的是_____ 。
(2)消毒液碘酒中的溶剂是_____ (写名称)。
(3)甲、乙、丙三种固体物质的溶解度曲线如图所示,回答下列问题:

①在t2°C时,甲的溶解度为_____ ,把30g甲溶解在50g水中得到溶液的质量为_____ 克。
②把N点甲的溶液转化为M点溶液的方法(写一种)_____ 。
③将甲、乙、丙三种物质的饱和溶液从t3°C降到t2°C,溶质质量分数由大到小的顺序是_____ 。
④要配制等质量t3°C的甲、乙、丙三种物质的饱和溶液,所需水的质量最多是_____ 。配制过程中若量取水时仰视读数,则会造成所配溶液的溶质质量分数_____ 。(“偏大”或“偏小”)
(1)将厨房中的下列物质:胡椒、花生油、面粉、白糖分别放入水中,能形成溶液的是
(2)消毒液碘酒中的溶剂是
(3)甲、乙、丙三种固体物质的溶解度曲线如图所示,回答下列问题:

①在t2°C时,甲的溶解度为
②把N点甲的溶液转化为M点溶液的方法(写一种)
③将甲、乙、丙三种物质的饱和溶液从t3°C降到t2°C,溶质质量分数由大到小的顺序是
④要配制等质量t3°C的甲、乙、丙三种物质的饱和溶液,所需水的质量最多是
您最近一年使用:0次
【推荐1】根据化学知识回答:
Ⅰ、溶液颜色的变化蕴含许多知识。
(1)下列物质加入水中能形成有色溶液的是______。
(2)进行水电解实验时,将含酚酞的稀Na2SO4溶液(呈中性且不参与反应)加入如图所示的装置中,打开电源。
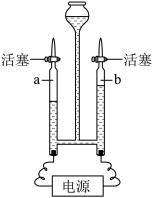
①a管中收集到的气体是______ ,a、b两管中收集到的气体质量比为______ 。
②通电后b管电极处溶液呈红色,电解结束后将容器内所有液体倒入烧杯中混合均匀,溶液又呈无色。下列说法正确的是______ 。
A.Na2SO4溶液使酚酞变红
B.电解过程中,b电极处中有酸性物质生成
C.待溶液混合均匀后呈无色,说明电解时a电极附近溶液呈酸性
Ⅱ、食盐的用途广泛,在工业上是制备纯碱的原料之一。1926年我国科学家侯德榜创立侯氏制碱法,大大提高了食盐的利用率,促进了世界制碱技术的发展。如图为氯化铵、氯化钠的溶解度曲线。试回答下列问题:

(3)t2℃时,NH4CI饱和溶液的溶质质量分数______ NaCl的饱和溶液的溶质质量分数(填“大于”“等于”或“小于”)。
(4)将t2℃时,将30gNH4Cl固体加入到50g水中,充分溶解后,所得NH4Cl溶液的溶质质量分数______ (列式,无需计算结果)。
(5)若NH4Cl中含有少量的NaCl,提纯NH4Cl可以用______ 法。
Ⅰ、溶液颜色的变化蕴含许多知识。
(1)下列物质加入水中能形成有色溶液的是______。
| A.碳酸钙 | B.高锰酸钾 | C.植物油 | D.食盐 |

①a管中收集到的气体是
②通电后b管电极处溶液呈红色,电解结束后将容器内所有液体倒入烧杯中混合均匀,溶液又呈无色。下列说法正确的是
A.Na2SO4溶液使酚酞变红
B.电解过程中,b电极处中有酸性物质生成
C.待溶液混合均匀后呈无色,说明电解时a电极附近溶液呈酸性
Ⅱ、食盐的用途广泛,在工业上是制备纯碱的原料之一。1926年我国科学家侯德榜创立侯氏制碱法,大大提高了食盐的利用率,促进了世界制碱技术的发展。如图为氯化铵、氯化钠的溶解度曲线。试回答下列问题:

(3)t2℃时,NH4CI饱和溶液的溶质质量分数
(4)将t2℃时,将30gNH4Cl固体加入到50g水中,充分溶解后,所得NH4Cl溶液的溶质质量分数
(5)若NH4Cl中含有少量的NaCl,提纯NH4Cl可以用
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐2】已知KNO3和KCl在不同温度时的溶解度如下表。请回答下列问题:
(1)依据上表数据,绘制了KNO3和KCl的溶解度曲线如图,能代表KNO3溶解度曲线的是_______ (填“a”或“b”)。
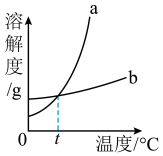
(2)分析表中数据,t的范围为_______(填字母序号)。
(3)40℃时,分别将30gKNO3和KCl加到50g水中,充分溶解后一定能形成饱和溶液的物质是_______ ,其溶液的溶质质量分数为_______ (结果精确到0.1%)。
(4)若KNO3中混有少量KCl,可采用_______ 的方法提纯KNO3。
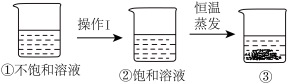
(5)下图是有关KNO3溶液的实验操作及变化情况。下列说法中正确的是_______。
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | |
| 溶解度/g | KNO3 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 |
| KCl | 27.6 | 31.0 | 34.0 | 37.0 | 40.0 | 42.6 | 45.5 | |
(1)依据上表数据,绘制了KNO3和KCl的溶解度曲线如图,能代表KNO3溶解度曲线的是

(2)分析表中数据,t的范围为_______(填字母序号)。
A. | B. | C. | D. |
(3)40℃时,分别将30gKNO3和KCl加到50g水中,充分溶解后一定能形成饱和溶液的物质是
(4)若KNO3中混有少量KCl,可采用
(5)下图是有关KNO3溶液的实验操作及变化情况。下列说法中正确的是_______。

| A.操作Ⅰ一定是降温 | B.①与②的溶液质量可能相等 |
| C.②与③的溶质质量一定相等 | D.②与③的溶质质量分数一定相等 |
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐3】氯化钠是生产、生活中的一种重要化合物,应用很广泛。
【微观探索】
图甲和图乙分别是钠原子和氯原子的结构示意图。___________ 。
(2)金属钠与氯气反应时,由图乙的结构可知,氯原子容易得到钠失去的1个电子,从而形成最外层有___________ 个电子的相对稳定的氯离子,氯离子用化学符号表示为___________ 。
【实验室操作】
下表是氯化钠在不同温度下的溶解度数据。
(3)30℃时,将10g氯化钠加入到50g水中,充分搅拌后,所得到的氯化钠溶液属于___________ (填“饱和”或“不饱和”)溶液。
(4)医用盐水(溶质为NaCl)的溶质质量分数为0.9%,现有200mL该盐水(假定该溶液的密度为1g/mL),其中含NaCl的质量为___________ g。
【工业应用】
海洋是人类宝贵的自然资源,海水“制盐”体现了人类利用化学科学征服和改造自然的智慧。通过晾晒海水,可以得到粗盐,粗盐中含有不溶性杂质(如泥沙等)和可溶性杂质(如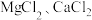 等)。
等)。
工业上以粗盐为原料制取精盐,其生产流程如图所示。
资料:部分物质的溶解性表(室温)
___________ 。
(6)加入Na2CO3溶液除去的离子是__________ (填离子符号),加入NaOH溶液发生反应的化学方程式是______ 。
(7)滤液中溶质的主要成分是_________ (填化学式),加入足量稀盐酸的目的是________ 。
(8)如果称量I中称得粗盐的质量为3g,称量中称得精盐的质量为3.1g,则下列分析正确的是___________(填字母)。
【微观探索】
图甲和图乙分别是钠原子和氯原子的结构示意图。

(2)金属钠与氯气反应时,由图乙的结构可知,氯原子容易得到钠失去的1个电子,从而形成最外层有
【实验室操作】
下表是氯化钠在不同温度下的溶解度数据。
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 |
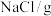 | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 | 37.8 |
(3)30℃时,将10g氯化钠加入到50g水中,充分搅拌后,所得到的氯化钠溶液属于
(4)医用盐水(溶质为NaCl)的溶质质量分数为0.9%,现有200mL该盐水(假定该溶液的密度为1g/mL),其中含NaCl的质量为
【工业应用】
海洋是人类宝贵的自然资源,海水“制盐”体现了人类利用化学科学征服和改造自然的智慧。通过晾晒海水,可以得到粗盐,粗盐中含有不溶性杂质(如泥沙等)和可溶性杂质(如
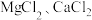 等)。
等)。工业上以粗盐为原料制取精盐,其生产流程如图所示。
资料:部分物质的溶解性表(室温)
| OH- |  | |
| Ca2+ | 微溶 | 不溶 |
| Mg2+ | 不溶 | 微溶 |
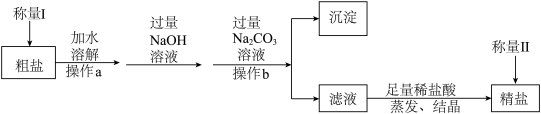
(6)加入Na2CO3溶液除去的离子是
(7)滤液中溶质的主要成分是
(8)如果称量I中称得粗盐的质量为3g,称量中称得精盐的质量为3.1g,则下列分析正确的是___________(填字母)。
| A.精盐的产率为103.3% | B.蒸发操作中可能有水分没有蒸干 |
| C.除杂过程中有NaCl生成 | D.溶解操作中粗盐没有完全溶解 |
您最近一年使用:0次
综合应用题
|
适中
(0.65)
名校
解题方法
【推荐1】(一)物质间的转化
如图所示,“一”表示相连的两物质可发生反应,“→”表示可以向箭头所指方向一步转化,部分反应物、生成物均已略去;所涉及的物质和反应在初中化学中均较常见,且A一E为五种不同类别的物质(指单质、氧化物、酸、碱、盐),A的浓溶液在实验室中常用作干燥剂。B为年产量最高的金属。请回答:
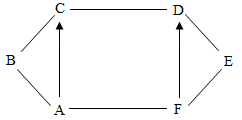
(1)A的化学式为______ 。
(2)D与E的化学方程式可能为______ (写一个即可)。
(二)化学工艺流程
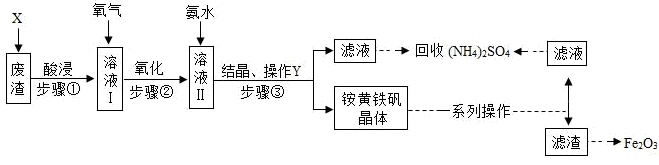
工业上利用某废渣[含FeSO4、Fe2(SO4)3及少量CaO和MgO]制备高档颜料铁红(主要成分为Fe2O3)和回收(NH4)2SO4,具体生产流程如图:
【查阅资料】
a.氧化还原反应中,会有元素化合价发生变化。
b.3Fe2(SO4)3+12NH3•H2O═(NH4)2Fe6(SO4)4(OH)12↓(铵黄铁钒晶体)+5(NH4)2SO4
(3)步骤①酸浸加入物质X应选用______ 。
A.盐酸 B.硫酸 C.氨水 D.氢氧化钠
(4)步骤①酸浸时,请写出一个生成盐的化学反应方程式______ (任写一个)。
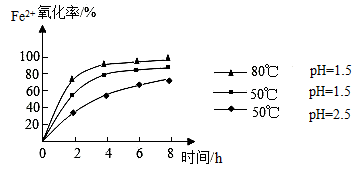
(5)步骤②通入氧气氧化的目的是______ 。根据如图有关数据分析,请写出影响氧化率的变化规律______ 。
(6)步骤③中操作Y的名称是______ ,最后回收得到的副产品(NH4)2SO4有什么用途______ (写一点)。
如图所示,“一”表示相连的两物质可发生反应,“→”表示可以向箭头所指方向一步转化,部分反应物、生成物均已略去;所涉及的物质和反应在初中化学中均较常见,且A一E为五种不同类别的物质(指单质、氧化物、酸、碱、盐),A的浓溶液在实验室中常用作干燥剂。B为年产量最高的金属。请回答:

(1)A的化学式为
(2)D与E的化学方程式可能为
(二)化学工艺流程
工业上利用某废渣[含FeSO4、Fe2(SO4)3及少量CaO和MgO]制备高档颜料铁红(主要成分为Fe2O3)和回收(NH4)2SO4,具体生产流程如图:

【查阅资料】
a.氧化还原反应中,会有元素化合价发生变化。
b.3Fe2(SO4)3+12NH3•H2O═(NH4)2Fe6(SO4)4(OH)12↓(铵黄铁钒晶体)+5(NH4)2SO4
(3)步骤①酸浸加入物质X应选用
A.盐酸 B.硫酸 C.氨水 D.氢氧化钠
(4)步骤①酸浸时,请写出一个生成盐的化学反应方程式
(5)步骤②通入氧气氧化的目的是

(6)步骤③中操作Y的名称是
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐2】诺贝尔化学奖得主德国化学家Gerhard Ertl对CO与 在催化剂
在催化剂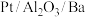 表面进行的研究,催生了汽车尾气净化装置。下图为该反应过程的模型,回答下列问题:
表面进行的研究,催生了汽车尾气净化装置。下图为该反应过程的模型,回答下列问题:

(1)该装置的最大贡献是___________ ,写出图中所示反应的化学方程式___________ 。
(2)以下各项中,在化学反应前后肯定不发生变化的是:___________ (填序号)。
①元素的种类 ②原子的质量 ③分子的种类 ④原子的数目
(3)氨气是一种重要的化工原料,工业上常用氨气来处理有毒气体 ,反应原理是:
,反应原理是: ,其中X的化学式是
,其中X的化学式是___________ 。
(4)科学合理施用化肥和农药,开发研制与推广使用新型高效、低毒、低残留肥料和农药是实现农业良性发展的需要。以下做法合理的是___________ (填序号)。
①为提高产量,尽量多地使用氮、磷、钾肥
②给韭菜施用大量有机磷农药以杀死害虫
③铵态氮肥不与碱性物质混用
④在蔬菜大棚中适量补充二氧化碳以促进光合作用
(5)碧水蓝天是盛世美景,保护水资源,人人有责。下列对水资源保护的做法正确的是___________(填字母序号)。
 在催化剂
在催化剂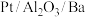 表面进行的研究,催生了汽车尾气净化装置。下图为该反应过程的模型,回答下列问题:
表面进行的研究,催生了汽车尾气净化装置。下图为该反应过程的模型,回答下列问题:
(1)该装置的最大贡献是
(2)以下各项中,在化学反应前后肯定不发生变化的是:
①元素的种类 ②原子的质量 ③分子的种类 ④原子的数目
(3)氨气是一种重要的化工原料,工业上常用氨气来处理有毒气体
 ,反应原理是:
,反应原理是: ,其中X的化学式是
,其中X的化学式是(4)科学合理施用化肥和农药,开发研制与推广使用新型高效、低毒、低残留肥料和农药是实现农业良性发展的需要。以下做法合理的是
①为提高产量,尽量多地使用氮、磷、钾肥
②给韭菜施用大量有机磷农药以杀死害虫
③铵态氮肥不与碱性物质混用
④在蔬菜大棚中适量补充二氧化碳以促进光合作用
(5)碧水蓝天是盛世美景,保护水资源,人人有责。下列对水资源保护的做法正确的是___________(填字母序号)。
| A.为了改善水质,向其中加入大量的净水剂和消毒剂 |
| B.为保护好水资源,禁止使用化肥和农药 |
| C.大量开采利用地下水 |
| D.工业废水处理达标后再排放 |
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐3】“二十四节气”是我国古代农耕文化的产物,农耕生产与节气息息相关。
(1)“立春”:万物复苏,春暖花开。乙酸笨甲酯(C9H10O2)是一种具有茉莉花香味的物质,乙酸苯甲酯分子中氢原子和氧原子的个数比是____________ (填最简整数比)。
(2)“谷雨”:时雨乃降,百果乃登。正常雨水略显酸性,原因是___________ (化学方程式表示)。pH<5.6的雨水容易导致土壤酸化,不利于农作物生长,常用______ 改良酸性土壤。
(3)“小满”:小满不满,麦有一险。为促进小麦生长,需追加肥料。
①下列肥料属于复合肥的是_________ (填字母)。
A.CO(NH2)2 B.Ca3(PO4)2 C.NH4NO3 D.KNO3
②草木灰是一种钾肥,主要成分是碳酸钾,一般不与铵态氮肥混合使用。据此推测,碳酸钾溶液中的阴离子主要是____________ 。
(4)“夏至”:夏至杨梅满山红。杨梅中含有丰富的钙、磷、铁等元素,补充铁元素可以预防___________ 。
(5)“秋分”:一粒好种,万担好粮。农业上常用溶质质量分数为16%的氯化钠溶液来选种。现有100g溶质质量分数为26.5%的氯化钠溶液,配成溶质质量分数为16%的氯化钠溶液加多少克水即可。(写出计算过程,结果保留一位小数)
(1)“立春”:万物复苏,春暖花开。乙酸笨甲酯(C9H10O2)是一种具有茉莉花香味的物质,乙酸苯甲酯分子中氢原子和氧原子的个数比是
(2)“谷雨”:时雨乃降,百果乃登。正常雨水略显酸性,原因是
(3)“小满”:小满不满,麦有一险。为促进小麦生长,需追加肥料。
①下列肥料属于复合肥的是
A.CO(NH2)2 B.Ca3(PO4)2 C.NH4NO3 D.KNO3
②草木灰是一种钾肥,主要成分是碳酸钾,一般不与铵态氮肥混合使用。据此推测,碳酸钾溶液中的阴离子主要是
(4)“夏至”:夏至杨梅满山红。杨梅中含有丰富的钙、磷、铁等元素,补充铁元素可以预防
(5)“秋分”:一粒好种,万担好粮。农业上常用溶质质量分数为16%的氯化钠溶液来选种。现有100g溶质质量分数为26.5%的氯化钠溶液,配成溶质质量分数为16%的氯化钠溶液加多少克水即可。(写出计算过程,结果保留一位小数)
您最近一年使用:0次



