【提出问题】这瓶无色溶液是什么物质的溶液?
【猜想与假设】小组同学提出了如下假设:
①碳酸钠溶液;②硫酸钠溶液;③氯化钠溶液
【讨论交流】在老师的指导下,小组同学经过讨论,认为有一条假设不合理。
(1)请你指出不合理的假设并说明不合理的理由
【查阅资料】硫酸钡既不溶解于水又不溶解于酸;碳酸钠溶液呈碱性;Ba(OH)2 的化学性质与 Ca(OH)2相似。
【进行实验】小组同学设计并进行了如下实验,请你完善小组同学的“相互评价”。
| 组次 | 实验操作 | 出现的现象与结论 | 同学相互评价 |
| 第 1 组 | 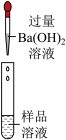 | 产生白色沉淀,第 1 组同学认为猜想②成立 | 第 2 组同学认为此方案结论不正确。 (2)你认为其理由是硫酸钡和 |
| 第 2 组 | 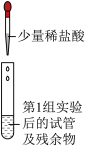 | 试管中无明显现象,第2 组同学认为猜想 ②成立。 | 第3组同学认为此方案结论不正确。 (3)你认为其理由是 |
| 第 3 组 | 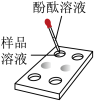 | 溶液无明显变化,第 3 组同学认为猜想②成立。 | 第 1 组同学认为此方案结论正确。 (4)你认为实验中用点滴板比试管具有更多的优点是 (写 1 条即可)。 |
(5)你认为倾倒液体药品时,要注意标签
相似题推荐

【提出问题】试管②中没有明显现象,是否发生了反应?
【实验探究】
(1)化学兴趣小组取少量实验后试管②中的溶液,分别放入a、b两支试管中,向a试管中滴入酚酞溶液,观察到了
A Zn B Fe(OH)3 C FeCl3 D AgNO3
(2)化学兴趣小组又利用pH传感器探究稀盐酸和氢氧化钠溶液的反应过程。实验操作和测定结果如图所示:
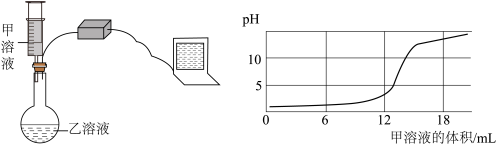
②加入甲溶液6mL时,烧瓶中的溶液溶质成分
③根据该实验测定结果,判断发生化学反应的依据是
【查阅资料】
I、离子浓度越大,溶液的导电性越强,电导率越大。
II、室温下,一些物质的电导率数值如下表[稀硫酸、Ba(OH)2溶液的浓度相同,设为c]。
| 物质 | 蒸馏水 | 稀硫酸 | Ba(OH)2溶液 | BaSO4悬浊液 |
| 电导率(μS/cm) | 3 | 3921 | 3273 | 3 |
任务一:探究NaOH溶液与稀硫酸反应
如图1,往滴有酚酞的 NaOH溶液中逐滴滴入稀硫酸。测得溶液的pH变化曲线如图2。

(1)c点所示的溶液中,含有的溶质是
(2)a、b、c三点所示溶液呈无色的是
(3)从a点到b点溶液的导电性逐渐减弱,其原因是
任务二:Ba(OH)2溶液与稀硫酸反应
【实验设计与探究】
按图3所示组装连接好仪器,在烧杯中加入浓度为c的Ba(OH)2溶液。开启磁力搅拌器,逐滴滴加相同浓度的稀硫酸,测得溶液的电导率变化曲线如图4。
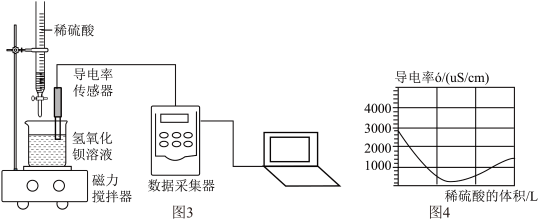
(4)实验开始前,测得Ba(OH)2溶液的电导率低于3273μS/cm的原因是
(5)反应过程中,电导率最小值可能是
任务三:碳酸钾与稀硫酸反应
(6)取少量碳酸钾于试管中,逐滴滴加稀硫酸,观察到的现象
【实验结论】
(7)结合已学知识可知,在溶液中,复分解反应发生的实质是参与反应的离子结合生成了沉淀、气体或水,导致离子浓度
(1)碳酸氢钠的俗名为
【问题 1】碳酸氢钠溶液与碳酸钠溶液的酸碱性
【实验 1】用 pH 计测定等浓度的碳酸氢钠和碳酸钠溶液的 pH,分别为 9.0 和 12.0;
【结论 1】两种溶液都呈碱性,它们的碱性强弱顺序为
【问题 2】碳酸氢钠溶液、碳酸钠溶液与酸的反应
【实验 2】等浓度的碳酸氢钠和碳酸钠溶液分别与相同浓度的盐酸反应操作和现象如下表:
| 序号 | 操作 | 现象 |
| 实验① | 碳酸氢钠溶液逐滴加入盐酸中 | 立刻产生气泡 |
| 实验② | 碳酸钠溶液逐滴加入盐酸中 | 立刻产生气泡 |
| 实验③ | 盐酸逐滴加入碳酸氢钠溶液中 | 立刻产生气泡 |
| 实验④ | 盐酸逐滴加入中碳酸钠溶液中 | 滴加一会后才有气泡产生 |
【实验 3】将等浓度的碳酸氢钠和碳酸钠溶液与相同浓度的盐酸互滴,利用手持传感器测定反应中溶液 pH 变化,四个实验的 pH 变化与时间的关系如图所示。

【分析】
(2)如图 4 表示的实验是
(3)比较图 3 与图 2 发现:图 3 中的阴影部分与图 2 叠合后,图象基本重合。则图 3 中的 AB 段发生反应的化学方程式为
【实验 4】分别向pH为 12 的碳酸钠溶液、pH为 9 的碳酸氢钠溶液中滴入 2~3 滴酚酞溶液,观察到碳酸钠溶液中酚酞呈红色,碳酸氢钠溶液中酚酞呈浅红色。
【实验 5】向滴入 2~3 滴酚酞溶液 pH 为 12 的碳酸钠溶液中不断通入纯净二氧化碳,观察到酚酞溶液由红色逐渐变为浅红色,且试管底部出现少量白色固体,用 pH 计测得最后溶液 pH为 9。
(4)用化学方程式解释酚酞溶液由红色变为浅红的原因
(5)试管底部出现少量白色固体,说明
【应用】(6)如何除去碳酸氢钠溶液中的碳酸钠
I.定性探究
实验一:探究鸡蛋壳的主要成分
【查阅资料】鸡蛋壳中含钙元素。
【实验步骤和现象】取一些鸡蛋壳于一支洁净的试管中,加入过量稀盐酸,产生无色无气味的气体,将该气体通入澄清石灰水中,石灰水变浑浊。
【结论】
写出该气体通入澄清石灰水中的化学反应方程式
实验二:做无壳鸡蛋
【实验步骤和现象】如图所示:将一个新鲜鸡蛋放入水中,鸡蛋沉入水底。加入量浓盐酸后,鸡蛋会出现上浮、下沉、再上浮、再下沉的现象,反复多次。最后变成无壳鸡蛋。
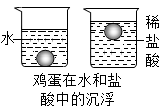
【解释与交流】用化学和物理知识解释鸡蛋上浮、下沉多次的原因
Ⅱ.定量探究
化学兴趣小组为了测定鸡蛋壳中主要成分的含量(其它成分不溶于水也不与酸反应)做如下实验。取用2.00 g鸡蛋壳样品,把20.00 g稀盐酸分4次加入样品中,充分反应后过滤,取滤渣,洗涤、干燥、称量,得实验数据如下:
| 稀盐酸的用量 | 剩余固体的质量 |
| 第一次加入5.00 g | 1.50 g |
| 第二次加入5.00 g | 1.00 g |
| 第三次加入5.00 g | 0.50 g |
| 第四次加入5.00 g | 0.30 g |
(1)从以上数据可知,这四次实验中,第
[(2)(3)计算过程中和最后数字精确到0.01,若是百分数,则精确到0.1%]
(2)求出鸡蛋壳中主要成分的含量和所用稀盐酸的溶质质量分数为
(3)在上述实验所得滤液中加30.00g水,加入
(4)用36.5%的浓盐酸配制20.00g上述稀盐酸需加水的体积为

【活动一】探究人体呼出气体中是否含有CO2
(1)向装有呼出气体的集气瓶中滴加少量澄清石灰水,振荡后观察到
【活动二】探究人体呼出气体中CO2的体积分数
(2)兴趣小组同学用图1所示装置进行实验。(锥形瓶内充满人体呼出的气体)实验前注射器内液体体积为50mL,向锥形瓶内注入少量液体后,注射器内的液体开始被自动吸入锥形瓶,充分反应后,注射器内NaOH溶液的体积为30mL。锥形瓶内发生的化学反应方程式为:
小亮同学提出疑问:锥形瓶内CO2是否反应完?
(3)同学们展开了激烈的讨论,设计实验并证明锥形瓶内无色溶液中确实含有NaOH,得出锥形瓶内CO2已反应完。
| 实验步骤 | 实验现象 | 实验结论 |
| |①取少量锥形瓶内无色溶液于试管中, 加入过量氯化钙溶液; ②过滤,向滤液中滴加几滴酚酞溶液 | ③ ④ | 无色溶液中含有NaOH |
(4)结论:人体呼出气体中CO2的体积分数为
【活动三】探究人体呼出气体中O2的体积分数
兴趣小组同学用图2所示装置进行实验。(注射器及玻璃管内充满人体呼出的气体)
(5)实验中需反复推拉注射器的目的是
(6)在操作中如何判断装置中的O2是否反应完?
结论:人体呼出气体中O2的体积分数为16%。
【实验反思】
(7)活动三所用方法与教科书上“测定空气里O2的含量”的方法相比,其优点是:

【观察与记录】A烧杯中发生反应的化学方程式(1)
实验后同学们将A烧杯中物质过滤,将所得滤液和B烧杯中物质集中到同 一废液缸中,观察到有白色沉淀产生,同学们将固液混合物过滤后得到C烧杯中滤液和滤渣D。同学们对C烧杯中滤液产生了浓厚的兴趣,进行了进一步的探究活动。
【提出问题】C烧杯滤液中含有哪些离子?
【实验探究】同学们根据以上实验及所学知识讨论后,甲同学取滤渣D,乙、丙同学取C烧杯中滤液做了如下的探究实验:

【评价与交流】甲同学根据实验现象分析得出结论:C烧杯中滤液一定不含有(2)
丙同学通过实验现象得出C烧杯中滤液一定含有的离子是(4)
【实验结论】综合上述所有实验及推理分析,经小组同学讨论后,最终确定了C烧杯中滤液的离子成分为(5)
【归纳与总结】通过上述实验探究过程,可以总结出,证明反应后溶液中的离子成分的思路是:首先根据实验现象及离子的化学性质等推测出一定存在的离子,并且无需证明,然后再针对可能存在的离子设计实验进行证明,但是要注意所选试剂不能同时和(6)
【推荐1】聊城市某学校2019年实验操作模拟训练的一个题目是:鉴别稀硫酸,稀盐酸和氢氧化钠三种无色溶液。小组的同学把标有序号1、2、3的三种溶液分别滴入标有对应序号的三支试管中,向三支试管中滴加酚酞试液,如甲图,鉴别出1号溶液,再向另两支试管中滴加BaCl2溶液,如乙图。
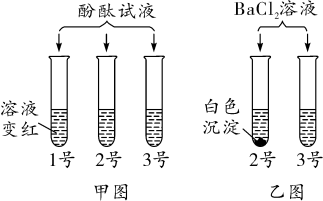
请回答:
(1)1号试管中是
(2)乙图中2号试管发生化学反应的实质是
【提出问题】除含有酚酞外,滤液中溶质的成分是什么?
【猜想假设】猜想一:HCl;猜想二:HCl和
【进行实验】①取一定量的滤液于试管中,向试管中滴加Na2SO4溶液,有白色沉淀生成,猜想
②为了验证该滤液的酸碱性,将一片pH试纸放在干燥的玻璃片上,用
【交流拓展】2号试管中滤液显酸性,要将该滤液调至中性,可向滤液中加入适量
A铁粉 B氯化钙溶液 C石灰石
探究一:探究物质的性质
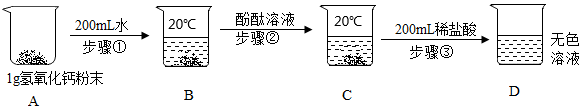
以上每个操作步骤均充分搅拌后静置,回答以下问题:
(1). C中溶液为
(2). 通过步骤①②中的现象说明氢氧化钙的溶解性是
(3). 步骤③发生反应的化学方程式为
探究二:探究物质的成分
有一包白色粉末,可能含有氢氧化钠、硫酸钠、碳酸钠、硫酸铜中的一种或几种。取少量白色粉末于烧杯中,加足量的水溶解,得到无色溶液A,滴加几滴酚酞,得红色溶液B.为进一步确定白色粉末成分,两个小组的同学分别进行了如图操作:
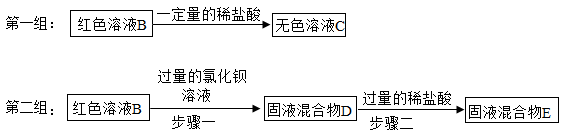
(1) 若白色粉末中含有碳酸钠,则第一组同学观察到实验现象是
(2)若固液混合物D中的溶液为红色,则原白色粉末的成分有
(3)实验结束后,第一、二组的同学将废液倒入同一烧杯中,然后过滤,滤液中除酚酞外一定还含有的溶质是
【资料卡片】BaCl2溶液显中性。
【初步结论】
甲同学根据固体的描述确定样品中肯定没有
(填化学式)。
【初步探究】
同学们设计的实验过程及现象如图所示。

【交流讨论】
同学们认为:无色溶液 M 中一定含有
【提出问题】
使溶液 M 显碱性的物质是什么?
【猜想与假设】
猜想一:是氢氧化钠;猜想二:是碳酸钠;猜想三:是氢氧化钠和碳酸钠。
【探究与结论】
(1)乙同学取无色溶液 M 于试管中,加入过量的氯化钡溶液,振荡,静置,观察到
(2)丙同学为进一步证明无色溶液 M 中的成分,进行的实验是:取乙同学实验所得上层清液少许于试管中,
综合分析,乙同学加入过量氯化钡溶液的作用:
【实验结论】
原白色固体中一定有的物质是



