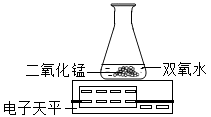
某兴趣小组同学对实验室制备氧气的条件进行如下探究实验。
①为探究催化剂的种类对氯酸钾分解速率的影响,甲设计以下对比实验:
Ⅰ中反应的化学方程式是_______ ;
Ⅱ中x的值应为________ 。
[实验结论]实验所用两种金属氧化物中,催化效果最好的是_______ 。
②乙探究了影响双氧水分解速率的某种因素,实验数据记录如下:
本实验中,测量O2体积的装置是______ (填编号)。
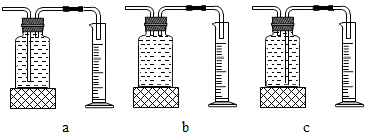
[实验结论]在相同条件下,_______ ,双氧水分解得越快。
[反思]丙用如图装置进行实验,通过比较_____ 也能达到实验目的。
①为探究催化剂的种类对氯酸钾分解速率的影响,甲设计以下对比实验:
| 编号 | 实验药品 | 分解温度(℃) |
| Ⅰ | 3.0gKClO3与1.0gMnO2均匀混合加热 | 350 |
| Ⅱ | xgKClO3与1.0gCuO均匀混合加热 | 370 |
Ⅰ中反应的化学方程式是
Ⅱ中x的值应为
[实验结论]实验所用两种金属氧化物中,催化效果最好的是
②乙探究了影响双氧水分解速率的某种因素,实验数据记录如下:
| 双氧水的质量 | 双氧水的浓度 | MnO2的质量 | 相同时间内产生O2体积 | |
| Ⅰ | 50.0g | 1% | 0.1g | 9mL |
| Ⅱ | 50.0g | 2% | 0.1g | 16mL |
| Ⅲ | 50.0g | 4% | 0.1g | 31mL |
本实验中,测量O2体积的装置是

[实验结论]在相同条件下,
[反思]丙用如图装置进行实验,通过比较

更新时间:2019-02-20 17:58:42
|
相似题推荐
【推荐1】学习了“过氧化氢制氧气使用二氧化锰作催化剂”,化学社团在“寻找新的催化剂”的活动中,对“硫酸铜能否作过氧化氢分解的催化剂”进行了以下探究。
(1)【实验探究】甲同学按如下方案进行实验。
(2)【评价改进】大家认为甲同学的实验结论不严谨。若要确定该实验结论正确,还需证明硫酸铜的___________ 在反应前后都没有发生改变。
(3)【讨论交流】大家认为:在甲同学实验的基础上,乙同学将甲同学实验时试管中的溶液蒸发、干燥得到白色固体,再称其质量为___________ g,然后将固体加入5%的过氧化氢溶液中,仍然可以加速过氧化氢分解。由此可以得出甲同学的实验结论。
(4)【拓展延伸】比较硫酸铜和二氧化锰对过氧化氢制氧气的催化效果,实验过程中不需要控制的条件是___________ (填序号)。
A.溶液的起始温度B.催化剂的质量C.溶液的浓度D.反应起始时间
(1)【实验探究】甲同学按如下方案进行实验。
| 实验步骤 | 实验现象 | 实验结论 |
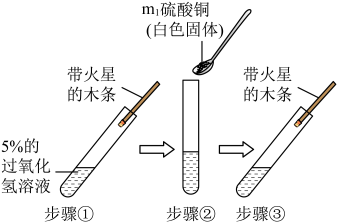 | 步骤①木条不复燃; 步骤②产生气泡,溶液变蓝色; 步骤③ | 硫酸铜能作过氧化氢分解的催化剂,反应的化学方程式为 |
(3)【讨论交流】大家认为:在甲同学实验的基础上,乙同学将甲同学实验时试管中的溶液蒸发、干燥得到白色固体,再称其质量为
(4)【拓展延伸】比较硫酸铜和二氧化锰对过氧化氢制氧气的催化效果,实验过程中不需要控制的条件是
A.溶液的起始温度B.催化剂的质量C.溶液的浓度D.反应起始时间
您最近一年使用:0次
【推荐2】学习了二氧化锰对过氧化氢分解有催化作用的知识后,我们对催化剂已有了初步的认识。某同学想:氧化铜 能否起到类似二氧化锰的催化作用呢?于是进行了以下探究。
能否起到类似二氧化锰的催化作用呢?于是进行了以下探究。
【猜想】
(1)猜想一:氧化铜不是催化剂,也不参与反应,反应前后质量和化学性质不变;
猜想二:氧化铜参与反应产生氧气,反应前后质量和化学性质发生改变;
猜想三:氧化铜是反应的催化剂,反应前后______ 。
【实验】
用天平称量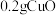 ,取
,取 5%的过氧化氢溶液于试管中,进行如图实验:
5%的过氧化氢溶液于试管中,进行如图实验:

【结论】猜想Ⅲ成立。
(2)请补充能证明猜想Ⅲ成立的实验现象:步聚③现象为______ ,步骤⑥中固体质量为______ 。
(3)步骤⑦的目的是______ 。
【拓展探究】
(4)欲比较催化剂氧化铜和二氧化锰对过氧化氢分解速率的影响,实验时需要控制相同的量有______(填字母序号)。
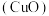 能否起到类似二氧化锰的催化作用呢?于是进行了以下探究。
能否起到类似二氧化锰的催化作用呢?于是进行了以下探究。【猜想】
(1)猜想一:氧化铜不是催化剂,也不参与反应,反应前后质量和化学性质不变;
猜想二:氧化铜参与反应产生氧气,反应前后质量和化学性质发生改变;
猜想三:氧化铜是反应的催化剂,反应前后
【实验】
用天平称量
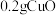 ,取
,取 5%的过氧化氢溶液于试管中,进行如图实验:
5%的过氧化氢溶液于试管中,进行如图实验:
【结论】猜想Ⅲ成立。
(2)请补充能证明猜想Ⅲ成立的实验现象:步聚③现象为
(3)步骤⑦的目的是
【拓展探究】
(4)欲比较催化剂氧化铜和二氧化锰对过氧化氢分解速率的影响,实验时需要控制相同的量有______(填字母序号)。
| A.过氧化氢溶液的浓度、体积 |
| B.过氧化氢溶液的温度 |
| C.催化剂的质量 |
| D.催化剂的种类 |
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐3】学习了MnO2对过氧化氢分解有催化作用的知识后,某同学想:CuO能否起到类似MnO2的催化剂作用呢?于是进行了以下探究.
【猜想】ⅠCuO不是催化剂、也不参与反应,反应前后质量和化学性质不变;
ⅡCuO参与反应产生O2,反应前后质量和化学性质发生了改变;
ⅢCuO是反应的催化剂,反应前后__________________ .
【实验】用天平称量0.2gCuO,取5mL5%的过氧化氢溶液于试管中,进行如下实验:
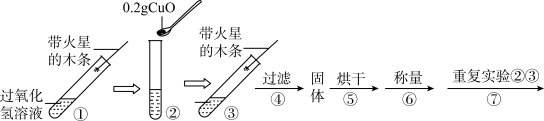
(1)填写下表:
(2)步骤①的目的是_____________________ .
(3)过氧化氢能被CuO催化分解放出O2的文字表达式为________________ ,其中CuO对反应生成的氧气的多少________ (填“有”或“无”)影响。
【猜想】ⅠCuO不是催化剂、也不参与反应,反应前后质量和化学性质不变;
ⅡCuO参与反应产生O2,反应前后质量和化学性质发生了改变;
ⅢCuO是反应的催化剂,反应前后
【实验】用天平称量0.2gCuO,取5mL5%的过氧化氢溶液于试管中,进行如下实验:

(1)填写下表:
| 步骤③现象 | 步骤⑥结果 | 步骤⑦现象 | 结论 |
| 溶液中有气泡放出, | 猜想Ⅰ、Ⅱ不成立;猜想Ⅲ成立. |
(3)过氧化氢能被CuO催化分解放出O2的文字表达式为
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐1】已知氯酸钾(KClO3)固体在二氧化锰作催化剂,在加热的条件下也可制得氧气,同时生成氯化钾(KCl)固体。写出该反应的化学方程式:____ ,该反应的基本类型是____ 。
小芳发现,氯酸钾与氧化铜混合加热,也能较快产生氧气,于是进行如下探究:
【提出猜想】除MnO2、CuO外,Fe2O3也可以作KClO3分解的催化剂。
【进行实验】按如表进行实验,并测定分解温度(分解温度越低,催化效果越好)。
【分析数据、得出结论】
(1)由实验______ 与实验④对比,证明猜想合理;
(2)实验所用的三种金属氧化物比较,氧化铜催化效果仅次于二氧化锰,请你推出其分解温度(用t表示)的取值范围:______ ;
【交流反思】
(3)若要证明Fe2O3是该反应的催化剂,还要验证它在化学反应前后的___ 和___ 不变;
(4)影响氯酸钾分解快慢除催化剂种类外,你认为还可能有的影响因素是____ (写出一种即可)。
小芳发现,氯酸钾与氧化铜混合加热,也能较快产生氧气,于是进行如下探究:
【提出猜想】除MnO2、CuO外,Fe2O3也可以作KClO3分解的催化剂。
【进行实验】按如表进行实验,并测定分解温度(分解温度越低,催化效果越好)。
| 实验编号 | 实验药品 | 分解温度(℃) |
| ① | KClO3 | 5 580 |
| ② | KClO3、MnO2(质量比1:1) | 3 350 |
| ③ | KClO3、CuO(质量比1:1) | |
| ④ | KClO3、Fe2O3(质量比1:1) | 3 390 |
(1)由实验
(2)实验所用的三种金属氧化物比较,氧化铜催化效果仅次于二氧化锰,请你推出其分解温度(用t表示)的取值范围:
【交流反思】
(3)若要证明Fe2O3是该反应的催化剂,还要验证它在化学反应前后的
(4)影响氯酸钾分解快慢除催化剂种类外,你认为还可能有的影响因素是
您最近一年使用:0次
【推荐2】关于催化剂的研究是一项重要的课题,某化学兴趣小组开展了“探究催化剂的奥秘”项目式学习。
【任务一】认识催化剂
(1)催化剂在化工生产中起着重要作用,下列说法正确的是_____(填字母)。
【任务二】定量探究催化剂的催化效果
【提出问题】二氧化锰常作为氯酸钾分解制取氧气的催化剂,其他氧化物是否也能催化氯酸钾分解呢?
【查阅资料】研究表明,许多金属氧化物对氯酸钾的分解有催化作用。同学们分别用等量、颗粒大小相同的三种金属氧化物作催化剂进行实验,氯酸钾开始发生分解反应和反应剧烈时的温度如表所示:
(2)用氯酸钾制取氧气,若替代二氧化锰作催化剂,根据上表分析,最佳的金属氧化物应选择_____ 。
【设计并完成实验】
(3)实验一:将3.0g氯酸钾放在试管中加热;
实验二:将3.0g氯酸钾与1.0g二氧化锰混合均匀加热;
实验三:将xg氯酸钾与1.0g氧化铜混合均匀加热;
①请写出检验试管中生成氧气的方法:_____ 。
②通过实验二与实验三可以比较出不同催化剂对实验的影响,则实验三中x的值为_____ ,写出实验三反应的化学方程式:_____ 。
③对比实验_____ (填“一”或“二”)和实验三的不同现象,可证明氧化铜能加快氯酸钾的分解速率。
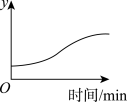
(4)加热一定量的氯酸钾和氧化铜的混合物,某变量y随时间的变化趋势如图所示。则纵坐标y表示的是_____(填字母)。
【实验结论】
(5)_____ 。
【任务一】认识催化剂
(1)催化剂在化工生产中起着重要作用,下列说法正确的是_____(填字母)。
| A.不加入催化剂化学反应就不能发生 |
| B.在过氧化氢溶液中加入二氧化锰,则生成氧气的质量将增加 |
| C.催化剂的化学性质在化学反应前后不发生改变 |
【任务二】定量探究催化剂的催化效果
【提出问题】二氧化锰常作为氯酸钾分解制取氧气的催化剂,其他氧化物是否也能催化氯酸钾分解呢?
【查阅资料】研究表明,许多金属氧化物对氯酸钾的分解有催化作用。同学们分别用等量、颗粒大小相同的三种金属氧化物作催化剂进行实验,氯酸钾开始发生分解反应和反应剧烈时的温度如表所示:
| 催化剂 | 氧化铁 | 氧化铝 | 氧化铜 |
| 开始反应/℃ | 420 | 515 | 305 |
| 剧烈反应/℃ | 490 | 540 | 350 |
(2)用氯酸钾制取氧气,若替代二氧化锰作催化剂,根据上表分析,最佳的金属氧化物应选择
【设计并完成实验】
(3)实验一:将3.0g氯酸钾放在试管中加热;
实验二:将3.0g氯酸钾与1.0g二氧化锰混合均匀加热;
实验三:将xg氯酸钾与1.0g氧化铜混合均匀加热;
①请写出检验试管中生成氧气的方法:
②通过实验二与实验三可以比较出不同催化剂对实验的影响,则实验三中x的值为
③对比实验
(4)加热一定量的氯酸钾和氧化铜的混合物,某变量y随时间的变化趋势如图所示。则纵坐标y表示的是_____(填字母)。

| A.固体中氧化铜的质量 |
| B.固体中氯酸钾的质量 |
| C.固体中氧化铜的质量分数 |
【实验结论】
(5)
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐3】实验室利用加热氯酸钾和二氧化锰混合物的方法来制取氧气,加热一段时间后,同学们制得了所需的氧气,此时,试管内剩余固体的成分是什么呢?同学们想继续探究:
【提出问题】试管内剩余固体的成分是什么?
(1)请写出该反应的文字(或符号)表达式____________________ 。
【猜想与假设】
(2)猜想一:氯化钾和二氧化锰
猜想二:氯酸钾和二氧化锰
猜想三:____________________ 。
【分析与思考】
(3)经分析,同学们一致认为猜想__________ 不成立。
【实验探究】
(4)请设计实验方案,通过观察到明显的实验现象证明猜想三正确,并完成表格:
【总结与提升】
(5)要想证明到底是哪一种猜想正确,只需要比较几种正确猜想的不同,确定需要__________ ,设计实验通过_________ 证明该物质是否存在即可。
【提出问题】试管内剩余固体的成分是什么?
(1)请写出该反应的文字(或符号)表达式
【猜想与假设】
(2)猜想一:氯化钾和二氧化锰
猜想二:氯酸钾和二氧化锰
猜想三:
【分析与思考】
(3)经分析,同学们一致认为猜想
【实验探究】
(4)请设计实验方案,通过观察到明显的实验现象证明猜想三正确,并完成表格:
实验操作 | 实验现象 | 实验结论 |
| 取少量剩余固体于试管中,继续 | 猜想三正确 |
【总结与提升】
(5)要想证明到底是哪一种猜想正确,只需要比较几种正确猜想的不同,确定需要
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐1】如图为实验室常见的装置。

(1)仪器①的名称:__________ 。
(2)某同学选用C、D装置组合制取CO2,化学方程式为______________ ,实验开始前,他关闭活塞,向长颈漏斗中倒水,观察到____________ 现象,说明该装置的气密性良好。
(3)同学们用高锰酸钾制取较为纯净的氧气,可选用的装置组合是__________ ,小明收集的气体纯度明显偏低,其原因可能是___________ (填字母序号)。
a 高锰酸钾中混入了二氧化锰
b 收集前,集气瓶中未装满水
c 收集后,集气瓶中仍留有水
d 未见气泡连续均匀冒出时就开始收集
(4)林同学称取一定质量的高锰酸钾制取氧气,将温度控制在250℃,实验结束时,林同学发现收集到的O2量大于理论产生的O2量,针对这一现象,同学们展开如下探究:
【提出猜想】依据质量守恒定律,提出猜想
猜想Ⅰ:反应生成的二氧化锰分解出O2
猜想Ⅱ:反应生成的锰酸钾分解出O2
【实验验证】同学们分为两组,分别进行以下实验:
①第一小组同学取一定质量的二氧化锰 ,在250℃条件下加热一段时间,冷却后测得二氧化锰的质量不变,由此他们得出的结论是________ 。
②第二小组同学也用同样的方法加热后,没有用测定质量的方法就验证了猜想Ⅱ正确,他们的实验操作是______ 。
(5)张同学查阅资料,得出信息:
①锰酸钾在较高温度下加热分解生成氧化钾、二氧化锰和氧气;
②锰酸钾受热只能部分分解,原因可能是生成的氧化钾对其分解产生影响。
对此,张同学设计了如下实验方案: 分别取等质量的锰酸钾固体于两支试管中,一支试管中加入氧化钾,另一支试管中不加氧化钾,分别加热,比较收集相同体积的气体所需的时间。该过程中还必须控制的变量是____ ,锰酸钾受热分解的化学方程式为_____ 。

(1)仪器①的名称:
(2)某同学选用C、D装置组合制取CO2,化学方程式为
(3)同学们用高锰酸钾制取较为纯净的氧气,可选用的装置组合是
a 高锰酸钾中混入了二氧化锰
b 收集前,集气瓶中未装满水
c 收集后,集气瓶中仍留有水
d 未见气泡连续均匀冒出时就开始收集
(4)林同学称取一定质量的高锰酸钾制取氧气,将温度控制在250℃,实验结束时,林同学发现收集到的O2量大于理论产生的O2量,针对这一现象,同学们展开如下探究:
【提出猜想】依据质量守恒定律,提出猜想
猜想Ⅰ:反应生成的二氧化锰分解出O2
猜想Ⅱ:反应生成的锰酸钾分解出O2
【实验验证】同学们分为两组,分别进行以下实验:
①第一小组同学取一定质量的二氧化锰 ,在250℃条件下加热一段时间,冷却后测得二氧化锰的质量不变,由此他们得出的结论是
②第二小组同学也用同样的方法加热后,没有用测定质量的方法就验证了猜想Ⅱ正确,他们的实验操作是
(5)张同学查阅资料,得出信息:
①锰酸钾在较高温度下加热分解生成氧化钾、二氧化锰和氧气;
②锰酸钾受热只能部分分解,原因可能是生成的氧化钾对其分解产生影响。
对此,张同学设计了如下实验方案: 分别取等质量的锰酸钾固体于两支试管中,一支试管中加入氧化钾,另一支试管中不加氧化钾,分别加热,比较收集相同体积的气体所需的时间。该过程中还必须控制的变量是
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐2】为了探究影响固体溶解性的因素,某同学设计了如下三组实验:
①观察三组实验,写出第二组实验中缺失的数据:_____ .
②分析上表,第一组实验研究的因素是_____ ;
由上述实验可知,影响固体溶解性的因素是_____ (填序号);
a.温度 b.加入溶剂种类 c.加入溶剂质量 d.加入固体种类 e.加入固体质量
③由实验组别中的_____ (填“第一组”、“第二组”或“第三组”)可知,20℃时固体A的溶解性_____ (填“>”、“﹦”或“<”)固体B的溶解性.
④根据上述实验,以下推论正确的是_____ (填序号).
Ⅰ 20℃时,B的溶解度为36g/100g水
Ⅱ 20℃时,A的饱和溶液的溶质质量分数为31%
Ⅲ 第三组实验中,80℃时A的溶液可能是饱和溶液
Ⅳ A的溶解性大于B的溶解性.
| 实验组别 | 第一组 | 第二组 | 第三组 | |||
| 实验温度 | 20℃ | 20℃ | 20℃ | 20℃ | 80℃ | 20℃ |
| 溶剂种类 | 水 | 酒精 | 水 | 水 | 水 | 水 |
| 溶剂质量 | 20g | 20g | 10g | 10g | 10g | 10g |
| 固体种类 | A | A | A | B | A | B |
| 加入固体质量 | 10g | 10g | 10g | 10g | 10g | 10g |
| 溶解固体质量 | 6.2g | 0g | —— | 3.6g | 10g | 3.6g |
①观察三组实验,写出第二组实验中缺失的数据:
②分析上表,第一组实验研究的因素是
由上述实验可知,影响固体溶解性的因素是
a.温度 b.加入溶剂种类 c.加入溶剂质量 d.加入固体种类 e.加入固体质量
③由实验组别中的
④根据上述实验,以下推论正确的是
Ⅰ 20℃时,B的溶解度为36g/100g水
Ⅱ 20℃时,A的饱和溶液的溶质质量分数为31%
Ⅲ 第三组实验中,80℃时A的溶液可能是饱和溶液
Ⅳ A的溶解性大于B的溶解性.
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐3】学习小组对蒸汽眼罩(结构成分为铁粉、活性炭、吸水树脂、食用盐水、无纺布、蛭石等)展开项目化学习,设计了以下项目任务:
【任务一】:证明蒸汽眼罩的粉末中含有铁粉
(1)小组同学将某品牌“蒸汽眼罩”内的粉末处理后,得到黑色粉末。用______ (填仪器名称)取少量黑色粉末置于试管中,加入稀盐酸,观察到有气泡产生,静置较长时间后溶液为浅绿色。该反应的化学方程式为______ 。
【任务二】:研究蒸汽眼罩打开后能迅速升温的原因
(2)小组同学查阅资料发现,蒸汽眼罩的热量来源于铁粉生锈,铁生锈是缓慢氧化,蒸汽眼罩内的粉末在使用后变为红棕色,其主要成分是______ (填化学式)。
(3)为研究铁粉生锈快慢的影响因素,小组同学设计了如下表所示的3组实验进行比对,请完善表格中的实验内容。
实验中,温度随时间变化的图像如图所示,从图像可以看出:______ (填名称)和______ (填名称)共同作用加快了铁生锈,短时间内迅速升温,使吸水树脂中的水分蒸发为水蒸气。

【任务三】:比较自制、市售蒸汽眼罩的发热差异
(4)取7g铁粉和2.5g活性炭于无纺布袋中,滴加15滴蒸馏水和10滴溶质质量分数为20%的浓盐水,混合均匀制得自制蒸汽眼罩,测得自制及市售蒸汽眼罩发热情况如图所示。市售蒸汽眼罩能持续放热并保温的原因是______ 和______ 。

【任务一】:证明蒸汽眼罩的粉末中含有铁粉
(1)小组同学将某品牌“蒸汽眼罩”内的粉末处理后,得到黑色粉末。用
【任务二】:研究蒸汽眼罩打开后能迅速升温的原因
(2)小组同学查阅资料发现,蒸汽眼罩的热量来源于铁粉生锈,铁生锈是缓慢氧化,蒸汽眼罩内的粉末在使用后变为红棕色,其主要成分是
(3)为研究铁粉生锈快慢的影响因素,小组同学设计了如下表所示的3组实验进行比对,请完善表格中的实验内容。
| 实验 | 药品 |
| 实验1 | 4g铁粉、2mL水、2g氯化钠 |
| 实验2 | |
| 实验3 | 4g铁粉、2mL水、 |

【任务三】:比较自制、市售蒸汽眼罩的发热差异
(4)取7g铁粉和2.5g活性炭于无纺布袋中,滴加15滴蒸馏水和10滴溶质质量分数为20%的浓盐水,混合均匀制得自制蒸汽眼罩,测得自制及市售蒸汽眼罩发热情况如图所示。市售蒸汽眼罩能持续放热并保温的原因是

您最近一年使用:0次
科学探究题
|
适中
(0.65)
名校
解题方法
【推荐1】1.小红欲通过实验证明“二氧化锰是过氧化氢分解的催化剂”这一命题。她设计并完成了下表所示的探究实验:
实验一:取5%的过氧化氢溶液于试管中,伸入带火星的木条,有气泡产生,木条不复燃;
实验二:向盛水的试管中加入二氧化锰,伸入带火星木条,无气泡产生;
实验三:________________ ,伸入带火星的木条,有大量气泡产生,木条复燃。
结论:二氧化锰是过氧化氢分解的催化剂。
(1)请你帮小红同学填写实验三的操作_______________ ;
(2)实验二的目的是____________________ ;
(3)小张同学认为仅有上述实验还不能完全得出结论,理由是_________ 。
(4)小伟通过查资料发现过氧化氢分解除了用二氧化锰外,还有氧化铜(CuO)等物质做催化剂。
【提出问题】氧化铜是否比二氧化锰的催化效果更好?影响氯酸钾分解速率的因素有哪些呢?
【设计实验】以生成等体积的氧气为标准,设计了下列机组实验(其他可能影响实验的因素均忽略)。
①若t1__________ t2(填“大于”“等于”“小于”),说明氧化铜能加快氯酸钾的分解速率。
②比较氧化铜和二氧化锰催化效果的实验组是________________ ;
③写出实验二中涉及反应的符号表达式_______________ ;
④将实验三和实验四对比,可得出化学反应快慢与温度的关系,那么实验四中控制MnO2的质量应为________ g,若t3>t4,则化学反应快慢与温度的关系是______ 。
实验一:取5%的过氧化氢溶液于试管中,伸入带火星的木条,有气泡产生,木条不复燃;
实验二:向盛水的试管中加入二氧化锰,伸入带火星木条,无气泡产生;
实验三:
结论:二氧化锰是过氧化氢分解的催化剂。
(1)请你帮小红同学填写实验三的操作
(2)实验二的目的是
(3)小张同学认为仅有上述实验还不能完全得出结论,理由是
(4)小伟通过查资料发现过氧化氢分解除了用二氧化锰外,还有氧化铜(CuO)等物质做催化剂。
【提出问题】氧化铜是否比二氧化锰的催化效果更好?影响氯酸钾分解速率的因素有哪些呢?
【设计实验】以生成等体积的氧气为标准,设计了下列机组实验(其他可能影响实验的因素均忽略)。
| 实验序号 | KClO3的质量 | 其他物质的质量 | 温度 | 氧气的体积 | 反应所需时间 |
| 一 | 2.0g | / | 3300C | 100mL | t1 |
| 二 | 2.0g | CuO 0.5g | 3300C | 100mL | t2 |
| 三 | 2.0g | MnO2 0.5g | 3300C | 100mL | t3 |
| 四 | 2.0g | MnO2 | 3800C | 100mL | t4 |
①若t1
②比较氧化铜和二氧化锰催化效果的实验组是
③写出实验二中涉及反应的符号表达式
④将实验三和实验四对比,可得出化学反应快慢与温度的关系,那么实验四中控制MnO2的质量应为
您最近一年使用:0次
科学探究题
|
适中
(0.65)
名校
解题方法
【推荐2】根据下列实验装置图,回答问题:

(1)实验仪器的名称:a_______________ ;b_________________ 。
(2)实验室用高锰酸钾制取氧气的化学表达式为:_____________________________ ,发生装置应该选用________ ,该装置有一处不足,请改正:______________________________ 。
(3)在收集氧气的方法也可采用_____________ (填“向上”或“向下”)排空气法。若用下图所示装置采用“排空气法”收集氧气,请在图中将导管补画完整 。

___________________________
(4)已知在常温下,一氧化氮是一种难溶于水的气体,密度比空气略大,与空气中的氧气迅速反应生成二氧化氮。若要收集一瓶一氧化氮,应选用下列收集方法中的_______________ ;

(5) 包包同学称取一定质量的KMnO4固体放入大试管中,将温度控制在250℃加热制取O2。实验结束时,宇宇同学发现用排水法收集到的O2大于理论产量。针对这一现象,包包和宇宇同学进行了如下探究:
【提出猜想】猜想I:反应生成的MnO2分解放出O2;
猜想II:反应生成的K2MnO4分解放出O2;
猜想III:反应生成的K2MnO4和MnO2分解都放出O2。
【实验验证】包包和宇宇分成两组,分别进行下列实验:
包包同学取一定质量的MnO2,在250℃条件下加热一段时间,冷却后测得MnO2的质量不变,则猜想_____ 错误;
宇宇同学取K2MnO4在250℃条件下加热,没有用测定质量的方法得出了猜想II正确的结论。宇宇同学选择的实验方法是_______________________________________________ 。

(1)实验仪器的名称:a
(2)实验室用高锰酸钾制取氧气的化学表达式为:
(3)在收集氧气的方法也可采用

(4)已知在常温下,一氧化氮是一种难溶于水的气体,密度比空气略大,与空气中的氧气迅速反应生成二氧化氮。若要收集一瓶一氧化氮,应选用下列收集方法中的

(5) 包包同学称取一定质量的KMnO4固体放入大试管中,将温度控制在250℃加热制取O2。实验结束时,宇宇同学发现用排水法收集到的O2大于理论产量。针对这一现象,包包和宇宇同学进行了如下探究:
【提出猜想】猜想I:反应生成的MnO2分解放出O2;
猜想II:反应生成的K2MnO4分解放出O2;
猜想III:反应生成的K2MnO4和MnO2分解都放出O2。
【实验验证】包包和宇宇分成两组,分别进行下列实验:
包包同学取一定质量的MnO2,在250℃条件下加热一段时间,冷却后测得MnO2的质量不变,则猜想
宇宇同学取K2MnO4在250℃条件下加热,没有用测定质量的方法得出了猜想II正确的结论。宇宇同学选择的实验方法是
您最近一年使用:0次
【推荐3】我国科学家首次在实验室实现了二氧化碳到淀粉的从头合成,使淀粉生产从传统农业种植模式向工业车间生产模式变为可能,也为推进“碳达峰”和“碳中和”目标实现的技术路线提供一种新思路。某兴趣小组对淀粉展开了探究。
【查阅资料】淀粉能作过氧化氢分解的催化剂。
【实验1】利用如图所示装置对比淀粉与二氧化锰对过氧化氢分解的催化效果。

(1)连接装置的接口顺序是a→______ (填字母编号)。
实验数据记录如下表所示:
(2)实验②中发生反应的化学方程式为______ 。
(3)若得出二氧化锰的催化效果比淀粉好,则得到此结论的实验证据应该是______ 。
(4)比较实验①和实验③的目的是______ 。
【实验2】
(5)取少量淀粉在硬质玻璃管中隔绝空气加强热,观察到玻璃管内出现水雾,说明淀粉中含有______ (填元素名称)。
(6)实验结束后观察到试管中残留有黑色固体,小组同学猜测该黑色固体是碳单质,于是进行下列实验进行验证。
【实验拓展】
(7)淀粉在一定条件下会发生爆炸。为了避免发生粉尘爆炸事故,生产淀粉的过程中采取的措施可行的是______(填字母代号)
【查阅资料】淀粉能作过氧化氢分解的催化剂。
【实验1】利用如图所示装置对比淀粉与二氧化锰对过氧化氢分解的催化效果。

(1)连接装置的接口顺序是a→
实验数据记录如下表所示:
实验 | 5%过氧化氢溶液的体积/mL | 催化剂种类及质量 | 收集10mL气体所需时间/s |
① | 40 | 淀粉0.5g |
|
② | 40 | 二氧化锰0.5g |
|
③ | 40 | 淀粉2g |
|
(3)若得出二氧化锰的催化效果比淀粉好,则得到此结论的实验证据应该是
(4)比较实验①和实验③的目的是
【实验2】
(5)取少量淀粉在硬质玻璃管中隔绝空气加强热,观察到玻璃管内出现水雾,说明淀粉中含有
(6)实验结束后观察到试管中残留有黑色固体,小组同学猜测该黑色固体是碳单质,于是进行下列实验进行验证。
实验步骤 | 实验现象 | 实验结论 |
①取少量黑色固体于燃烧匙内,加热至红热, 放入盛有氧气的集气瓶中;②向集气瓶中倒入 适量澄清石灰水 | ①黑色固体剧烈燃烧, 发出白光; ② | 该黑色固体 是碳单质 |
【实验拓展】
(7)淀粉在一定条件下会发生爆炸。为了避免发生粉尘爆炸事故,生产淀粉的过程中采取的措施可行的是______(填字母代号)
| A.密封门窗,隔绝氧气 | B.严谨吸烟,杜绝火源 |
| C.轻拿轻放,减少粉尘飞扬 | D.提高淀粉的着火点 |
您最近一年使用:0次