广泛存在的“金属”与我们的各行各业,日常生活以及学习有着密切的关系。
请回答下列问题
(1)人体中缺少某些元素,会影响健康,甚至引起疾病。丁丁小朋友比同龄的孩子矮小很多,你认为他的体内可能缺少的元素名称是________________________________ 。
(2)镁带能在空气中燃烧,可用于做照明弹的原因是___________________________________ 。
(3)铝粉又称“银粉”,涂在铸铁暖气片上的作用是_____________________________________ 。
(4)铜在空气中生锈变成“铜锈”,化学式为Cu2(OH)2CO3,结合你的所学推测铜生锈过程中一定参与反应的其他物质有_______________________________________ 。
(5)熄灭蜡烛有很多方法,归纳起来有A._____________________________ ,B.移开可燃物C. ______________________________ ,当当同学将石棉网放在蜡烛火焰上方移动,火焰熄灭。因为铁具有 _________________________________ 。
(6)使金属矿物变成金属的过程叫做金属的冶炼,高炉炼铁的主要反应过程如下。
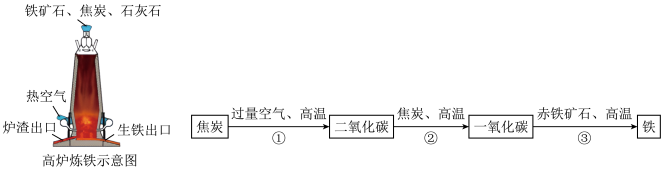
图中标号①的基本反应类型_________________________________ 。
图中标号②的化学方程式为_________________________________ 。
经过③的化学反应过程,若用500t含氧化铁为80%的赤铁矿作原料,可得含杂质3%生铁的质量______________________________ 。
请回答下列问题
(1)人体中缺少某些元素,会影响健康,甚至引起疾病。丁丁小朋友比同龄的孩子矮小很多,你认为他的体内可能缺少的元素名称是
(2)镁带能在空气中燃烧,可用于做照明弹的原因是
(3)铝粉又称“银粉”,涂在铸铁暖气片上的作用是
(4)铜在空气中生锈变成“铜锈”,化学式为Cu2(OH)2CO3,结合你的所学推测铜生锈过程中一定参与反应的其他物质有
(5)熄灭蜡烛有很多方法,归纳起来有A.
(6)使金属矿物变成金属的过程叫做金属的冶炼,高炉炼铁的主要反应过程如下。

图中标号①的基本反应类型
图中标号②的化学方程式为
经过③的化学反应过程,若用500t含氧化铁为80%的赤铁矿作原料,可得含杂质3%生铁的质量
更新时间:2019-03-12 20:53:28
|
相似题推荐
综合应用题
|
适中
(0.65)
名校
【推荐1】硫酸铜是制备铜化合物的重要原料,农业上用于配制波尔多液,作杀菌剂。硫酸铜和氧气、二氧化碳、铁、稀硫酸、氢氧化钠之间的关系如图甲所示(“一”表示物质之间能反应,“→”表示物质之间的转化关系),③④发生置换反应。回答下列问题:

(1)B的化学式是_____ 。
(2)④的化学方程式是_____ 。
(3)若⑤发生中和反应,则反应的化学方程式是_____ 。
(4)其它物质不变,CuSO4换为下列物质中的_____ (填序号)时,也有图中的关系。
①氧化铜 ②盐酸 ③氢氧化钙 ④硫酸镁
(5)用表面附着有铜绿的久置铜片制取硫酸铜实验流程如图乙所示【铜绿化学式为Cu2(OH)2CO3,能与稀硫酸反应产生硫酸铜、水和二氧化碳,加热时产生氧化铜、水和二氧化碳】

铜与空气中的_____ 、O2反应产生铜绿;固体A的化学式是_____ ;同一久置铜片通过方法一和方法二得到的硫酸铜的质量;方法一:_____ (选填“大于”“等于”或“小于”)方法二:方法一除不产生污染物外,还具有的优点是_____ (答一点)。

(1)B的化学式是
(2)④的化学方程式是
(3)若⑤发生中和反应,则反应的化学方程式是
(4)其它物质不变,CuSO4换为下列物质中的
①氧化铜 ②盐酸 ③氢氧化钙 ④硫酸镁
(5)用表面附着有铜绿的久置铜片制取硫酸铜实验流程如图乙所示【铜绿化学式为Cu2(OH)2CO3,能与稀硫酸反应产生硫酸铜、水和二氧化碳,加热时产生氧化铜、水和二氧化碳】

铜与空气中的
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐2】2020年6月23日,长征三号乙运载火箭将北斗三号最后一颗组网卫星成功送入预定轨道,我国北斗导航地位将进一步提升。从化学视角回答下列问题:
(1)卫星制造使用了黄金、钛合金,其中用作天线的是______ 。使用黄金制作卫星的电子元件,利用了金的什么化学性质?______ 填序号。
A.光泽好 B.耐磨、易加工 C.容易导电 D.很难被氧化
(2)卫星的太阳能电池帆板用先进的砷化镓主板和铝合金边框制成,砷(As)原子的结构示意图如图,其中X=______ 。铝合金比纯铝具有的优势是______ (写出1条即可)。

(3)运载火箭用偏二甲肼(C2H8N2)作燃料,N2O4作氧化剂。火箭发射时,燃料与氧化剂剧烈反应放出大量的热,并生成对空气无污染的两种氧化物和一种单质,这种单质的化学式为______ ,两种氧化物中相对分子质量较大的是______ 。
(1)卫星制造使用了黄金、钛合金,其中用作天线的是
A.光泽好 B.耐磨、易加工 C.容易导电 D.很难被氧化
(2)卫星的太阳能电池帆板用先进的砷化镓主板和铝合金边框制成,砷(As)原子的结构示意图如图,其中X=

(3)运载火箭用偏二甲肼(C2H8N2)作燃料,N2O4作氧化剂。火箭发射时,燃料与氧化剂剧烈反应放出大量的热,并生成对空气无污染的两种氧化物和一种单质,这种单质的化学式为
您最近一年使用:0次
【推荐3】氢能是一种极具发展潜力的清洁能源。
I.甲烷热解制氢
高温时,以熔融金属锡(Sn)为液态传热介质,细小的甲烷气泡从鼓泡反应器底部注入并发生分解,得到固体石墨。反应原理示意图如图所示。
已知:物质的部分性质
_______________ 。
(2)该反应温度T3与金属锡的熔点T1、沸点T2三者之间的大小关系为_______________ 。
(3)该方法可避免石墨在介质中大量附着,主要原因是_______________ 。
II.海水电解制氢
海水无淡化直接电解制氢的原理和装置如图所示。PTFE膜两侧有水蒸气压力差,使膜外侧的水转化为水蒸气,水蒸气通过PTFE膜后液化。液态水和高分子均不能直接通过PTFE膜。_______________ 。
(5)在电解过程中,PTFE膜内侧KOH溶液的溶质质量分数保持不变,原因是____________ 。
Ⅲ.热化学循环制氢
一种循环利用Zn/ZnO制氢的原理如下。
反应l:
反应2:
(6)理论上产生氢气与氧气的质量比为_______________ 。
(7)已知ZnO在2000℃左右充分分解,但反应1分离得到的Zn很少,若往装置中充入氩气,制得到的Zn明显增加。可能的原因是_______________ 。
I.甲烷热解制氢
高温时,以熔融金属锡(Sn)为液态传热介质,细小的甲烷气泡从鼓泡反应器底部注入并发生分解,得到固体石墨。反应原理示意图如图所示。
已知:物质的部分性质
| 液态锡 | 石墨 | |
| 密度g/cm3 | 7.0 | 2.2 |
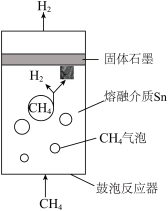
(2)该反应温度T3与金属锡的熔点T1、沸点T2三者之间的大小关系为
(3)该方法可避免石墨在介质中大量附着,主要原因是
II.海水电解制氢
海水无淡化直接电解制氢的原理和装置如图所示。PTFE膜两侧有水蒸气压力差,使膜外侧的水转化为水蒸气,水蒸气通过PTFE膜后液化。液态水和高分子均不能直接通过PTFE膜。
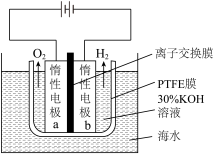
(5)在电解过程中,PTFE膜内侧KOH溶液的溶质质量分数保持不变,原因是
Ⅲ.热化学循环制氢
一种循环利用Zn/ZnO制氢的原理如下。
反应l:

反应2:

(6)理论上产生氢气与氧气的质量比为
(7)已知ZnO在2000℃左右充分分解,但反应1分离得到的Zn很少,若往装置中充入氩气,制得到的Zn明显增加。可能的原因是
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐1】化学是以实验为基础的科学,实验是科学探究的重要手段,化学兴趣小组利用下图装置制取CO2并进行相关的系列实验。二氧化碳在饱和碳酸氢钠溶液中的溶解度更小。

(1)如果让装置A能控制反应的发生和停止,请指出装置A需要怎样调整______ 。
(2)装置C的作用是______ 。
(3)装置D中发生反应的化学方程式为______ 。
(4)装置E中观察到的现象是______ ,发生反应的化学方程式为______ 。
(5)尾气CO可用装置G收集,利用了CO的性质有______ 。
(6)F中发生反应的化学方程式为______ 。
(7)兴趣小组的同学将足量的大理石加入200g一定质量分数的稀盐酸中,充分反应(杂质不参加反应),反应结束后得知混合物质量减轻22g(不考虑氯化氢和水蒸气的挥发),求该盐酸的质量分数______ 。

(1)如果让装置A能控制反应的发生和停止,请指出装置A需要怎样调整
(2)装置C的作用是
(3)装置D中发生反应的化学方程式为
(4)装置E中观察到的现象是
(5)尾气CO可用装置G收集,利用了CO的性质有
(6)F中发生反应的化学方程式为
(7)兴趣小组的同学将足量的大理石加入200g一定质量分数的稀盐酸中,充分反应(杂质不参加反应),反应结束后得知混合物质量减轻22g(不考虑氯化氢和水蒸气的挥发),求该盐酸的质量分数
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐2】兴趣小组用以下装置模拟炼铁原理。(B 中的NaOH 溶液可吸收二氧化碳)
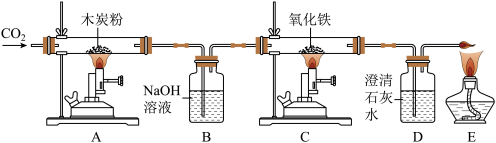
(1)A 装置玻璃管中反应的化学方程式为____________ ,该反应属于____________ 反应(填“放热”或“吸热”)。
(2)C 装置玻璃管中的现象为___________ 。
(3)D 装置中反应的化学反应方程式为____________ 。
(4)E 装置的作用是__________ 。
(5)如果C 装置中氧化铁质量为 8g,完全反应后剩余固体质量是多少____________ 。(利用化学方程式进行计算,写出计算过程)

(1)A 装置玻璃管中反应的化学方程式为
(2)C 装置玻璃管中的现象为
(3)D 装置中反应的化学反应方程式为
(4)E 装置的作用是
(5)如果C 装置中氧化铁质量为 8g,完全反应后剩余固体质量是多少
您最近一年使用:0次
【推荐3】金属可用于制造货币、合金结构钢、氢化催化剂等。粗制氧化镍主要含氧化镍(NiO),以及少量氧化钻(CoO)和氧化铁,以粗制氧化镍为原料制备纯镍的流程如下:
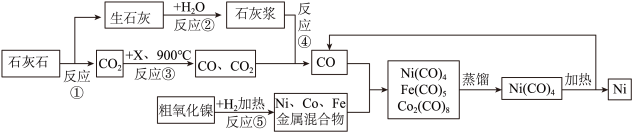
(1)反应③中,黑色单质 X 发生了___________ 反应(填“氧化”或者“还原”) 。
(2)反应②中生石灰在生活中的用途是___________ 。
(3)反应⑤开始前用氮气充分吹扫设备内部,其目的是___________ ,该反应中氧化镍转化为金属镍的化学方程式是___________ 。
(4)查阅资料,获知部分物质的沸点:
从Ni(CO)4、Fe(CO)5和 Co2(CO)8的混合物中用蒸馏的方法提Ni(CO)4应选择的温度(T)范围是_______
(5)以上生产流程中循环使用的物质是_________ (填化学式)
(6)若将制得的 Ni 放入 FeSO4 溶液中,没有观察到明显现象,证明 Ni 的金属活动性比Fe___________ (选填“强”或“弱”)。
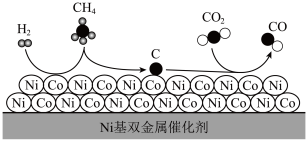
(7)科学家开发出了镍钴双金属基催化剂;用其来催化 CH4和 CO2制取合成气,反应过程如图,有关说法正确的是___________。(填字母)

(1)反应③中,黑色单质 X 发生了
(2)反应②中生石灰在生活中的用途是
(3)反应⑤开始前用氮气充分吹扫设备内部,其目的是
(4)查阅资料,获知部分物质的沸点:
| 物质 | Ni(CO)4 | Fe(CO)5 | Co2(CO)8 |
| 沸点/℃ | 43 | 106 | 52 |
(5)以上生产流程中循环使用的物质是
(6)若将制得的 Ni 放入 FeSO4 溶液中,没有观察到明显现象,证明 Ni 的金属活动性比Fe
(7)科学家开发出了镍钴双金属基催化剂;用其来催化 CH4和 CO2制取合成气,反应过程如图,有关说法正确的是___________。(填字母)

| A.Ni 基双金属催化剂在应前后质量和化学性质都没有改变,可重复使用 |
| B.该反应的最终生成物是氢气和一氧化碳 |
| C.反应前后各元素的化合价均未改变 |
您最近一年使用:0次
【推荐1】金属是人类生活中的常用的材料。
(1)金属元素在自然界中分布很广,地壳中含量最多的金属元素是______ 。
(2)还原铁粉常用作食品干燥剂,又称“双吸剂”。它能够吸收空气中的______ 。
(3)在实验室中,金属及其化合物可用于制备常见的气体,下图为制备气体的几种装置。
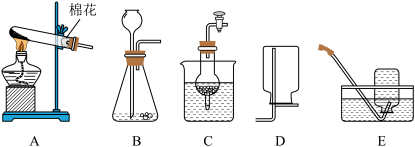
①实验室用高锰酸钾制取氧气应选择的装置组合是______ (填字母)。
②在浓硫酸作催化剂的条件下,加热甲酸(HCOOH)能够制取一氧化碳,同时生成水,反应的化学方程式为______ ,利用E装置收集一氧化碳的理由是______ 。
(4)在实验室中,老师用下面所示的装置进行实验(图中固定试管的仪器已略去):加热一段时间后,观察到木炭粉的质量明显减少;氧化铜粉处出现了一层红亮的物质;澄清石灰水变浑浊。停止加热并冷却到室温。
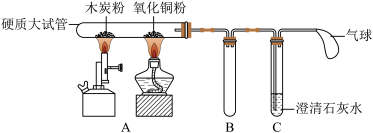
①B装置的作用是______ 。
②实验后要从硬质大试管的剩余固体中回收金属铜,写出操作步骤______ (要求过程中要用到“湿法冶金”的原理)。
(5)某钢铁厂采用赤铁矿(主要成分为Fe2O3)炼铁,日产含铁2.1×104t的生铁,至少需要含Fe2O375%的赤铁矿的质量是多少?
(1)金属元素在自然界中分布很广,地壳中含量最多的金属元素是
(2)还原铁粉常用作食品干燥剂,又称“双吸剂”。它能够吸收空气中的
(3)在实验室中,金属及其化合物可用于制备常见的气体,下图为制备气体的几种装置。

①实验室用高锰酸钾制取氧气应选择的装置组合是
②在浓硫酸作催化剂的条件下,加热甲酸(HCOOH)能够制取一氧化碳,同时生成水,反应的化学方程式为
(4)在实验室中,老师用下面所示的装置进行实验(图中固定试管的仪器已略去):加热一段时间后,观察到木炭粉的质量明显减少;氧化铜粉处出现了一层红亮的物质;澄清石灰水变浑浊。停止加热并冷却到室温。

①B装置的作用是
②实验后要从硬质大试管的剩余固体中回收金属铜,写出操作步骤
(5)某钢铁厂采用赤铁矿(主要成分为Fe2O3)炼铁,日产含铁2.1×104t的生铁,至少需要含Fe2O375%的赤铁矿的质量是多少?
您最近一年使用:0次
综合应用题
|
适中
(0.65)
【推荐2】现代社会能源得到了不断开发和利用,合理安全使用能源很重要。
(1)下列物质中①煤②石油③天然气③乙醇,其中属于化石燃料的是(填序号)_____
(2)当房屋起火时,消防员用高压水枪将火扑灭,其中水在灭火过程中的主要作用为_____ 。
(3)石油炼制的产品之一是汽油。在汽油中加入适量乙醇作为汽车燃料,可适当节省石油资源。请写出乙醇在空气中完全燃烧的化学方程式_____ 。
(4)人类的生产生活离不开金属。在地壳里含量居第一位的金属元素是_____ 。下列三种金属被发现和使用的先后顺序为:铜、铁、铝。你认为金属大规模被使用的先后顺序跟_____ (填字母)关系最大。
A 地壳中金属元素的含量 B 金属的导电性 C 金属的化学活动性
(5)将CO气体通入盛有10g 的试管中,加热一段时间后,停止加热。继续通入CO至试管冷却,测得试管内剩余固体的质量为7.6g,则剩余固体中铁单质的质量为
的试管中,加热一段时间后,停止加热。继续通入CO至试管冷却,测得试管内剩余固体的质量为7.6g,则剩余固体中铁单质的质量为_____ 。
(1)下列物质中①煤②石油③天然气③乙醇,其中属于化石燃料的是(填序号)
(2)当房屋起火时,消防员用高压水枪将火扑灭,其中水在灭火过程中的主要作用为
(3)石油炼制的产品之一是汽油。在汽油中加入适量乙醇作为汽车燃料,可适当节省石油资源。请写出乙醇在空气中完全燃烧的化学方程式
(4)人类的生产生活离不开金属。在地壳里含量居第一位的金属元素是
A 地壳中金属元素的含量 B 金属的导电性 C 金属的化学活动性
(5)将CO气体通入盛有10g
 的试管中,加热一段时间后,停止加热。继续通入CO至试管冷却,测得试管内剩余固体的质量为7.6g,则剩余固体中铁单质的质量为
的试管中,加热一段时间后,停止加热。继续通入CO至试管冷却,测得试管内剩余固体的质量为7.6g,则剩余固体中铁单质的质量为
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐3】金属材料在生产、生活中有广泛的应用,人类的生产和生活都离不开金属。
(一)铁的应用和防护
(1)常州地铁的轨道主要材料是铁合金制作的,其硬度比纯铁_______ 。
(2)为防止铁生锈,通常会对铁制品进行“烤蓝”处理,烤蓝是用化学方法在铁表面生成层致密的四氧化三铁(Fe3O4)保护膜。烤蓝的原理是:在高温下,铁与水发生反应,生成四氧化三铁和一种单质气体,写出该反应的化学反应方程式:_______ 。
(二)铁的冶炼
我国劳动人民在春秋战国时期就会冶铁炼钢,实验室模拟炼铁实验装置如下图所示。

(3)实验时,应先注水片刻后再加热的目的是_______ 。
(4)实验过程中,硬质玻璃管中发生的化学方程式为_______ 。
(5)有同学提出黑色粉末中还可能含有Fe3O4。已知:Fe3O4能溶于稀H2SO4,且有Fe3+生成;Fe3+遇到硫氰化钾溶液显血红色。为证明黑色粉末成分,该同学取少量样品于烧杯中,加过量稀H2SO4,充分反应后,滴加少量硫氰化钾,证明黑色粉末中含有Fe和Fe3O4的现象是_______ 。
(6)若取16g氧化铁粉末进行实验,反应一段时间后,经检测剩余黑色固体成分是Fe和 ,称量固体的质量为X,则X的范围为
,称量固体的质量为X,则X的范围为_______ 。
(一)铁的应用和防护
(1)常州地铁的轨道主要材料是铁合金制作的,其硬度比纯铁
(2)为防止铁生锈,通常会对铁制品进行“烤蓝”处理,烤蓝是用化学方法在铁表面生成层致密的四氧化三铁(Fe3O4)保护膜。烤蓝的原理是:在高温下,铁与水发生反应,生成四氧化三铁和一种单质气体,写出该反应的化学反应方程式:
(二)铁的冶炼
我国劳动人民在春秋战国时期就会冶铁炼钢,实验室模拟炼铁实验装置如下图所示。

(3)实验时,应先注水片刻后再加热的目的是
(4)实验过程中,硬质玻璃管中发生的化学方程式为
(5)有同学提出黑色粉末中还可能含有Fe3O4。已知:Fe3O4能溶于稀H2SO4,且有Fe3+生成;Fe3+遇到硫氰化钾溶液显血红色。为证明黑色粉末成分,该同学取少量样品于烧杯中,加过量稀H2SO4,充分反应后,滴加少量硫氰化钾,证明黑色粉末中含有Fe和Fe3O4的现象是
(6)若取16g氧化铁粉末进行实验,反应一段时间后,经检测剩余黑色固体成分是Fe和
 ,称量固体的质量为X,则X的范围为
,称量固体的质量为X,则X的范围为
您最近一年使用:0次
综合应用题
|
适中
(0.65)
【推荐1】某初中化学社团------“拉瓦锡实验室”的活动丰富多彩。下面是它们以“化学与社会发展”为主题的两次活动记录:
活动1:在观看了“西气东输”与“石油分馏”等视频后,通过小组讨论,同学们认识到:
①煤、石油、天然气是人类社会重要的自然资源。天然气的主要成分是_______ 。(填化学式)
②现在化石燃料等不可再生能源面临枯竭,化石燃料对环境的影响也不容忽视。所以开发和利用风能、________ 等新能源成为越来越迫切的要求。
③人们将化石燃料通过化学工艺可制造和合成价值更高的药物、化学纤维、塑料盒合成橡胶等。其中塑料属于_____________ 材料,随意丢弃会造成“白色污染”。
活动2:同学们展示了各自收集到的有关“化学物质与健康”的相关资料及一些常见食品,如:高钙牛奶、加点食盐等。并针对“化学制品对人体有益有害”展开了激烈的辩论,从而认识到钙、铁、锌等元素对人体健康有重要作用,如缺铁元素会引起缺铁性贫血,缺钙元素会引起_________________ ;还认识到一氧化碳、甲醛等物质对人体健康的危害。 通过这样的社团活动,大家形成了“保护自然,关爱生命”的共识。
活动1:在观看了“西气东输”与“石油分馏”等视频后,通过小组讨论,同学们认识到:
①煤、石油、天然气是人类社会重要的自然资源。天然气的主要成分是
②现在化石燃料等不可再生能源面临枯竭,化石燃料对环境的影响也不容忽视。所以开发和利用风能、
③人们将化石燃料通过化学工艺可制造和合成价值更高的药物、化学纤维、塑料盒合成橡胶等。其中塑料属于
活动2:同学们展示了各自收集到的有关“化学物质与健康”的相关资料及一些常见食品,如:高钙牛奶、加点食盐等。并针对“化学制品对人体有益有害”展开了激烈的辩论,从而认识到钙、铁、锌等元素对人体健康有重要作用,如缺铁元素会引起缺铁性贫血,缺钙元素会引起
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐2】以化合价为纵坐标、物质类别为横坐标所绘制的图象叫二维价类图,价类图可有效帮助我们建立物质之间的联系,高效进行化学学习。下图所示为碳的价类图

(1)常见的碳单质有金刚石、石墨和C60等,其中常用作电池电极的是_______ (填“金刚石”或“石墨”)。它们的化学性质相似,都具有可燃性,写出C60在空气中完全燃烧的化学方程式_______ ,从热效应的角度分析,该反应___ 热量(填“吸收”或“释放”)。
(2)由图可知,M物质是氧化物,其保持M物质化学性质的最小微粒是______ (填名称),实验室常用_____ (填试剂的名称)检验M物质,实验室制备M物质的化学方程式是______ 。
(3)将CO2通入紫色石蕊试液,溶液变为_______ 色,该实验说明_______ 。
(4)碳酸钙由Ca2+和______ (填符号)构成,碳酸钙中氧元素的质量分数为_______ 。石灰石是生产建筑材料生石灰的原料,该生产的原理(用化学方程式表示)________ 。
(5)钙_______ (填“是”或“不是”)人体所需的微量元素,儿童缺钙易得______ (填字母)。
a侏儒症 b佝偻病 c贫血病 d白内障

(1)常见的碳单质有金刚石、石墨和C60等,其中常用作电池电极的是
(2)由图可知,M物质是氧化物,其保持M物质化学性质的最小微粒是
(3)将CO2通入紫色石蕊试液,溶液变为
(4)碳酸钙由Ca2+和
(5)钙
a侏儒症 b佝偻病 c贫血病 d白内障
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐3】铁是现代化学工业的基础,人类进步所必不可少的金属材料。
(1)看图1回答,铁元素为______ 元素(填“金属或非金属”)。
(2)健康人体内,总量4~5g的铁元素主要以化合物形式存在,缺铁会患______ (填字母)。
a.骨质疏松 b.甲状腺疾病 c.贫血症 d.侏儒症
【实验一】兴趣小组通过图2实验研究铁的冶炼
(3)该装置有一明显不当之处,你的改进方案是______ 。
(4)试写出一氧化碳和氧化铁在高温下生成铁的化学反应方程式______ 。
(5)实验一段时间后,观察到B处澄清石灰水变______ ,A处红棕色固体变为黑色,小明将所得的黑色固体物质放入足量的稀盐酸中,发现有少量气泡。写出反应的化学方程式______ 。
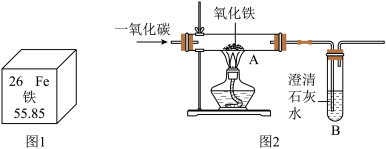
【资料1】已知铁的氧化物均能逐步失去其中的氧,最终被还原为铁。

【资料2】实验研究表明:该实验得到是四氧化三铁与铁粉的混合物。同时实验说明温度对CO和Fe2O3反应有影响。
【实验二】兴趣小组继续用图3实验研究一氧化碳和四氧化三铁的反应
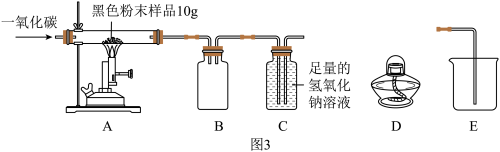
【资料3】氢氧化钠溶液可以与二氧化碳反应,吸收二氧化碳。
(6)从安全与规范的角度考虑,装置C后面应连接______ (选填装置序号)。
(7)四氧化三铁的质量为2.32g,充分反应。请计算产生单质铁的质量。(写出解题过程)
(1)看图1回答,铁元素为
(2)健康人体内,总量4~5g的铁元素主要以化合物形式存在,缺铁会患
a.骨质疏松 b.甲状腺疾病 c.贫血症 d.侏儒症
【实验一】兴趣小组通过图2实验研究铁的冶炼
(3)该装置有一明显不当之处,你的改进方案是
(4)试写出一氧化碳和氧化铁在高温下生成铁的化学反应方程式
(5)实验一段时间后,观察到B处澄清石灰水变

【资料1】已知铁的氧化物均能逐步失去其中的氧,最终被还原为铁。

【资料2】实验研究表明:该实验得到是四氧化三铁与铁粉的混合物。同时实验说明温度对CO和Fe2O3反应有影响。
【实验二】兴趣小组继续用图3实验研究一氧化碳和四氧化三铁的反应

【资料3】氢氧化钠溶液可以与二氧化碳反应,吸收二氧化碳。
(6)从安全与规范的角度考虑,装置C后面应连接
(7)四氧化三铁的质量为2.32g,充分反应。请计算产生单质铁的质量。(写出解题过程)
您最近一年使用:0次



