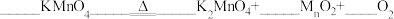写出下列反应的化学方程式。
(1)酒精充分燃烧。
(2)实验室常温下制取氧气。
(3)实验室用石灰石与稀盐酸反应制取二氧化碳。
(1)酒精充分燃烧。
(2)实验室常温下制取氧气。
(3)实验室用石灰石与稀盐酸反应制取二氧化碳。
更新时间:2019-03-11 18:30:22
|
相似题推荐
填空与简答-填空题
|
适中
(0.65)
名校
【推荐1】新版《生活饮用水卫生标准》(简称新国标)中水质检测指标从原来的35项增加 到106项,对供水各环节的水质提出了相应的要求。
(1)新国标在无机物指标中修订了镉、铅等的限量,这里的镉、铅指的是______ (填序号)。
A.原子 B.分子 C.元素 D.单质
(2)新国标中消毒剂由1项增至4项,加入了对用臭氧、二氧化氯和氯胺消毒的规定。
①臭氧在消毒过程中转化为氧气,臭氧转化为氧气属于__________ (填“物理”或者“化学”) 变化;
②氧气中氧元素的化合价为________________ ;消毒过程中产生的次氯酸根离子(ClO-)也有消毒作用, ClO-中氯元素的化合价为 __________ ;
(3)城镇自来水厂生产流程可用如图表示:
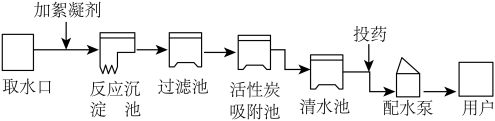
常用的絮凝剂是_______________ ;除去水中固态杂质的设备是 __________ ;活性炭吸附池的作 用是 __________ ;净水过程中发生化学变化的是 ____________ 。
(4)自然界的水多含有杂质,含有较多______ 的水通常称为硬水;鉴别硬水 和软水可用 ________ ;生活中一种软化硬水的简易办法是 _______________________ 。
(5)下列关于水的说法中,不正确的有_________________ (填序号)。
①水是由氢元素和氧元素组成的化合物②清澈、透明的泉水是纯净物③禁止施用农药、化肥, 以减少水体污染④将活性炭放入硬水中可使其软化⑤洗菜、洗衣后的水用来浇花、冲洗厕所。
(6)电解水实验揭示了水的组成,如图实验中得到氧气的试管是____ 。(填“1” 或“2”)。该反应的符号表达式是 ________ 。
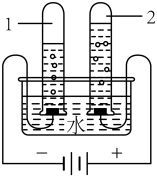
(7)水电解的过程中,发生变化的有_________ (填字母序号)
A.元素的种类 B.分子种类 C.原子的种类 D.元素的化合价
(1)新国标在无机物指标中修订了镉、铅等的限量,这里的镉、铅指的是
A.原子 B.分子 C.元素 D.单质
(2)新国标中消毒剂由1项增至4项,加入了对用臭氧、二氧化氯和氯胺消毒的规定。
①臭氧在消毒过程中转化为氧气,臭氧转化为氧气属于
②氧气中氧元素的化合价为
(3)城镇自来水厂生产流程可用如图表示:

常用的絮凝剂是
(4)自然界的水多含有杂质,含有较多
(5)下列关于水的说法中,不正确的有
①水是由氢元素和氧元素组成的化合物②清澈、透明的泉水是纯净物③禁止施用农药、化肥, 以减少水体污染④将活性炭放入硬水中可使其软化⑤洗菜、洗衣后的水用来浇花、冲洗厕所。
(6)电解水实验揭示了水的组成,如图实验中得到氧气的试管是

(7)水电解的过程中,发生变化的有
A.元素的种类 B.分子种类 C.原子的种类 D.元素的化合价
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】在一定条件下,A、B能发生化学反应生成C和D,其微观示意图如下:

①若D为空气中体积分数最大的气体,则该反应中生成的C和D的分子个数比为___ .
②若D为氧化物,且A、B的分子个数比为5:4,则该反应的化学方程式为______ .

①若D为空气中体积分数最大的气体,则该反应中生成的C和D的分子个数比为
②若D为氧化物,且A、B的分子个数比为5:4,则该反应的化学方程式为
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
【推荐3】我国具有丰富的煤炭资源,煤制取乙二醇的产业化发展已列入我国石化产业调整和振兴规划,由煤制取乙二醇的流程示意图:
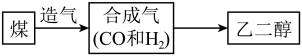
(1)煤属于____ (填“可再生”或“不可再生”)能源;
(2)合成气可用作气体燃料,写出合成气中CO燃烧的化学方程式:_____ ;
(3)合成气(CO和H2)在不同催化剂的作用下,可以合成不同的物质,从物质组成的角度考虑,仅用合成气为原料不可能得到的物质是____ (填序号),理由是:_____ 。
①乙醇(C2H5OH);②甲醇(CH3OH);③尿素[CO(NH2)2]
(4)为了防止煤矿的矿井发生瓦斯爆炸事故,下列做法可行的是___ (填序号,下同)
A 进矿井前先做灯火实验 B 工人必须戴安全帽才能进入矿井
C 矿井内要加强通风 D 安装瓦斯探头传感器监测瓦斯浓度

(1)煤属于
(2)合成气可用作气体燃料,写出合成气中CO燃烧的化学方程式:
(3)合成气(CO和H2)在不同催化剂的作用下,可以合成不同的物质,从物质组成的角度考虑,仅用合成气为原料不可能得到的物质是
①乙醇(C2H5OH);②甲醇(CH3OH);③尿素[CO(NH2)2]
(4)为了防止煤矿的矿井发生瓦斯爆炸事故,下列做法可行的是
A 进矿井前先做灯火实验 B 工人必须戴安全帽才能进入矿井
C 矿井内要加强通风 D 安装瓦斯探头传感器监测瓦斯浓度
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐1】将二氧化碳转化为有机物是实现“碳中和”的途径之一,我国科学家研制了全球首套捕集二氧化碳合成甲醇(CH3OH)的装置,有利于实现“碳中和”。以下是将二氧化碳在一定条件下转化成CH3OH的工艺流程图。
查阅资料:甲醇常温下是一种无色液体,易溶于水,熔点一97.8℃,沸点64.7℃。
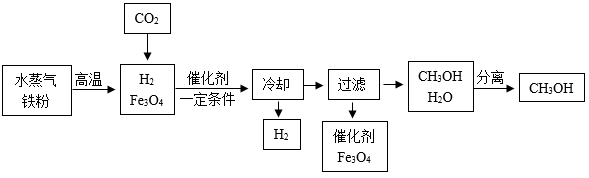
(1)实验室进行过滤操作需要用到的玻璃仪器有______ (填一种即可)。
(2)请写出铁和水蒸气发生反应的化学方程式______ 。
(3)CO2合成CH3OH的化学方程式: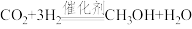 。该反应使用过量H2的原因是
。该反应使用过量H2的原因是______ 。
(4)请你设计分离出CH3OH的一种方案:______ 。
查阅资料:甲醇常温下是一种无色液体,易溶于水,熔点一97.8℃,沸点64.7℃。

(1)实验室进行过滤操作需要用到的玻璃仪器有
(2)请写出铁和水蒸气发生反应的化学方程式
(3)CO2合成CH3OH的化学方程式:
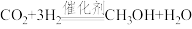 。该反应使用过量H2的原因是
。该反应使用过量H2的原因是(4)请你设计分离出CH3OH的一种方案:
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
名校
解题方法
【推荐2】一定条件下,A和B反应生成C和D。反应前后分子种类变化的微观示意图如下所示:
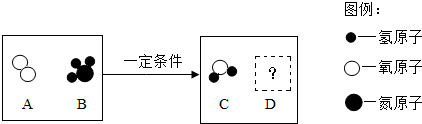
(1)一个B分子中含有________ 个原子;
(2)A、B、C中属于化合物的是________ ;(填字母序号)
(3)写出C在通电条件下分解的方程式______________ 。
(4)①若D为空气中体积分数最大的气体,则该反应中生成的C和D的质量比为__________ ;(填最简整数比)
②若D为氧化物,且A和B的分子个数比为7∶4,则该反应的化学方程式为_____________ 。

(1)一个B分子中含有
(2)A、B、C中属于化合物的是
(3)写出C在通电条件下分解的方程式
(4)①若D为空气中体积分数最大的气体,则该反应中生成的C和D的质量比为
②若D为氧化物,且A和B的分子个数比为7∶4,则该反应的化学方程式为
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】质量守恒定律应用的研究对化学科学发展具有重大作用。
(1)对质量守恒定律的微观解释是:在化学反应中,反应前后原子的____ 、____ 、___ 都不改变。
(2)在一定条件下,将100 mL的CO2缓缓通过足量的淡黄色固体Na2O2,充分反应后,生成50mL纯净的气体X,X能使带火星的木条复燃,淡黄色固体部分变为白色固体Y。
友情提示:在同温同压下,气体的体积比等于分子个数比。
请回答:X气体是______ ;该反应的化学方程式可表示为:a Na2O2 + b CO2 =cX + d Y (其中a、b、c、d为化学计量数),则b:c = _______ ;已知a:b=1:1,则Y是______ 。
(3)汽车安装安全气囊可以有效保护乘车人员,在车辆发生剧烈碰撞的瞬间,安全装置通电点火,使其中的粉末迅速分反应放出大量的氮气,形成气囊。该粉末由Fe2O3固体和化合物甲组成,加热13.0 g化合物甲,完全分解生成8.4 g氮气和单质乙。单质乙可在高温隔绝空气的条件下与Fe2O3发生置换反应生成Na2O。则化合物甲的化学式是______ 。
(1)对质量守恒定律的微观解释是:在化学反应中,反应前后原子的
(2)在一定条件下,将100 mL的CO2缓缓通过足量的淡黄色固体Na2O2,充分反应后,生成50mL纯净的气体X,X能使带火星的木条复燃,淡黄色固体部分变为白色固体Y。
友情提示:在同温同压下,气体的体积比等于分子个数比。
请回答:X气体是
(3)汽车安装安全气囊可以有效保护乘车人员,在车辆发生剧烈碰撞的瞬间,安全装置通电点火,使其中的粉末迅速分反应放出大量的氮气,形成气囊。该粉末由Fe2O3固体和化合物甲组成,加热13.0 g化合物甲,完全分解生成8.4 g氮气和单质乙。单质乙可在高温隔绝空气的条件下与Fe2O3发生置换反应生成Na2O。则化合物甲的化学式是
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐1】铜是人类最早利用的金属之一。利用废旧电池铜帽(含Cu、Zn两种金属)制取海绵铜(Cu),并得到硫酸锌溶液,主要流程如图所示(反应条件已略去),已知: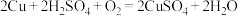 。
。
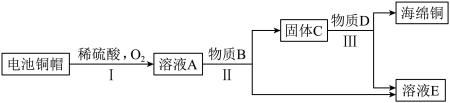
(1)溶液A中溶质一定有的是________ (填化学式)。
(2)过程Ⅱ的实验操作是________ ,物质B的名称是________ 。
(3)请写出过程Ⅲ发生反应的化学方程式________ 。
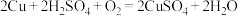 。
。
(1)溶液A中溶质一定有的是
(2)过程Ⅱ的实验操作是
(3)请写出过程Ⅲ发生反应的化学方程式
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐2】整理归纳是有效的学习方法.下面是某学习小组的同学对Mg、Fe、Cu、Hg、Ag五种金属相关知识的归纳复习,请回答下列问题:
(1)从物理性质上看,每种金属都有自己的特性,你认为Hg与其它四种金属的不同之处是________ .
(2)从化学性质上看,与盐酸反应最剧烈的是________ , 反应的化学方程式________ .
(3)在这五种金属中,有一种金属的盐溶液能与其它四种金属反应,该金属是________ ,写出其中一个反应的化学方程式: ________ .
(4)性质决定用途,用途反映性质是重要的化学学科思想,用镁粉制作烟花,在夜空中发出耀眼白光,这是利用镁的________ 性.
(1)从物理性质上看,每种金属都有自己的特性,你认为Hg与其它四种金属的不同之处是
(2)从化学性质上看,与盐酸反应最剧烈的是
(3)在这五种金属中,有一种金属的盐溶液能与其它四种金属反应,该金属是
(4)性质决定用途,用途反映性质是重要的化学学科思想,用镁粉制作烟花,在夜空中发出耀眼白光,这是利用镁的
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐3】高纯碳酸钙广泛应用于精密电子陶瓷、医药等的生产,以石灰石矿粉(含有SiO2、Fe2O3、MgSO4等杂质)为原料,生产高纯碳酸钙的流程如图:______ 。
(2)氧化铁与盐酸反应的化学方程式为______ 。
(3)滤渣3中除有Ca(OH)2外,还有______ (填化学式);
(4)将得到的NH4Cl溶液中加入氢氧化钙溶液并加热,可以得到的气体是______ (填化学式)。

(2)氧化铁与盐酸反应的化学方程式为
(3)滤渣3中除有Ca(OH)2外,还有
(4)将得到的NH4Cl溶液中加入氢氧化钙溶液并加热,可以得到的气体是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】配平下列化学方程式
(1)___ A1+___ Fe2O3﹣﹣___ Fe+___ A12O3
(2)___ C3H6 +___ O2 
___ CO2 +___ H2O
(3)___ Al+___ HCl﹣﹣___ AlCl3 +___ H2↑
(4)___ NH3 +___ O2
___ NO+___ H2O
(5)___ Fe2O3 +___ CO 
___ Fe+___ CO2
(1)
(2)

(3)
(4)

(5)

您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐3】今年入冬以来,我国北方大部分地区遭遇几十年未见的特大旱灾,为缓解灾情,有些地区使用了干冰进行人工降雨,但二氧化碳也是温室效应的元凶之一,因此有科学家设想:将排放到空气中的二氧化碳压缩使其液化,然后将其压入到深海中,但也有科学家担心海水中富含二氧化碳后酸度会增强,可能会杀死一 些海生物,甚至会溶解掉部分海床,从而造成灾难性的后果。
(1)为验证二氧化碳溶于水呈酸性,一般把二氧化碳通入到_____ 试液;
(2)一定条件下可将二氧化碳气体压缩成干冰,从分子角度可解释为分子间有_____ ;
(3)为减少大气中二氧化碳含量,将过多的二氧化碳和氢气在催化剂和加热的条件下反应,转化为水和甲烷(CH4),这个反应的化学方程式为_____ 。
(1)为验证二氧化碳溶于水呈酸性,一般把二氧化碳通入到
(2)一定条件下可将二氧化碳气体压缩成干冰,从分子角度可解释为分子间有
(3)为减少大气中二氧化碳含量,将过多的二氧化碳和氢气在催化剂和加热的条件下反应,转化为水和甲烷(CH4),这个反应的化学方程式为
您最近一年使用:0次