为了研究质量守恒定律,设计了右图“白磷燃烧前后质量测定”的实验,请分析有关问题:

(1)装置:锥形瓶的底部铺有一层细沙,其作用是_______________________ 。
(2)燃烧前称量,锥形瓶的总质量为27.6g,则右图托盘天平中游码的读数为______ g.
(3)白磷燃烧:白磷燃烧过程中看到的现象是____________________________ 。
(4)燃烧后称量:发现托盘天平指针偏向右边,造成的原因可能是_________ (只写一条)。
(5)反思:白磷燃烧_______ (填“遵守”或“不遵守”)质量守恒定律,
理由是_______________________________ 。

(1)装置:锥形瓶的底部铺有一层细沙,其作用是
(2)燃烧前称量,锥形瓶的总质量为27.6g,则右图托盘天平中游码的读数为
(3)白磷燃烧:白磷燃烧过程中看到的现象是
(4)燃烧后称量:发现托盘天平指针偏向右边,造成的原因可能是
(5)反思:白磷燃烧
理由是
2011·广东佛山·中考真题 查看更多[5]
(已下线)2011年初中毕业升学考试(广东佛山卷)化学(已下线)2013届江苏省常州市七校九年级12月联考化学试卷2016届江西省抚州市金溪二中九年级下学期第四次月考化学试卷鲁教版九年级上册第五单元第一节 化学反应中的质量守恒河北省邢台市临西县2019-2020学年九年级(实验班)上学期期中化学试题
更新时间:2019-01-30 18:14:09
|
【知识点】 实验探究质量守恒定律解读
相似题推荐
综合应用题
|
较难
(0.4)
【推荐1】化学实验是科学探究的重要手段。
(1)某化学小组用下图装置制取氧气。
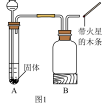
①A中发生反应的化学方程式为___________ 。
②若用B装置收集氧气,请将B装置中导管补画完整___________ 。
③下图2是探究燃烧条件的实验装置,铜片上的白磷燃烧,铜片上的红磷未燃烧,说明燃烧的条件之一是___________ 。

(2)如图是A、B、C三位同学设计的验证质量守恒定律的实验装置,请回答:
①A同学设计的实验中,导气管上端绑上了一个小气球,其目的是___________ 。
②请描述B同学实验过程中的现象___________ ,该反应的化学方程式是___________ 。
③C同学在实验验证时,发现反应结束天平不平衡,请用化学方程式解释原因___________ 。
(3)为测定鸡蛋壳中碳酸钙的质量分数,称取6g洗净、干燥的鸡蛋壳放入烧杯中,向其中加入25g稀盐酸,二者恰好完全反应。反应结束后称量烧杯中剩余物质的总质量为28.8g(不包括烧杯的质量,且气体的溶解忽略不计)。请计算该鸡蛋壳中碳酸钙的质量分数(写出计算过程,精确到0.1%)。________
(1)某化学小组用下图装置制取氧气。

①A中发生反应的化学方程式为
②若用B装置收集氧气,请将B装置中导管补画完整
③下图2是探究燃烧条件的实验装置,铜片上的白磷燃烧,铜片上的红磷未燃烧,说明燃烧的条件之一是

(2)如图是A、B、C三位同学设计的验证质量守恒定律的实验装置,请回答:
 |  |  |
| A | B | C |
②请描述B同学实验过程中的现象
③C同学在实验验证时,发现反应结束天平不平衡,请用化学方程式解释原因
(3)为测定鸡蛋壳中碳酸钙的质量分数,称取6g洗净、干燥的鸡蛋壳放入烧杯中,向其中加入25g稀盐酸,二者恰好完全反应。反应结束后称量烧杯中剩余物质的总质量为28.8g(不包括烧杯的质量,且气体的溶解忽略不计)。请计算该鸡蛋壳中碳酸钙的质量分数(写出计算过程,精确到0.1%)。
您最近一年使用:0次
综合应用题
|
较难
(0.4)
解题方法
【推荐2】科学探究是学习化学的一条重要途径和有效方法。兴趣小组的同学依据教材实验对化学反应前后的质量变化进行了探究和定量计算。
【查阅资料】碳酸钠和稀盐酸反应生成氯化钠、水和二氧化碳气体。
【装置设计】甲、乙、丙三组同学分别设计了如图所示的装置:

【讨论与探究】
(1)甲实验中,反应的化学方程式是______ ,该实验可观察到的现象是______ 。
(2)乙实验可观察到天平指针向______ (填“左”或“右”)偏,产生该现象的原因是______ 。
(3)根据丙组实验可得出:参加化学反应的各物质的质量总和______ (填“大于”或“小于”或“等于”)反应后生成的各物质的质量总和。
【实验分析】
(4)请解释化学反应前后质量守恒的原因:在化学反应前后原子种类没有改变,______ 没有增减,原子的质量也没有改变。
【反思与交流】
(5)通过对甲、乙、丙三组实验的探究,得到的启示是:验证质量守恒定律时,如果有气体参加或生成,应该在密闭容器中进行。
(6)丁组同学探究并测定摩擦剂中CaCO3的质量分数。
已知某品牌牙膏中的摩擦剂是CaCO3和SiO2。已知:SiO2不溶于水也不与稀盐酸反应,CaCO3与稀盐酸反应的化学方程式为 ,CO2全部逸出。现将10g摩擦剂与36.5g稀盐酸充分混合,两者恰好完全反应,称量剩余混合物为44.3g。
,CO2全部逸出。现将10g摩擦剂与36.5g稀盐酸充分混合,两者恰好完全反应,称量剩余混合物为44.3g。
①求生成CO2的质量为______ g。
②求摩擦剂中CaCO3的质量分数______ 。(写出计算过程)
【查阅资料】碳酸钠和稀盐酸反应生成氯化钠、水和二氧化碳气体。
【装置设计】甲、乙、丙三组同学分别设计了如图所示的装置:

【讨论与探究】
(1)甲实验中,反应的化学方程式是
(2)乙实验可观察到天平指针向
(3)根据丙组实验可得出:参加化学反应的各物质的质量总和
【实验分析】
(4)请解释化学反应前后质量守恒的原因:在化学反应前后原子种类没有改变,
【反思与交流】
(5)通过对甲、乙、丙三组实验的探究,得到的启示是:验证质量守恒定律时,如果有气体参加或生成,应该在密闭容器中进行。
(6)丁组同学探究并测定摩擦剂中CaCO3的质量分数。
已知某品牌牙膏中的摩擦剂是CaCO3和SiO2。已知:SiO2不溶于水也不与稀盐酸反应,CaCO3与稀盐酸反应的化学方程式为
 ,CO2全部逸出。现将10g摩擦剂与36.5g稀盐酸充分混合,两者恰好完全反应,称量剩余混合物为44.3g。
,CO2全部逸出。现将10g摩擦剂与36.5g稀盐酸充分混合,两者恰好完全反应,称量剩余混合物为44.3g。①求生成CO2的质量为
②求摩擦剂中CaCO3的质量分数
您最近一年使用:0次
综合应用题
|
较难
(0.4)
【推荐3】科学探究是学习化学的重要方法之一。
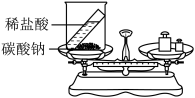
(1)用如图所示的实验装置验证质量守恒定律。将装有碳酸钠粉末的烧杯倾斜,使试管中的稀盐酸流入烧杯中,反应的化学方程式是___________ ,反应结束后将烧杯放回天平托盘上,天平指针________ (填“向左偏”“向右偏”或“指向正中”)
(2)成成对(1)中反应后溶液中的溶质提出以下猜想:
猜想一:NaCl;猜想二:Na2CO3、NaCl;猜想三:Na2CO3、NaCl、HCl。
上述猜想错误的是______________ ;原因:____________________________ 。
(3)如果你进行该探究活动,会对实验方案做出怎样的改进?____________
(4)同学们认为还可以有别的猜想,提出你的猜想并设计实验验证(简要写出操作、现象)。___________
(5)超细氮化铝(其中氮元素为-3价)粉末被广泛应用于大规模集成电路生产领域。其制取原理为氧化铝、碳、氮气在高温下反应生成氮化铝和一氧化碳。现欲用以上方法来制备16.4t氮化铝,需要参加反应的氧化铝(Al2O3)质量是多少?____________
(1)用如图所示的实验装置验证质量守恒定律。将装有碳酸钠粉末的烧杯倾斜,使试管中的稀盐酸流入烧杯中,反应的化学方程式是

(2)成成对(1)中反应后溶液中的溶质提出以下猜想:
猜想一:NaCl;猜想二:Na2CO3、NaCl;猜想三:Na2CO3、NaCl、HCl。
上述猜想错误的是
(3)如果你进行该探究活动,会对实验方案做出怎样的改进?
(4)同学们认为还可以有别的猜想,提出你的猜想并设计实验验证(简要写出操作、现象)。
(5)超细氮化铝(其中氮元素为-3价)粉末被广泛应用于大规模集成电路生产领域。其制取原理为氧化铝、碳、氮气在高温下反应生成氮化铝和一氧化碳。现欲用以上方法来制备16.4t氮化铝,需要参加反应的氧化铝(Al2O3)质量是多少?
您最近一年使用:0次



