如图是甲、乙、丙三种固体物质(均不含结晶水)的溶解度曲线,回答下列问题。
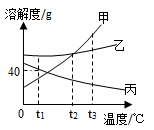
①t3℃ 时,物质甲、乙、丙的溶解度由小到大的是____ 。
②t1℃时,将25g丙加入到50g水中充分溶解后所得溶液的质量为____ 。
③甲中含有少量的乙,欲提纯甲应采用的方法是____ 。
④将100g10%的甲溶液稀释到4%需加入____ 水。
⑤t3℃时,将甲、乙、丙三种物质的饱和溶液降温至t1℃时,这时三种溶液的溶质质量分数由大到小是___________ 。

①t3℃ 时,物质甲、乙、丙的溶解度由小到大的是
②t1℃时,将25g丙加入到50g水中充分溶解后所得溶液的质量为
③甲中含有少量的乙,欲提纯甲应采用的方法是
④将100g10%的甲溶液稀释到4%需加入
⑤t3℃时,将甲、乙、丙三种物质的饱和溶液降温至t1℃时,这时三种溶液的溶质质量分数由大到小是
更新时间:2019-03-28 17:14:34
|
相似题推荐
填空与简答-流程题
|
较难
(0.4)
解题方法
【推荐1】近年来北部湾经济发展迅速,城市建设需要使用大量木材,硫酸锌是木材的防腐材料。工业上用废旧电池(锌皮中含有杂质铁,炭包是被二氧化锰包围的石墨电极)制备七水硫酸锌的流程如下。

已知:①过氧化氢具有强氧化性,能将亚铁离子氧化为铁离子。
②ZnSO4·7H2O 加热至 39℃以上会逐渐失去结晶水。
③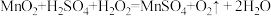 。
。
(1)“溶解”前将锌皮粉碎的目的是______ 。
(2)写出加入 NaOH 溶液“调 pH”的目的是______ 。
(3)从滤液得到 ZnSO4·7H2O 需经过蒸发浓缩、结晶等,此过程中温度范围应控制在______ 。
(4)写出加入 Na2CO3溶液“沉锰”时发生的化学反应方程式______ 。
(5)“焙烧”的目的有______ (填序号)。
①是将 MnCO3转化为 MnO2
②是除去 MnO2中未反应的石墨
③使硫酸挥发

已知:①过氧化氢具有强氧化性,能将亚铁离子氧化为铁离子。
②ZnSO4·7H2O 加热至 39℃以上会逐渐失去结晶水。
③
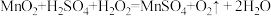 。
。(1)“溶解”前将锌皮粉碎的目的是
(2)写出加入 NaOH 溶液“调 pH”的目的是
(3)从滤液得到 ZnSO4·7H2O 需经过蒸发浓缩、结晶等,此过程中温度范围应控制在
(4)写出加入 Na2CO3溶液“沉锰”时发生的化学反应方程式
(5)“焙烧”的目的有
①是将 MnCO3转化为 MnO2
②是除去 MnO2中未反应的石墨
③使硫酸挥发
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
解题方法
【推荐2】如表是氯化钠和硝酸钾在不同温度下的溶解度(假设硝酸钾与氯化钠同时溶解在水中各自的溶解度不变,实验过程中水分损失忽略不计)。
(1)60℃时,KNO3的溶解度为______ g;
(2)硝酸钾和氯化钠溶解度相同时的温度范围是______;
(3)在80℃的200g水中溶解NaCl和KNO3,进行以下实验:

对整个实验过程分析正确的是______ 。
A x 的数值为50g
B 对溶液B降温时,当温度达到60℃开始析出晶体
C 固体E中只含有206.1g KNO3
D 上述方法不能将氯化钠和硝酸钾完全分离
E 溶液A直接降温结晶,析出硝酸钾的质量不变
| 温度(℃) | 0 | 20 | 40 | 60 | 80 | 100 | |
| 溶解度(g) | KNO3 | 13.3 | 31.6 | 63.9 | 110.0 | 169.0 | 246.0 |
| NaCl | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 | |
(1)60℃时,KNO3的溶解度为
(2)硝酸钾和氯化钠溶解度相同时的温度范围是______;
| A.0℃—20℃ | B.20℃—40℃ | C.40℃—60℃ | D.60℃—80℃ |
(3)在80℃的200g水中溶解NaCl和KNO3,进行以下实验:

对整个实验过程分析正确的是
A x 的数值为50g
B 对溶液B降温时,当温度达到60℃开始析出晶体
C 固体E中只含有206.1g KNO3
D 上述方法不能将氯化钠和硝酸钾完全分离
E 溶液A直接降温结晶,析出硝酸钾的质量不变
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
真题
解题方法
【推荐3】为研究溶解度曲线的应用,学习小组查得资料:某钢铁厂处理高盐废水(含氯化钠、硫酸钠及微量的其他盐)的流程、相关物质的溶解度曲线如下图所示。请和小组同学一起研究。_________________ 。
(2)当温度高于________________ ℃时,硫酸钠的溶解度随温度升高而降低。
(3)40℃时,将50g硫酸钠固体加入100g水中,充分搅拌后所得溶液的溶质质量分数为________________ (列出计算式即可)。
(4)降温至0℃的“冷冻结晶”过程,析出的两种物质中较多的是_________________ 。
(5)结合溶解度曲线解释,“蒸发结晶2”主要得到氯化钠的原因是_________________ 。

(2)当温度高于
(3)40℃时,将50g硫酸钠固体加入100g水中,充分搅拌后所得溶液的溶质质量分数为
(4)降温至0℃的“冷冻结晶”过程,析出的两种物质中较多的是
(5)结合溶解度曲线解释,“蒸发结晶2”主要得到氯化钠的原因是
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
【推荐1】根据下图甲、乙、丙三种固体(均不含结晶水)的溶解度曲线回答:
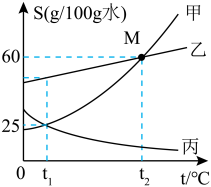
(1)t1℃甲物质的溶解度是_____ 。
(2)t2℃时,对 50g 甲物质投入到 80g 水中充分溶解,溶质与溶液的质量比为_____ 。
(3)t1℃时,对恰好处于 a 点状态的甲的溶液,升温至 t2℃,溶质质量分数_____ (选填“变大”、“变小”或“不变”)。
(4)分别将 t2℃的三种物质的饱和溶液 100g 降温到 t1℃时,甲、乙、丙溶液质量由大到小关系为_____ (选 填“<”、“>”或“=”)。
(5)溶液甲中含有少量的乙,提纯甲物质的方法是_____ 。
(6)A 是 t2℃含有 120g 水的甲物质的溶液,经过如下操作,得到 32g 甲的固体。
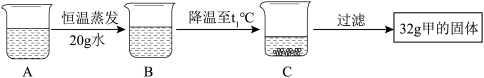
Ⅰ. A 溶液为_____ (选填“饱和”或“不饱和”)溶液。
关于溶质的质量分数:溶液 B_____ 溶液 C(选填“>”、“>”或“=”)。
Ⅱ. 对 A→C 的过程的分析,正确的是_____ (选填编号)。
a A 到 B 的过程中,溶质质量不变
b B 中溶质与溶剂的质量比为 57:100
c A 中溶液的质量等于 187g
d 无法比较A、C 烧杯中溶液溶质的质量分数
(7)欲配制 200g 溶质质量分数为 5%的丙物质的溶液,需要固体丙_____ g,水_____ mL。

(1)t1℃甲物质的溶解度是
(2)t2℃时,对 50g 甲物质投入到 80g 水中充分溶解,溶质与溶液的质量比为
(3)t1℃时,对恰好处于 a 点状态的甲的溶液,升温至 t2℃,溶质质量分数
(4)分别将 t2℃的三种物质的饱和溶液 100g 降温到 t1℃时,甲、乙、丙溶液质量由大到小关系为
(5)溶液甲中含有少量的乙,提纯甲物质的方法是
(6)A 是 t2℃含有 120g 水的甲物质的溶液,经过如下操作,得到 32g 甲的固体。

Ⅰ. A 溶液为
关于溶质的质量分数:溶液 B
Ⅱ. 对 A→C 的过程的分析,正确的是
a A 到 B 的过程中,溶质质量不变
b B 中溶质与溶剂的质量比为 57:100
c A 中溶液的质量等于 187g
d 无法比较A、C 烧杯中溶液溶质的质量分数
(7)欲配制 200g 溶质质量分数为 5%的丙物质的溶液,需要固体丙
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
解题方法
【推荐2】工业上采用氨碱法生产纯碱(Na2CO3),主要流程如图:

加热碳酸化吸氨纯碱饱和氨盐水碳酸钠饱和食盐水.其生产过程中有下列反应:①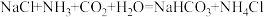 ;②
;②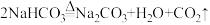 ;
;
碳酸氢钠和氯化铵的溶解度曲线如图所示.
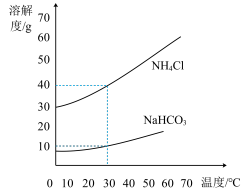
请回答下列问题:
(1)30℃时,碳酸氢钠的溶解度是_____ 。
(2)30℃时,氯化铵饱和溶液中溶质质量分数_____ 碳酸氢钠饱和溶液中溶质质量分数(填“大于”“小于”“等于”之一)
(3)反应①中生成物碳酸氢钠和氯化铵的质量比为____ :_____ 。
(4)氨盐水吸收二氧化碳后生成碳酸氢钠和氯化铵,哪种物质首先结晶析出?____ 根据溶解度曲线和两者的质量关系分析原因_______ 。

加热碳酸化吸氨纯碱饱和氨盐水碳酸钠饱和食盐水.其生产过程中有下列反应:①
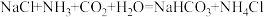 ;②
;②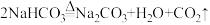 ;
;碳酸氢钠和氯化铵的溶解度曲线如图所示.

请回答下列问题:
(1)30℃时,碳酸氢钠的溶解度是
(2)30℃时,氯化铵饱和溶液中溶质质量分数
(3)反应①中生成物碳酸氢钠和氯化铵的质量比为
(4)氨盐水吸收二氧化碳后生成碳酸氢钠和氯化铵,哪种物质首先结晶析出?
您最近一年使用:0次
【推荐3】(1)下图是不与水发生化学反应的a、b、c三种物质的溶解度曲线,a与c的溶解度曲线相交于P点。据图回答:

①P 点的含义是_________________________ 。
②t 2℃时a、b、c三种物质的溶解度按由小到大的顺序排列是_______ (填写物质序号)。
③t 2℃时30ga物质加入50g水中不断搅拌,所得溶液的溶质质量分数___________ 。
④将t1℃时a、b、c三种物质饱和溶液的温度升高到t2℃时,三种溶液的溶质质量分数大小关系是_____ (填写选项序号)。
(2)根据下表回答:
①BaCO3的溶解性______________ 。从上表中找出一种不溶碱______________ (填化学式)。
②Zn(NO3)2、BaCl2两种溶液能不能发生反应?____________ (填:能”或“不能”)
③利用上表写一个有氢氧化铜生成的复分解反应化学方程式:___________ 。

①P 点的含义是
②t 2℃时a、b、c三种物质的溶解度按由小到大的顺序排列是
③t 2℃时30ga物质加入50g水中不断搅拌,所得溶液的溶质质量分数
④将t1℃时a、b、c三种物质饱和溶液的温度升高到t2℃时,三种溶液的溶质质量分数大小关系是
| A.c>a=b | B.a=b>c | C.a>b>c | D.b>a>c |
| OH- |  | Cl- |  |  | |
| H+ | 溶、挥 | 溶、挥 | 溶 | 溶、挥 | |
| Na+ | 溶 | 溶 | 溶 | 溶 | 溶 |
| Ca2+ | 微溶 | 溶 | 溶 | 微溶 | 不溶 |
| Cu2+ | 不溶 | 溶 | 溶 | 溶 | 不溶 |
| Ba2+ | 溶 | 溶 | 溶 | 不溶 | 不溶 |
| Zn2+ | 不溶 | 溶 | 溶 | 溶 | 不溶 |
②Zn(NO3)2、BaCl2两种溶液能不能发生反应?
③利用上表写一个有氢氧化铜生成的复分解反应化学方程式:
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
名校
【推荐1】氯酸钾常用于制造火柴盒烟花等。工业上通过如图 1 所示转化可制得氯酸钾晶体。结合图2的溶解度曲线,回答下列问
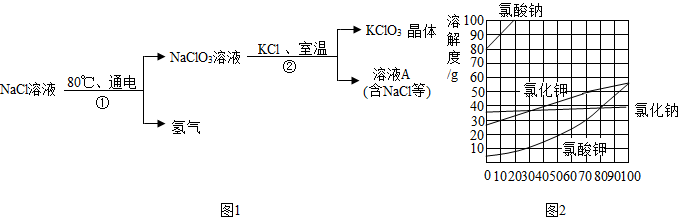
(1)80℃的氯化钠溶液中,氯化钠与水的质量比为 7:20,该溶液是_____ (填“饱和溶液”或“不饱和溶液”)。
(2)40℃,氯化钾溶解度为 40g,要配置 70g 该温度的饱和溶液,需要氯化钾_____ g, 水_____ g。
(3)10℃时,如图中四种物质的饱和溶液,其中_____ 溶液的溶质质量分数最小。
(4)写出反应①的化学方程式:_____ 。
(5)反应②能发生的原因是_____ 。
(6)生成过程中,溶液 A 可循环利用,其优点是_____ (写一点)。

(1)80℃的氯化钠溶液中,氯化钠与水的质量比为 7:20,该溶液是
(2)40℃,氯化钾溶解度为 40g,要配置 70g 该温度的饱和溶液,需要氯化钾
(3)10℃时,如图中四种物质的饱和溶液,其中
(4)写出反应①的化学方程式:
(5)反应②能发生的原因是
(6)生成过程中,溶液 A 可循环利用,其优点是
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
【推荐2】金属在生活、生产中应用广泛。
(1)从微观角度分析,水银温度计测量体温的原理是____________________________ 。
(2)写出工业上用赤铁矿石炼铁的化学方程式____________________________________ 。
(3)下图是光亮铁钉的一系列变化。

①中铁钉锈蚀主要是铁与空气中的____________ 发生化学反应。
②中稀盐酸除铁锈的化学方程式为____________________________ 。
③中所用的溶液X中的金属阳离子为_________ (用符号表示)。
(4)为验证Fe、Cu、Ag三种金属的活动性顺序,下列选用的药品可行的是____ (填字母)。
A Fe、CuSO4溶液、Ag B FeSO4溶液、Cu、Ag
C FeSO4溶液、Cu、AgNO3溶液D FeSO4溶液、CuSO4溶液、Ag
(5)某金属粉末可能由铁、镁、锌、铝、银中的一种或几种组成。取该样品2.4g,向其中加入100g一定溶质量分数的稀硫酸,恰好完全反应,生成0.2g氢气,得到无色溶液,固体无剩余。下列说法正确的是__________ (填字母)。
A 样品中一定含有锌 B 样品中一定不含有银,可能含有铁
C 所得溶液中溶质总质量为12g D 加入的稀硫酸的溶质质量分数为9.8%
(1)从微观角度分析,水银温度计测量体温的原理是
(2)写出工业上用赤铁矿石炼铁的化学方程式
(3)下图是光亮铁钉的一系列变化。

①中铁钉锈蚀主要是铁与空气中的
②中稀盐酸除铁锈的化学方程式为
③中所用的溶液X中的金属阳离子为
(4)为验证Fe、Cu、Ag三种金属的活动性顺序,下列选用的药品可行的是
A Fe、CuSO4溶液、Ag B FeSO4溶液、Cu、Ag
C FeSO4溶液、Cu、AgNO3溶液D FeSO4溶液、CuSO4溶液、Ag
(5)某金属粉末可能由铁、镁、锌、铝、银中的一种或几种组成。取该样品2.4g,向其中加入100g一定溶质量分数的稀硫酸,恰好完全反应,生成0.2g氢气,得到无色溶液,固体无剩余。下列说法正确的是
A 样品中一定含有锌 B 样品中一定不含有银,可能含有铁
C 所得溶液中溶质总质量为12g D 加入的稀硫酸的溶质质量分数为9.8%
您最近一年使用:0次
【推荐1】填空:
(1)用化学符号填空:
①2个氢分子________ ;
②碘酒中的溶剂______ 。
(2)甲、乙两溶液中共有7种离子:K+、Cu2+、Ba2+、Mg2+、OH-、 、
、 。已知两溶液中所含离子各不相同,甲溶液中含有四种离子,且能使紫色石蕊溶液变蓝,则乙溶液中含有的离子是
。已知两溶液中所含离子各不相同,甲溶液中含有四种离子,且能使紫色石蕊溶液变蓝,则乙溶液中含有的离子是______ (填离子符号)。
(3)如下图所示为a、b、c三种物质的溶解度曲线。
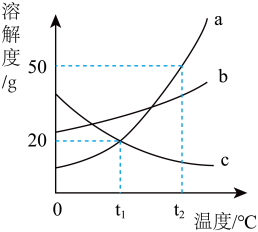
①t1 ℃时,将30 g a物质加入到50 g水中,而后升温到t2 ℃,此时该溶液的溶质和溶剂的质量比为______ 。
②t1 ℃时,将24 g a的饱和溶液稀释为10%的a溶液,需要加入水___ g。
③将t2 ℃时等质量的a、c的饱和溶液降温至t1 ℃,此时两种溶液中溶质的质量分数大小关系为________ 。
(1)用化学符号填空:
①2个氢分子
②碘酒中的溶剂
(2)甲、乙两溶液中共有7种离子:K+、Cu2+、Ba2+、Mg2+、OH-、
 、
、 。已知两溶液中所含离子各不相同,甲溶液中含有四种离子,且能使紫色石蕊溶液变蓝,则乙溶液中含有的离子是
。已知两溶液中所含离子各不相同,甲溶液中含有四种离子,且能使紫色石蕊溶液变蓝,则乙溶液中含有的离子是(3)如下图所示为a、b、c三种物质的溶解度曲线。

①t1 ℃时,将30 g a物质加入到50 g水中,而后升温到t2 ℃,此时该溶液的溶质和溶剂的质量比为
②t1 ℃时,将24 g a的饱和溶液稀释为10%的a溶液,需要加入水
③将t2 ℃时等质量的a、c的饱和溶液降温至t1 ℃,此时两种溶液中溶质的质量分数大小关系为
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
名校
【推荐2】在抗击新型冠状病毒肺炎战役中做好杀菌消毒工作至关重要。下面是几种常见的消毒剂:
(一)酒精(C2H5OH)
(1)在配制 75%的医用酒精溶液时发现 75mL 的酒精和 25mL 的水混合后体积小于 100mL,其原因是________ ;
(2)在室内使用酒精消毒剂时,遇到明火易发生燃烧甚至爆炸。从燃烧的条件分析,明火的作用是______ ,酒精完全燃烧的化学方程式是______ 。
(二)过氧乙酸溶液 其标签上的部分文字如图。
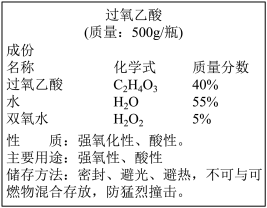
(1)从标签上的成分信息可以推知,过氧乙酸溶液受热时容易发生_____ ;
(2)一瓶这种溶液中含溶质过氧乙酸_____ g;
(3)过氧乙酸中碳、氢、氧元素的质量比为________________ (填最简整数比);
(4)新区实验初中的校医每天都用溶质质量分数为0.5%的过 氧乙酸溶液对教室等场所进行消毒。要配制这种溶液 600kg,需要溶质质量分数为 40%的过氧乙酸溶液____________ kg。
(三)二氧化氯(ClO2)
资料:①ClO2是一种黄绿色、有刺激性气味的气体,熔点:﹣59.0℃,沸点:11.0℃,②冷却至11.0℃以下时变成红色液体,③易溶于水,④见光易分解,⑤易与碱反应,⑥杀菌、漂白能力均优 于 Cl2。消毒水体时不生成有害物质,也不存在用氯气消毒时残留的臭味。
(1)以上关于 ClO2 的描述中,属于化学性质的是________________ (填序号);
(2)制取 ClO2 的方法有多种,目前欧洲一些国家用氯酸钠(NaClO3)与浓盐酸反应制取 ClO2(Kestiog 法),同时有 Cl2、NaCl 和一种常见的氧化物生成,该反应中涉及的氯元素的化合价有________ 种;
(3)我国最近研究成功用 Cl2 和 NaClO2(N2 保护下)制取 ClO2,同时有 NaCl 生成,该反应的化学方程式是_____________ ;此法与 Kestiog 法相比,其优点是_________ ; (写出其中的一条)
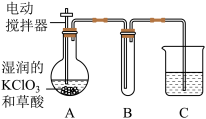
(4)工业上也可以在 60℃时,用稍加潮湿的 KClO3 与草酸(C2H2O4)反应制取 ClO2。某实验小组用如下图装置制取并收集 ClO2,A 为 ClO2 的发生装置,B 为 ClO2 的收集装置,C 为尾气吸收装置。
请问:为了保证实验成功,实验时,A 装置应浸在_____ 中加热; B 装置外加冰水冷却,试管内可观察到的现象是________ ;C 中所盛放的药品可以是______ 。
(一)酒精(C2H5OH)
(1)在配制 75%的医用酒精溶液时发现 75mL 的酒精和 25mL 的水混合后体积小于 100mL,其原因是
(2)在室内使用酒精消毒剂时,遇到明火易发生燃烧甚至爆炸。从燃烧的条件分析,明火的作用是
(二)过氧乙酸溶液 其标签上的部分文字如图。

(1)从标签上的成分信息可以推知,过氧乙酸溶液受热时容易发生
(2)一瓶这种溶液中含溶质过氧乙酸
(3)过氧乙酸中碳、氢、氧元素的质量比为
(4)新区实验初中的校医每天都用溶质质量分数为0.5%的过 氧乙酸溶液对教室等场所进行消毒。要配制这种溶液 600kg,需要溶质质量分数为 40%的过氧乙酸溶液
(三)二氧化氯(ClO2)
资料:①ClO2是一种黄绿色、有刺激性气味的气体,熔点:﹣59.0℃,沸点:11.0℃,②冷却至11.0℃以下时变成红色液体,③易溶于水,④见光易分解,⑤易与碱反应,⑥杀菌、漂白能力均优 于 Cl2。消毒水体时不生成有害物质,也不存在用氯气消毒时残留的臭味。
(1)以上关于 ClO2 的描述中,属于化学性质的是
(2)制取 ClO2 的方法有多种,目前欧洲一些国家用氯酸钠(NaClO3)与浓盐酸反应制取 ClO2(Kestiog 法),同时有 Cl2、NaCl 和一种常见的氧化物生成,该反应中涉及的氯元素的化合价有
(3)我国最近研究成功用 Cl2 和 NaClO2(N2 保护下)制取 ClO2,同时有 NaCl 生成,该反应的化学方程式是
(4)工业上也可以在 60℃时,用稍加潮湿的 KClO3 与草酸(C2H2O4)反应制取 ClO2。某实验小组用如下图装置制取并收集 ClO2,A 为 ClO2 的发生装置,B 为 ClO2 的收集装置,C 为尾气吸收装置。
请问:为了保证实验成功,实验时,A 装置应浸在

您最近一年使用:0次
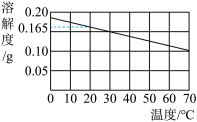
【推荐3】向装有100克水的A、B、C烧杯中分别加入10g、20g、25g某种固体充分溶解后,现象如图一所示。_______ (填“A”“B”或“C”)。
(2)现将C烧杯中溶液加水稀释得到10%的溶液,则需加入水的质量为________ 。
(3)图二能表示该固体溶解度曲线的是______ (填“甲”或“乙”)。
(4)由图二分析,若分别将100g甲、乙的饱和溶液从t2°C降温到t1°C,对所得溶液的叙述正确的是_____(填序号)。

(2)现将C烧杯中溶液加水稀释得到10%的溶液,则需加入水的质量为
(3)图二能表示该固体溶解度曲线的是
(4)由图二分析,若分别将100g甲、乙的饱和溶液从t2°C降温到t1°C,对所得溶液的叙述正确的是_____(填序号)。
| A.甲,乙都是饱和溶液 | B.所含溶剂质量:甲<乙 |
| C.溶液质量:甲>乙 | D.溶质质量分数:甲>乙 |
您最近一年使用:0次