金属及其金属制品对人类社会的发展有着极其重要的作用。
汽车制造过程中要用到大量的铁、铜、铝等金属材料,请按要求填空。
(1)汽车制造中用得最多的金属材料是钢。钢____ (填“是”或“不是”)纯金属。为了防止车体表面生锈,车体要进行____ 。炼铁的原理是利用一氧化碳与氧化铁反应还原出铁,反应的化学方程式为___________________ 。
(2)汽车电路中的导线大都是铜芯的,这主要是利用了铜的____ 性。将赤铜矿(主要成分Cu2O)和辉铜矿(主要成分Cu2S)混合焙烧可得到铜,请将反应的方程式补充完整:2Cu2O+Cu2S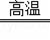 6Cu+
6Cu+____ 。
(3)铁、铜、铝三种元素在地壳中的含量最大的是_______ ,但三种金属被人类发现和利用的时间是铜最早,而铝最晚,主要是因为铝具有很好的抗腐蚀性能,原因是______ (用化学方程式表示)。
(4)为了探究铝、铁、银三种金属活动性顺序,可选择Al、Ag和____ 来进行实验。
汽车制造过程中要用到大量的铁、铜、铝等金属材料,请按要求填空。
(1)汽车制造中用得最多的金属材料是钢。钢
(2)汽车电路中的导线大都是铜芯的,这主要是利用了铜的
 6Cu+
6Cu+(3)铁、铜、铝三种元素在地壳中的含量最大的是
(4)为了探究铝、铁、银三种金属活动性顺序,可选择Al、Ag和
更新时间:2019-03-28 17:14:34
|
相似题推荐
填空与简答-流程题
|
较难
(0.4)
解题方法
【推荐1】富含淀粉的谷物、甘薯等可以酿酒,在酿酒过程中淀粉在酶的作用下转化为葡萄糖,葡萄糖发酵为酒精,香甜的酒酿就是利用该原理,用酒曲酶(俗称酒药)制作的,家庭一般制作酒酿的简单流程图如下(注:有机反应化学方程式可用箭号表示):

(1)配平化学方程式:(C6H10O5)n(淀粉)+________ H2O nC6H12O6(葡萄糖)。
nC6H12O6(葡萄糖)。
(2)如温度、水分等因素控制不当,易导致乳酸量过多而味偏酸,请完成该反应的化学方程式:C6H12O4(葡萄糖)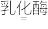 2
2________ (乳酸)。
(3)成熟的酒酿放置时间越长酒味越浓,因为更多的葡萄糖在酒化酶作用下发酵分解为酒精(C2H5OH)和二氧化碳,写出该反应的化学方程式:________________________________________________ 。
(4)若用1kg大米酿米酒,假设其中有0.81kg的淀粉全部转化为酒精,则理论上可酿制含酒精质量分数为10%的米酒________ kg。
[提示]由淀粉转化为酒精的关系式为(C6H10O5)n~2nC2H5OH。

(1)配平化学方程式:(C6H10O5)n(淀粉)+
 nC6H12O6(葡萄糖)。
nC6H12O6(葡萄糖)。(2)如温度、水分等因素控制不当,易导致乳酸量过多而味偏酸,请完成该反应的化学方程式:C6H12O4(葡萄糖)
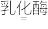 2
2(3)成熟的酒酿放置时间越长酒味越浓,因为更多的葡萄糖在酒化酶作用下发酵分解为酒精(C2H5OH)和二氧化碳,写出该反应的化学方程式:
(4)若用1kg大米酿米酒,假设其中有0.81kg的淀粉全部转化为酒精,则理论上可酿制含酒精质量分数为10%的米酒
[提示]由淀粉转化为酒精的关系式为(C6H10O5)n~2nC2H5OH。
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
【推荐2】配平下列化学反应方程式(答题卷上从左到右依次填写系数)
(1)( ) C2H5OH+( ) O2=( ) CO2+( ) H2O
(2)( ) Cu+( ) HNO3=( ) Cu(NO3)2+( ) NO↑+( ) H2O
(1)
(2)
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
名校
解题方法
【推荐1】我国自主研制的C919大型客机试飞成功,标志着我国飞机制造技术又有了新的突破。回答下列问题。
(1)飞机外壳的主要材料是铝合金,“铝合金”属于________ (填“金属材料”或“合成材料”,下同),飞机座椅上常用到耐磨、耐腐蚀的涤纶等,涤纶属于__________ 。
(2)为了探究飞机材料中铝、铁、铜三种金属的活动性强弱,小鸣设计了下列实验并通过实验现象得出了正确的结论:将三种金属分别取样,分别加入等质量等浓度的稀硫酸,通过看到的现象得出的结论是:活动性__________ ,得出此结论你的依据是_______________ 。
(3)防止金属腐蚀是保护金属资源的有效途径之一。为防止金属锈蚀,可以采取的措施有____ (写一种),用稀盐酸清除铁锈的化学方程式为____________ 。
(4)向硝酸银和硝酸铜的混合溶液中加入一定量的铁粉,充分反应后过滤,得到滤液和滤渣。向滤渣中滴加稀盐酸,有气泡冒出,则滤液中一定含有的溶质是________ 。
(1)飞机外壳的主要材料是铝合金,“铝合金”属于
(2)为了探究飞机材料中铝、铁、铜三种金属的活动性强弱,小鸣设计了下列实验并通过实验现象得出了正确的结论:将三种金属分别取样,分别加入等质量等浓度的稀硫酸,通过看到的现象得出的结论是:活动性
(3)防止金属腐蚀是保护金属资源的有效途径之一。为防止金属锈蚀,可以采取的措施有
(4)向硝酸银和硝酸铜的混合溶液中加入一定量的铁粉,充分反应后过滤,得到滤液和滤渣。向滤渣中滴加稀盐酸,有气泡冒出,则滤液中一定含有的溶质是
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
【推荐2】(1)已知金属M和N能够发生如下反应:M+H2SO4=MSO4+H2↑;Fe+MCl2=M+FeCl2;N+FeCl2=Fe+NCl2判断Fe、M、N的活动性由强到弱的顺序是____ ,以上三个化学反应均属于_____ (填基本反应类型)。
(2)在AgNO3、Cu(NO3)2的混合溶液中加入一定量锌粉,充分反应后过滤,得滤渣和滤液:
①若滤液呈无色,则滤渣中一定含有的物质是______ (填化学式);
②若向滤渣中滴加稀盐酸,无明显现象,则滤液中所含溶质的成分可能有_____ 种情况。
(2)在AgNO3、Cu(NO3)2的混合溶液中加入一定量锌粉,充分反应后过滤,得滤渣和滤液:
①若滤液呈无色,则滤渣中一定含有的物质是
②若向滤渣中滴加稀盐酸,无明显现象,则滤液中所含溶质的成分可能有
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
解题方法
【推荐3】铝、铁、铜是生产生活中常见的金属。
(1)下列不属于铝、铁、铜三种金属都具有的性质是___________(填字母)。
(2)为验证铝、铁、铜的金属活动性顺序,化学兴趣小组的同学分别进行了如下实验:(金属片已打磨)

①甲组同学利用图1所示实验得出了金属活动性顺序Al>Fe>Cu,实验中发生反应的化学方程式为___________ 。
②乙组同学按照铁片、铜片、铝片的顺序插入盛有Y溶液的试管中(如图2),充分反应后(能与Y溶液反应的要一次将Y溶液消耗完),也可得出相同的结论,则Y溶液不可能是___________ (填字母)。
A.稀盐酸 B.硝酸铜 C.硫酸亚铁 D.氯化铝
(1)下列不属于铝、铁、铜三种金属都具有的性质是___________(填字母)。
| A.导热性 | B.导电性 | C.有银白色金属光泽 | D.与稀盐酸反应生成氢气 |
(2)为验证铝、铁、铜的金属活动性顺序,化学兴趣小组的同学分别进行了如下实验:(金属片已打磨)

①甲组同学利用图1所示实验得出了金属活动性顺序Al>Fe>Cu,实验中发生反应的化学方程式为
②乙组同学按照铁片、铜片、铝片的顺序插入盛有Y溶液的试管中(如图2),充分反应后(能与Y溶液反应的要一次将Y溶液消耗完),也可得出相同的结论,则Y溶液不可能是
A.稀盐酸 B.硝酸铜 C.硫酸亚铁 D.氯化铝
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
解题方法
【推荐1】金属是重要的资源,在日常生活中已得到越来越广泛的应用。
(1)早在春秋战国时期,我国就开始生产和使用铁器。请写出以赤铁矿(主要成分为Fe2O3)为原料的工业炼铁的化学方程式:_________ 。
(2)生活中常给门窗和铁栅栏喷漆而防止其生锈,其防锈原理是_______ 。
(3)生活中能见到各种形状的金属制品,这主要是利用了金属的________ 性;而电缆中包裹着铜,这主要是利用了铜的_______ 性。
(4)将一定量的铁粉加入到Al(NO3)3、Cu(NO3)2、AgNO3三种物质的混合溶液中,充分反应后过滤,向滤渣中加入稀盐酸,有气泡产生。则滤液中一定含有________ ,发生的反应属于_______ (填基本反应类型);下列描述中错误的是_______ 。
A.滤液为浅绿色
B.四种金属的活动性顺序是Al>Fe>Cu>Ag
C.滤渣中一定有Ag、Cu、Fe、Al
D.滤液中一定有Fe2+、Al3+、
(1)早在春秋战国时期,我国就开始生产和使用铁器。请写出以赤铁矿(主要成分为Fe2O3)为原料的工业炼铁的化学方程式:
(2)生活中常给门窗和铁栅栏喷漆而防止其生锈,其防锈原理是
(3)生活中能见到各种形状的金属制品,这主要是利用了金属的
(4)将一定量的铁粉加入到Al(NO3)3、Cu(NO3)2、AgNO3三种物质的混合溶液中,充分反应后过滤,向滤渣中加入稀盐酸,有气泡产生。则滤液中一定含有
A.滤液为浅绿色
B.四种金属的活动性顺序是Al>Fe>Cu>Ag
C.滤渣中一定有Ag、Cu、Fe、Al
D.滤液中一定有Fe2+、Al3+、

您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
名校
解题方法
【推荐2】提起金属材料,你应不会感到陌生。金属材料在生产生活中有广泛的用途,请根据你的生活经验和题目中所提供的信息,分析回答下列问题。

(1)厉害了,我的国!“中国智慧”、“中国制造”誉满全球。首艘由我国自主建造的极地科学考察破冰船“雪龙2号”于2019年上半年交付使用,执行我国极地考察任务。如图是“雪龙2号”,请回答相关问题。
①船体表面涂有红色防护漆,其防锈原理是_______ 。
②船舱内的灯是用铜导线连接的LED灯,主要是利用铜的_______ 性。
③制造船舶所需的大量钢铁是以铁矿石为主要原料冶炼而得。写出工业上用赤铁矿炼铁的化学方程式_______ 。
(2)镁是一种银白色金属,密度为1.74g/cm3,熔点为650℃,沸点为1090℃,质地轻、有延展性。在空气中燃烧时会发出耀眼的白光,放热,生成白色固体。一些烟花和照明弹里都含有镁粉,就是利用了这一性质。镁还能和乙醇、水反应生成氢气。将镁条在酒精灯火焰上点燃,伸入盛有二氧化碳的集气瓶中,会观察到镁条剧烈燃烧,发出强光。反应结束后,可看到生成白色固体氧化镁(MgO),和集气瓶内壁附着黑色固体碳(C)。说明镁能与二氧化碳反应,生成氧化镁和碳,依据文章内容,回答下列问题。
①金属镁的用途有_______ 。
②如果存放在仓库中的少量金属镁发生了火灾,消防官兵可以选用_______ 灭火。
A.沙土 B.二氧化碳 C.水
③将一定量镁粉、锌粉的混合物加入到适量硝酸亚铁和硝酸银的混合溶液中,充分反应后,过滤,得到滤渣和滤液,下列说法正确的是_______ (填序号)。
A.滤液中一定有硝酸镁,滤渣中一定有银
B.若滤液为无色,则滤渣中一定有锌
C.取少量滤液,加入氯化钠溶液,无明显现象,则滤渣中一定有铁
D.取少量滤渣,加入过量稀盐酸,产生气泡,则滤渣的组成有3种情况

(1)厉害了,我的国!“中国智慧”、“中国制造”誉满全球。首艘由我国自主建造的极地科学考察破冰船“雪龙2号”于2019年上半年交付使用,执行我国极地考察任务。如图是“雪龙2号”,请回答相关问题。
①船体表面涂有红色防护漆,其防锈原理是
②船舱内的灯是用铜导线连接的LED灯,主要是利用铜的
③制造船舶所需的大量钢铁是以铁矿石为主要原料冶炼而得。写出工业上用赤铁矿炼铁的化学方程式
(2)镁是一种银白色金属,密度为1.74g/cm3,熔点为650℃,沸点为1090℃,质地轻、有延展性。在空气中燃烧时会发出耀眼的白光,放热,生成白色固体。一些烟花和照明弹里都含有镁粉,就是利用了这一性质。镁还能和乙醇、水反应生成氢气。将镁条在酒精灯火焰上点燃,伸入盛有二氧化碳的集气瓶中,会观察到镁条剧烈燃烧,发出强光。反应结束后,可看到生成白色固体氧化镁(MgO),和集气瓶内壁附着黑色固体碳(C)。说明镁能与二氧化碳反应,生成氧化镁和碳,依据文章内容,回答下列问题。
①金属镁的用途有
②如果存放在仓库中的少量金属镁发生了火灾,消防官兵可以选用
A.沙土 B.二氧化碳 C.水
③将一定量镁粉、锌粉的混合物加入到适量硝酸亚铁和硝酸银的混合溶液中,充分反应后,过滤,得到滤渣和滤液,下列说法正确的是
A.滤液中一定有硝酸镁,滤渣中一定有银
B.若滤液为无色,则滤渣中一定有锌
C.取少量滤液,加入氯化钠溶液,无明显现象,则滤渣中一定有铁
D.取少量滤渣,加入过量稀盐酸,产生气泡,则滤渣的组成有3种情况
您最近一年使用:0次
填空与简答-推断题
|
较难
(0.4)
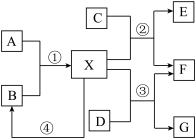
【推荐3】固体X是应用最广泛的金属。小组同学围绕X的冶炼及其合理利用,设计了如图所示的转化关系图(部分反应物、生成物和反应条件已略去)。A~I为初中化学常见物质,其中A是一种单质,E是紫红色固体。请回答下列问题:___________ 。
(2)反应②的基本反应类型为___________ 。
(3)反应③的化学方程式为___________ (写出一个即可)。
(4)反应④可造成X资源的浪费,生活中减少反应④发生的一种措施为___________ 。
(2)反应②的基本反应类型为
(3)反应③的化学方程式为
(4)反应④可造成X资源的浪费,生活中减少反应④发生的一种措施为
您最近一年使用:0次



