为了探究皮蛋中的化学知识,同学们找来一包皮蛋加工配料,经过查找资料得知皮蛋加工配料的主要成分是氧化钙、纯碱和食盐.为了验证皮蛋加工配料的主要成分,他们进行了如下实验:
取少量配料于小烧杯中,并向其中加入足量的水,搅拌、静置、过滤.过滤后得到的白色固体为_____ .它们在水中发生反应的化学方程式为_____ .滤液中一定存在的溶质是_____ ,如果反应物没有恰好完全反应,滤液中还可能存在的溶质是_____ 或_____ .
为了进一步确定滤液中可能存在的物质,他们设计了如下实验,请你帮助他们完善:
取少量配料于小烧杯中,并向其中加入足量的水,搅拌、静置、过滤.过滤后得到的白色固体为
为了进一步确定滤液中可能存在的物质,他们设计了如下实验,请你帮助他们完善:
| 实验步骤 | 实验现象 | 实验结论 |
| 取一支试管,倒入少量滤液,往其中滴加稀盐酸 | 若有气泡产生 | |
| 若无气泡产生 |
更新时间:2019-06-24 09:22:52
|
相似题推荐
科学探究题
|
适中
(0.65)
【推荐1】腌制皮蛋的主要原料有:生石灰、纯碱和食盐,某兴趣小组向这三种物质中加入适量水,充分搅拌,过滤,对滤液中溶质的成分进行探究。
小组讨论后一致认为,滤液中的溶质一定含有NaCl和______ (写化学式)。
【提出问题】滤液中还可能含有哪些溶质呢?
【作出猜想】猜想一:Ca(OH)2;猜想二:Na2CO3;猜想三:Ca(OH)2和Na2CO3;
大家都认为猜想三不合理,原因是:______ 。(用化学方程式表示)
【实验探究】同学们设计了3种不同的实验方案如下:
【交流讨论】同学们一致认为,实验三得出结论不严密,原因是______ 。有些同学往实验一中滴加稀盐酸后,却没有观察到明显现象,对此深感疑惑,经老师的指导和大家的认真思考后,终于找出了没有观察到明显现象的原因是______ 。
小组讨论后一致认为,滤液中的溶质一定含有NaCl和
【提出问题】滤液中还可能含有哪些溶质呢?
【作出猜想】猜想一:Ca(OH)2;猜想二:Na2CO3;猜想三:Ca(OH)2和Na2CO3;
大家都认为猜想三不合理,原因是:
【实验探究】同学们设计了3种不同的实验方案如下:
| 实验操作 | 实验现象 | 实验结论 |
| 实验一:取少量滤液于试管中,滴加足量的稀盐酸 | 猜想二正确 | |
| 实验二:取少量滤液于试管中,滴加 | 产生白色沉淀 | 猜想二正确 |
| 实验三:取少量滤液于试管中,滴加Na2CO3溶液 | 无明显现象 | 猜想二正确 |
【交流讨论】同学们一致认为,实验三得出结论不严密,原因是
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐2】红枣包装中常使用一种袋装防腐剂,品名为“504双吸剂”,其标签如图所示。同学们对一包久置的“504双吸剂”固体样品很好奇,设计实验进行探究。

【提出问题】久置固体的成分是什么?
【查阅资料】铁与氯化铁溶液在常温下发生反应生成氯化亚铁。
【作出猜想】久置固体中可能含有Fe、Fe2O3、CaO、Ca(OH)2、CaCO3。
【实验探究1】甲同学的方案:
【实验质疑】
(1)乙同学认为甲同学的实验中不能得出一定含Ca(OH)2的结论,理由是_________ 。
(2)丙同学认为甲同学的实验并不能得出一定不含Fe₂O3的结论,理由是_________ 。
【实验探究2】乙、丙同学设计如下实验方案继续验证:

(1)乙、丙同学实验中又能得出固体样品中一定还含有_______ ,仍有一种物质不能确定,该物质是_______ 。
(2)乙、丙同学又经过实验测得上述3.9g残留固体中含钙物质的总质量为2.3g,滤渣B中CaCO3的质量为1.0g,滤渣C的质量为2.0g。
【实验结论】综合上述实验及所给数据:
(1)判断久置固体的成分是_______ 。
(2)计算上述残留固体中氧化钙的质量的质量为______ 克。

【提出问题】久置固体的成分是什么?
【查阅资料】铁与氯化铁溶液在常温下发生反应生成氯化亚铁。
【作出猜想】久置固体中可能含有Fe、Fe2O3、CaO、Ca(OH)2、CaCO3。
【实验探究1】甲同学的方案:
| 实验操作 | 实验现象 | 实验结论 |
| (1)取少量固体于试管中,溶解,静置后取上层清液滴加无色酚酞溶液 | 固体溶解时试管外壁发烫,试管底部有不溶物,溶液变红 | 固体中一定含 |
| (2)另取少量固体于试管中,滴加足量的 | 固体逐渐消失,有大量无色气体产生,得到浅绿色溶液 | 固体中一定含有 |
| (3)将步骤(2)中产生的气体通入到澄清的石灰水中 | 固体中一定含有CaCO3 |
【实验质疑】
(1)乙同学认为甲同学的实验中不能得出一定含Ca(OH)2的结论,理由是
(2)丙同学认为甲同学的实验并不能得出一定不含Fe₂O3的结论,理由是
【实验探究2】乙、丙同学设计如下实验方案继续验证:

(1)乙、丙同学实验中又能得出固体样品中一定还含有
(2)乙、丙同学又经过实验测得上述3.9g残留固体中含钙物质的总质量为2.3g,滤渣B中CaCO3的质量为1.0g,滤渣C的质量为2.0g。
【实验结论】综合上述实验及所给数据:
(1)判断久置固体的成分是
(2)计算上述残留固体中氧化钙的质量的质量为
您最近一年使用:0次
【推荐3】某实验小组的同学对某食品包装袋中一个写有“生石灰干燥剂,请勿食用”的小纸袋产生兴趣。
【提出问题】(1)该干燥剂是否还具有干燥能力?请设计实验证明(写出实验步骤、现象及结论):_______________ 。
(2)干燥剂中加水充分溶解后的白色固体是什么物质?
【进行猜想】 甲同学认为可能是Ca(OH)2,乙同学认为可能是CaCO3;
你认为可能是________________ 。
【实验探究】请设计实验证明你的猜想。请你完成实验,填写以下表格:
通过以上探究,最后确定你的猜想是正确的。
【反思与拓展】白色固体中碳酸钙形成的原因(写化学方程式)_____________ 。
【提出问题】(1)该干燥剂是否还具有干燥能力?请设计实验证明(写出实验步骤、现象及结论):
(2)干燥剂中加水充分溶解后的白色固体是什么物质?
【进行猜想】 甲同学认为可能是Ca(OH)2,乙同学认为可能是CaCO3;
你认为可能是
【实验探究】请设计实验证明你的猜想。请你完成实验,填写以下表格:
| 实验步骤 | 实验现象 | 实验结论 |
| 取适量白色固体于烧杯中加水后搅拌、溶解、静置。取上层清夜于试管中滴入适量 | ||
| ②取下层不溶物于试管中,加入足量 | 白色固体中有CaCO3, |
通过以上探究,最后确定你的猜想是正确的。
【反思与拓展】白色固体中碳酸钙形成的原因(写化学方程式)
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐1】“氧泡泡”系列产品去污能力强、绿色环保,其主要成分是过碳酸钠(2Na2CO3·3H2O2)。某化学活动小组对过碳酸钠产生了浓厚的兴趣,决定对其进行探究。
【查阅资料】
Ⅰ.过碳酸钠在水中易离解成Na2CO3和H2O2,其水溶液具有Na2CO3和H2O2的双重性质;
Ⅱ.过碳酸钠与盐酸反应:2(2Na2CO3∙3H2O2)+8HCl=8NaCl+4CO2↑+3O2↑+10H2O;
Ⅲ.过碳酸钠的去污能力主要与其在反应中释放出的“活性氧”有关,“活性氧”含量越高,去污能力越强。
(1)20℃时测得1%过碳酸钠水溶液的pH为10.5,说明其溶液呈_______ (选填“酸性”、“碱性”或“中性”)。
(2)向过碳酸钠水溶液中加入少量MnO2时产生大量气泡,发生反应的化学方程式是_______ 。
(3)为测定某“氧泡泡”样品中“活性氧”的含量,取20g样品按如图实验装置与足量盐酸反应。
(已知样品中杂质不溶于水且不与盐酸反应,装置气密性良好)。

①将盐酸慢慢地滴入A中,反应一段时间后,观察到_______ 时,停止滴加盐酸。
②装置B可吸收生成的CO2,该反应的化学方程式是_______ 。
③甲同学想用C与D装置收集氧气并测量O2的体积,则B装置需连接C装置的_______ 端(填“a”或“b”),若想得出生成氧气的质量,除要记录量筒内液体的读数外,还需要知道的数据是该实验条件下 _______ 。
④如图所示,将反应后A中所得溶液过滤、蒸发、结晶、烘干,称得固体质量为11.7g,乙同学据此计算出该过碳酸钠样品的“活性氧”含量_______ 。(提示:过碳酸钠样品中“活性氧”含量可按如下公式计算;“活性氧”含量=样品与足量盐酸反应生成的氧气质量÷样品质量×100%)。
⑤完成上述探究后,丙同学提出:称量反应前后装置B的质量,其质量差就是反应生成CO2的质量,据此可计算出样品中“活性氧”含量。但丁同学认为该方案不合理,丁同学的理由是_____ (填写一条即可)。
【查阅资料】
Ⅰ.过碳酸钠在水中易离解成Na2CO3和H2O2,其水溶液具有Na2CO3和H2O2的双重性质;
Ⅱ.过碳酸钠与盐酸反应:2(2Na2CO3∙3H2O2)+8HCl=8NaCl+4CO2↑+3O2↑+10H2O;
Ⅲ.过碳酸钠的去污能力主要与其在反应中释放出的“活性氧”有关,“活性氧”含量越高,去污能力越强。
(1)20℃时测得1%过碳酸钠水溶液的pH为10.5,说明其溶液呈
(2)向过碳酸钠水溶液中加入少量MnO2时产生大量气泡,发生反应的化学方程式是
(3)为测定某“氧泡泡”样品中“活性氧”的含量,取20g样品按如图实验装置与足量盐酸反应。
(已知样品中杂质不溶于水且不与盐酸反应,装置气密性良好)。

①将盐酸慢慢地滴入A中,反应一段时间后,观察到
②装置B可吸收生成的CO2,该反应的化学方程式是
③甲同学想用C与D装置收集氧气并测量O2的体积,则B装置需连接C装置的
④如图所示,将反应后A中所得溶液过滤、蒸发、结晶、烘干,称得固体质量为11.7g,乙同学据此计算出该过碳酸钠样品的“活性氧”含量
⑤完成上述探究后,丙同学提出:称量反应前后装置B的质量,其质量差就是反应生成CO2的质量,据此可计算出样品中“活性氧”含量。但丁同学认为该方案不合理,丁同学的理由是
您最近一年使用:0次
科学探究题
|
适中
(0.65)
名校
【推荐2】某同学欲探究 “双钙防蛀”牙膏、“皓清”牙膏和牙粉的主要成分。
【查阅资料】(1)牙膏和牙粉均是由摩擦剂、活性剂、香料等成分构成。
(2)常用的摩擦剂有极细颗粒的碳酸钙(CaCO3) 和水合硅酸(SiO2·nH2O)等。
(3)牙膏和牙粉中除了碳酸钙以外,其它物质均不与稀盐酸反应产生气体。
【实验一】探究“两种牙膏和牙粉中是否都含有碳酸钙?
实验结论:__________ 。
碳酸钙与x稀溶液反应的化学方程式为___________ 。
【实验二】比较样品中碳酸钙的含量
实验结论:_____________________
步骤③的作用是:_________________ 。
【反思】
(1)若不改动原有装置和基本步骤,要测定牙粉中碳酸钙的质量分数,还应测定的数据有:_____ 。
(2)小美认为这样测得的数据计算结果会产生较大的误差,试分析产生的误差是______ (填“偏大”、“偏小”或“没有”)。原因是_______ (如你认为没有误差本空不填)。
(3)小明认为该实验前不需要测定装置的气密性,请你说明其原因________ 。
【查阅资料】(1)牙膏和牙粉均是由摩擦剂、活性剂、香料等成分构成。
(2)常用的摩擦剂有极细颗粒的碳酸钙(CaCO3) 和水合硅酸(SiO2·nH2O)等。
(3)牙膏和牙粉中除了碳酸钙以外,其它物质均不与稀盐酸反应产生气体。
【实验一】探究“两种牙膏和牙粉中是否都含有碳酸钙?
| 步骤 | 实验操作 | 实验现象 |
| ① | 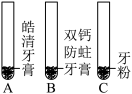 如图所示,取三只试管分别加入适量待测样品,再分别加入适量x稀溶液。x稀溶液是 | A试管中无明显变化, B和C试管中有无色气体生成。 |
| ② | 将B和C试管中生成的无色气体通入 | 现象Ⅱ: |
碳酸钙与x稀溶液反应的化学方程式为
【实验二】比较样品中碳酸钙的含量
| 步骤 | 实验操作 | 实验现象 |
| ① | 组装两套如图装置进行实验。分别取(操作Ⅰ),放于锥形瓶中。并在分液漏斗中分别加入等质量的x稀溶液。 | |
| ② | 打开分液漏斗注入一定量x稀溶液,然后关闭活塞。 | 有气泡产生。 |
| ③ | 待②反应结束后,再打开分液漏斗,注入一定量x稀溶液,然后关闭活塞。 | 无明显现象 |
| ④ | 称量反应后装置及药品的总质量并加以比较 | 加入“双钙防蛀”牙膏的装置及药品的总质量大于加入牙粉的装置及药品的总质量 |
步骤③的作用是:
【反思】
(1)若不改动原有装置和基本步骤,要测定牙粉中碳酸钙的质量分数,还应测定的数据有:
(2)小美认为这样测得的数据计算结果会产生较大的误差,试分析产生的误差是
(3)小明认为该实验前不需要测定装置的气密性,请你说明其原因
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐3】某兴趣小组同学准备进行常见酸、碱、盐性质实验时,发现实验台上有一瓶失去瓶塞并且标签破损的液体药品(如图),于是决定对这瓶溶液的成分进行实验探究:

【提出问题】这瓶溶液是什么溶液?
【获得信息】酸、碱、盐的性质实验中用到含钠元素的物质是氯化钠、氢氧化钠、碳酸钠。
【提出猜想】这瓶溶液可能是:
①氯化钠溶液; ②氢氧化钠溶液; ③碳酸钠溶液。
【实验推断】
(3)小青认为上述实验(2)的结论不完全正确,小组同学讨论后一致认为还需要进行如下实验:另取样于试管中,加入过量的中性CaCl2溶液,观察到有白色沉淀产生,设计这一步骤的目的是_______________ ;静置后,取上层清液,滴入酚酞试液,溶液呈红色。
【实验结论】这瓶溶液原来是____________ 。

【提出问题】这瓶溶液是什么溶液?
【获得信息】酸、碱、盐的性质实验中用到含钠元素的物质是氯化钠、氢氧化钠、碳酸钠。
【提出猜想】这瓶溶液可能是:
①氯化钠溶液; ②氢氧化钠溶液; ③碳酸钠溶液。
【实验推断】
| 实验 | 实验操作 | 实验现象 | 实验结论和解释 |
| (1) | 取样于试管中,滴加无色酚酞试液。 | 溶液呈红色 | 该溶液不可能是 理由是 |
| (2) | 另取样于试管中,滴加足量稀盐酸。 | 该溶液为碳酸钠溶液 |
【实验结论】这瓶溶液原来是
您最近一年使用:0次



