如图所示为某些化肥制备的转化关系。A为空气,B为无色液体,是大理石的主要成分,C、F、H、J为气体,且H有刺激性气味。请根据图示回答问题:
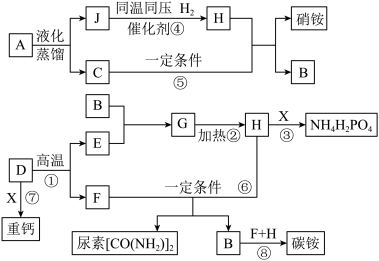
(1)反应②的化学方程式为_______________ 。由此反应可知,在农业生产中施用铵态氮肥时应注意___________ 。
(2)H的化学式为____________ ,反应④的化学反应基本类型是______________ 。
(3)反应⑤的化学方程式为___________________ 。由于该反应合成的硝铵猛烈撞击易爆炸,在使用时应避免____________ 。
(4)自然界中普遍存在着F转化为C的反应,名称为____________ ;工业生产中用反应⑥合成尿素,用反应⑧合成碳铵,60kg的尿素与____________ kg的碳铵肥效相当。
(5)试剂X的化学式是____________ ,图示中属于复合肥料的化学式是____________ ,反应⑦的化学方程式为______________ 。
(6)某庄稼呈比较明显的缺少氮、磷两种元素的症状。从化肥的功效和价格(见下表)等方面综合考虑,你认为应该购买的化肥是____________ (填化学式)。

(1)反应②的化学方程式为
(2)H的化学式为
(3)反应⑤的化学方程式为
(4)自然界中普遍存在着F转化为C的反应,名称为
(5)试剂X的化学式是
(6)某庄稼呈比较明显的缺少氮、磷两种元素的症状。从化肥的功效和价格(见下表)等方面综合考虑,你认为应该购买的化肥是
| 化肥 | 尿素 | 碳铵 | 磷矿粉 | 一铵 | 重钙 |
| 价格/(元/吨) | 1200 | 500 | 500 | 1700 | 700 |
更新时间:2019/08/26 10:46:51
|
相似题推荐
综合应用题
|
困难
(0.15)
解题方法
【推荐1】石灰石是重要的化工原料。为研究石灰石的性质和用途进行如下探究。
Ⅰ.石灰石分解的探究
取三块形状大小相近的石灰石、一块不加热,另两块分别在酒精灯和酒精喷灯的火焰上加热2min(假设杂质加热时不发生变化)。探究过程如图所示,实验现象见表1。
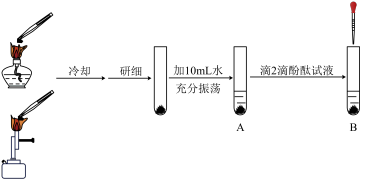
表1不同条件下的实验现象
(1)通过甲、乙、丙三组对比实验,得出影响石灰石分解的因素是_____ 。
(2)丙组实验加热石灰石时,在火焰上方倒扣一个用澄清石灰水润湿的烧杯,石灰水变浑浊,出现浑浊的化学方程式为_____ 。此实验能否推断石灰石煅烧产生二氧化碳,并说明理由:_____ 。
(3)丙组实验中,向试管B中逐滴滴入稀盐酸,至红色恰好褪去。若轻轻晃动试管,溶液自下而上又变为红色,其原因_____ 。
(4)为检验丙组实验中的石灰石部分分解,设计实验与预期现象:取研细后的粉末少许于试管中,_____ 。
Ⅱ.石灰石煅烧温度的探究
某研究小组在电炉内煅烧石灰石样品,并测定煅烧产物(CaO)的活性度,数据见表2。
表2不同等件下煅绕产物的活性度(mL)
(5)石灰石煅绕的最佳温度范围为1100~1200℃的证据是_____ 。
Ⅲ.石灰石用途的探究
(6)“超越者”学习小组探究稀盐酸与石灰石反应后的混合溶液成分,进行了如下实验:
①配制溶液:配制溶质质量分数为5.3%的 溶液。
溶液。
②实验探究:取混合溶液40g置于烧杯中,加入(1)中配制好的5.3% 溶液,产生沉淀的质量与加入
溶液,产生沉淀的质量与加入 溶液的质量关系如图所示。混合液中
溶液的质量关系如图所示。混合液中 的溶质质量分数
的溶质质量分数_____ 。
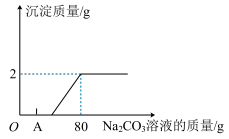
③将图中A点的溶液中和液面上方存在的微观粒子的种类在上图中补充完整;(粒子数目不作要求,不考虑空气、水)_____ 。

Ⅰ.石灰石分解的探究
取三块形状大小相近的石灰石、一块不加热,另两块分别在酒精灯和酒精喷灯的火焰上加热2min(假设杂质加热时不发生变化)。探究过程如图所示,实验现象见表1。

表1不同条件下的实验现象
| 实验组别 | 实验条件 | 试管B中的现象 |
| 甲 | 未加热 | 无明显现象 |
| 乙 | 酒精灯加热 | 呈浅红色 |
| 丙 | 酒精喷灯加热 | 呈红色 |
(2)丙组实验加热石灰石时,在火焰上方倒扣一个用澄清石灰水润湿的烧杯,石灰水变浑浊,出现浑浊的化学方程式为
(3)丙组实验中,向试管B中逐滴滴入稀盐酸,至红色恰好褪去。若轻轻晃动试管,溶液自下而上又变为红色,其原因
(4)为检验丙组实验中的石灰石部分分解,设计实验与预期现象:取研细后的粉末少许于试管中,
Ⅱ.石灰石煅烧温度的探究
某研究小组在电炉内煅烧石灰石样品,并测定煅烧产物(CaO)的活性度,数据见表2。
表2不同等件下煅绕产物的活性度(mL)
| 煅烧时间/活性度/燃烧温度 | 1050℃ | 1100℃ | 1150℃ | 1200℃ | 1250℃ | 1300℃ |
| 12min | 790 | 836 | 868 | 808 | 454 | 412 |
| 16min | 793 | 856 | 871 | 845 | 556 | 530 |
| 20min | 795 | 863 | 873 | 864 | 617 | 623 |
Ⅲ.石灰石用途的探究
(6)“超越者”学习小组探究稀盐酸与石灰石反应后的混合溶液成分,进行了如下实验:
①配制溶液:配制溶质质量分数为5.3%的
 溶液。
溶液。②实验探究:取混合溶液40g置于烧杯中,加入(1)中配制好的5.3%
 溶液,产生沉淀的质量与加入
溶液,产生沉淀的质量与加入 溶液的质量关系如图所示。混合液中
溶液的质量关系如图所示。混合液中 的溶质质量分数
的溶质质量分数
③将图中A点的溶液中和液面上方存在的微观粒子的种类在上图中补充完整;(粒子数目不作要求,不考虑空气、水)

您最近一年使用:0次
综合应用题
|
困难
(0.15)
解题方法
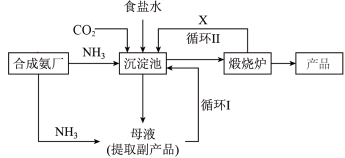
【推荐2】我国化学家侯德榜发明的“侯氏制碱法”联合工业生产纯碱和氮肥,工艺流程图如图。
(1)精盐的获得。
食盐是海水通过淡化处理后被使用。常用的海水淡化方法有蒸馏法和反渗透法等。
利用太阳能蒸馏淡化海水是一种节能的方法,其原理如图所示。
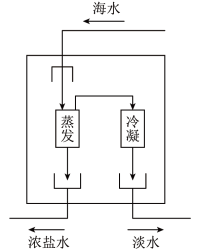
蒸馏法过程为:海水 水蒸气
水蒸气 淡水。
淡水。
①从能量角度看,a过程需要_______ (填“吸收”或“放出”)热量:
②从微观角度看,b过程中发生的改变是_______ (具体描述)。
(2)纯碱的获得
①使用原料氯化钠的利用率从70%提高到90%以上,主要是设计了_______ (填“循环Ⅰ”或“循环Ⅱ”),流程中物质X为_______ (填化学式)。
②在实验过程中,需要控制装置的温度在30℃~35℃,宜采取的方法是_______ 。其温度不能过高也不能过低原因是:_______ 。
(3)某校化学兴趣小组的同学根据Na2CO3和NaHCO3的性质进行了一系列探究。
【查阅资料】
①溶解度比较:
②已知碳酸氢钠在270℃左右就能分解而碳酸钠受热不分解。
③常温下,浓度相同的Na2CO3溶液比NaHCO3溶液的碱性强。
【探究一】NaHCO3和Na2CO3性质差异的探究。
①验证水溶液的酸碱性的差异:分别测两种物质等浓度溶液的pH,测定结果:NaHCO3溶液的pH__ (填“>”或“<”)Na2CO3溶液。
②利用溶解度的差异鉴别NaHCO3和Na2CO3:小方同学分别取xg两种固体粉末加入20℃10g水中充分溶解,通过观察现象区分出碳酸钠和碳酸氢钠,x可能是_____ 。
A.2 B.0.96 C.0.5 D.3
【探究二】测定某NaHCO3和Na2CO3混合物中NaHCO3的质量分数利用如图装置进行实验,装置B中放有样品(整套装置气密性良好,各装置中气体吸收剂足量)。
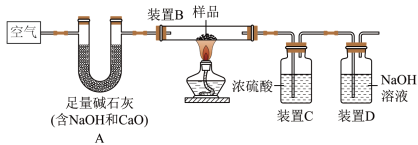
【实验步骤】
①检查装置的气密性;②称取样品10g,加到装置B中;③称量装置B、D的质量(含药品);④连接装置;⑤加热;⑥停止加热继续通入空气;⑦再次称量装置B、D的质量(含药品)。
【数据记录】
【问题讨论】
①B装置中盛样品的仪器名称是_______ 。
②写出装置A中可能发生复分解反应的的化学方程式:_______ 。
【数据分析】③选择合适的数据进行计算NaHCO3和Na2CO3混合物中NaHCO3的质量分数是_____ ?
【拓展应用】④固体Na2CO3中混有少量NaHCO3,可通过_______ 的方法除去。

(1)精盐的获得。
食盐是海水通过淡化处理后被使用。常用的海水淡化方法有蒸馏法和反渗透法等。
利用太阳能蒸馏淡化海水是一种节能的方法,其原理如图所示。

蒸馏法过程为:海水
 水蒸气
水蒸气 淡水。
淡水。①从能量角度看,a过程需要
②从微观角度看,b过程中发生的改变是
(2)纯碱的获得
①使用原料氯化钠的利用率从70%提高到90%以上,主要是设计了
②在实验过程中,需要控制装置的温度在30℃~35℃,宜采取的方法是
(3)某校化学兴趣小组的同学根据Na2CO3和NaHCO3的性质进行了一系列探究。
【查阅资料】
①溶解度比较:
| 溶解度 | 10℃ | 20℃ | 30℃ | 40℃ |
| Na2CO3 | 12.5g | 21.5g | 39.7g | 49.0g |
| NaHCO3 | 8.1g | 9.6g | 11.1g | 12.7g |
③常温下,浓度相同的Na2CO3溶液比NaHCO3溶液的碱性强。
【探究一】NaHCO3和Na2CO3性质差异的探究。
①验证水溶液的酸碱性的差异:分别测两种物质等浓度溶液的pH,测定结果:NaHCO3溶液的pH
②利用溶解度的差异鉴别NaHCO3和Na2CO3:小方同学分别取xg两种固体粉末加入20℃10g水中充分溶解,通过观察现象区分出碳酸钠和碳酸氢钠,x可能是
A.2 B.0.96 C.0.5 D.3
【探究二】测定某NaHCO3和Na2CO3混合物中NaHCO3的质量分数利用如图装置进行实验,装置B中放有样品(整套装置气密性良好,各装置中气体吸收剂足量)。

【实验步骤】
①检查装置的气密性;②称取样品10g,加到装置B中;③称量装置B、D的质量(含药品);④连接装置;⑤加热;⑥停止加热继续通入空气;⑦再次称量装置B、D的质量(含药品)。
【数据记录】
| 装置B | 装置D | |
| 实验前物质的质量/g | 180.0 | 122.2 |
| 实验后物质的质量/g | 176.9 | 124.4 |
①B装置中盛样品的仪器名称是
②写出装置A中可能发生复分解反应的的化学方程式:
【数据分析】③选择合适的数据进行计算NaHCO3和Na2CO3混合物中NaHCO3的质量分数是
【拓展应用】④固体Na2CO3中混有少量NaHCO3,可通过
您最近一年使用:0次
综合应用题
|
困难
(0.15)
名校
解题方法
【推荐3】化学是以实验为基础的科学,实验是科学探究的重要手段。
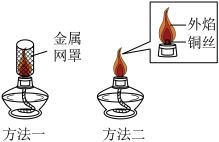
Ⅰ. 酒精广泛应用于生产、生活等多个领域。实验室常用酒精灯作为加热仪器,对酒精灯适当改进,可提高其火焰的温度,以下是两种改进方法的示意图。
(1)对比分析;方法一添加金属网罩的目的是______ ;方法二将铜丝的两端插入酒精灯的灯芯处,从燃烧条件上看,插入铜丝的作用是_______ 。______ 。
Ⅱ.叠氮化钠(NaN3)被广泛应用于汽车安全气囊,某兴趣小组对其进行下列研究。
应用研究:
(3)汽车经撞击后,30毫秒内引发NaN3,迅速分解为Na、N2,反应方程式为_______ 。
制备研究:
(4)将金属钠与液态氨反应得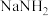 ,再将
,再将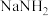 与
与 反应可生成
反应可生成 、NaOH和气体X,该反应的化学方程式为
、NaOH和气体X,该反应的化学方程式为 ,实验室检验X气体使用的试纸是湿润的
,实验室检验X气体使用的试纸是湿润的_____ 。Na2CO3质量分数测定:工业级NaN3中常含有少量的Na2CO3,为测定样品中Na2CO3的质量分数设计如图装置(已知 溶液与
溶液与 ,反应不生成气体)。
,反应不生成气体)。_______ 。设计的实验步骤为:①精确称量样品,检查装置气密性;②打开弹簧夹,鼓入空气,称量装置C;③关闭弹簧夹,打开分液漏斗活塞;④再打开弹簧夹,_______ ;⑤再次称量装置C,计算碳酸钠含量至少需要测定_______ (填数字)个数据。根据制备反应,分析工业级 中含有
中含有 的可能原因
的可能原因_______ 。
 纯度测定:精确称量0.14g
纯度测定:精确称量0.14g 样品,设计如图装置,测定其纯度,已知2NaN3→3N2中的N全部转化为N2,其他产物略),反应中放出大量的热。
样品,设计如图装置,测定其纯度,已知2NaN3→3N2中的N全部转化为N2,其他产物略),反应中放出大量的热。_______ (填“变大”、“变小”或“不变”),说明气密性良好。
(7)使小试管中的NaN3样品与M溶液接触的操作是_________ 。
(8)使用冷水冷凝的目的是_______ 。反应前应将液面调节到量气管的“0”刻度并使两边液面相平,反应后读数时,还需要进行的操作是_______ 。
(9)常温下测得量气管读数为67.2mL(N2的密度为1.25g/L),则实验中选用的量气管规格合适的是________(填字母序号)。
(10)计算NaN3样品的纯度______ 。
Ⅰ. 酒精广泛应用于生产、生活等多个领域。实验室常用酒精灯作为加热仪器,对酒精灯适当改进,可提高其火焰的温度,以下是两种改进方法的示意图。
(1)对比分析;方法一添加金属网罩的目的是
Ⅱ.叠氮化钠(NaN3)被广泛应用于汽车安全气囊,某兴趣小组对其进行下列研究。
应用研究:
(3)汽车经撞击后,30毫秒内引发NaN3,迅速分解为Na、N2,反应方程式为
制备研究:
(4)将金属钠与液态氨反应得
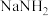 ,再将
,再将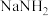 与
与 反应可生成
反应可生成 、NaOH和气体X,该反应的化学方程式为
、NaOH和气体X,该反应的化学方程式为 ,实验室检验X气体使用的试纸是湿润的
,实验室检验X气体使用的试纸是湿润的 溶液与
溶液与 ,反应不生成气体)。
,反应不生成气体)。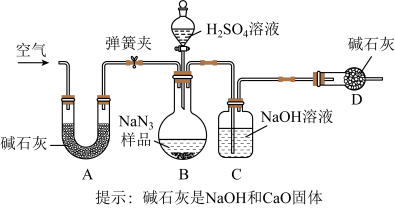
 中含有
中含有 的可能原因
的可能原因 纯度测定:精确称量0.14g
纯度测定:精确称量0.14g 样品,设计如图装置,测定其纯度,已知2NaN3→3N2中的N全部转化为N2,其他产物略),反应中放出大量的热。
样品,设计如图装置,测定其纯度,已知2NaN3→3N2中的N全部转化为N2,其他产物略),反应中放出大量的热。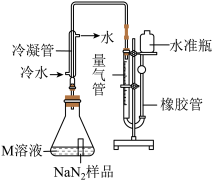
(7)使小试管中的NaN3样品与M溶液接触的操作是
(8)使用冷水冷凝的目的是
(9)常温下测得量气管读数为67.2mL(N2的密度为1.25g/L),则实验中选用的量气管规格合适的是________(填字母序号)。
| A.100mL | B.1L | C.2L |
您最近一年使用:0次
【推荐1】酸碱盐是初中化学学习的重要内容,它们在生活中有重要的用途。
(1)下列物质中一定含有氧元素的是______ (填序号)。
A.酸 B.碱 C.盐 D.有机物
(2)硝酸铵不能与熟石灰混合使用的原因是______ (用化学方程式表示)。
(3)某同学在实验室准备实验用品时,发现实验桌上有瓶敞口放置的NaOH溶液。
【提出问题】这瓶溶液中的溶质是什么?
【猜想与假设】
猜想I:NaOH;
猜想Ⅱ:Na2CO3;
猜想Ⅲ:______ 。
【实验探究】根据表中内容填写相应的实验现象:
【实验反思】①氢氧化钠溶液敞口放置,变质的原因是______ (用化学方程式表示)。
②CaCl2溶液、Ca(NO3)2溶液、Ca(OH)2溶液中不能替代BaCl2溶液进行实验的是______ 。
(4)向一定量的碳酸钠粉末中加入100g稀盐酸(足量),充分反应后,固体全部溶解,溶液的质量增加至106.2g。求碳酸钠粉末的质量______ 。
(1)下列物质中一定含有氧元素的是
A.酸 B.碱 C.盐 D.有机物
(2)硝酸铵不能与熟石灰混合使用的原因是
(3)某同学在实验室准备实验用品时,发现实验桌上有瓶敞口放置的NaOH溶液。
【提出问题】这瓶溶液中的溶质是什么?
【猜想与假设】
猜想I:NaOH;
猜想Ⅱ:Na2CO3;
猜想Ⅲ:
【实验探究】根据表中内容填写相应的实验现象:
| 实验步骤 | 实验现象 | 实验结论 |
| ①取少量BaCl2溶液,向其中滴加酚酞试液; ②取少量该NaOH溶液样品于试管中,先滴加足量的BaCl2溶液;静置后滴加酚酞试液 | ①无明显现象; ② | 猜想Ⅲ正确 |
②CaCl2溶液、Ca(NO3)2溶液、Ca(OH)2溶液中不能替代BaCl2溶液进行实验的是
(4)向一定量的碳酸钠粉末中加入100g稀盐酸(足量),充分反应后,固体全部溶解,溶液的质量增加至106.2g。求碳酸钠粉末的质量
您最近一年使用:0次
综合应用题
|
困难
(0.15)
解题方法
【推荐1】(1)如图1是元素周期表中的一部分,图2是铜原子的结构示意图。据图回答:
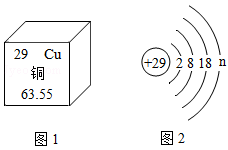
①图2中n的值为____ ;铜元素位于元素周期表中的第____ 周期。
②古代青铜器工艺精湛,但出土的青铜器表面大都锈蚀,锈蚀部分存在CuCl,CuCl的化学名称为________ ,为防止出土的青铜器再锈蚀,文物工作者将糊状Ag2O涂在被腐蚀部位,Ag2O与CuCl发生复分解反应,可以防止青铜器进一步被腐蚀,写出该反应的化学方程式_______ 。某新出土的青铜器通过分析测得Sn、Pb的质量分别为119 g、20.7 g,则该青铜器中Sn和Pb原子的数目之比为__ 。
(2)二氧化氯(ClO2)是一种高效净水剂。以粗盐为原料生产ClO2的工艺主要包括:A. 粗盐精制;B. 特殊条件下电解NaCl溶液制NaClO3;C. ClO2的制取。工艺流程如图。
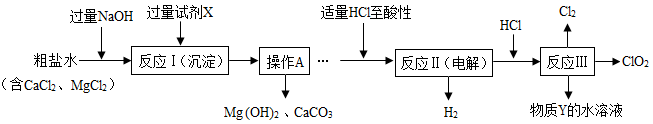
(其中反应Ⅲ制取ClO2的化学方程式为:2NaClO3+4HCl==2ClO2↑+Cl2↑+2NaCl+2H2O)
①试剂X中溶质的化学式为________________ ;操作A名称_____________ 。
②分析完成反应Ⅱ的化学方程式:_______________________________ 。
③我国最近已研究出ClO2的新制法,其反应的微观过程如图所示:
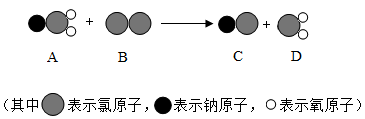
该反应的化学方程式是___________________ ;该反应中,反应物和生成物所属物质类别有________ 类。
(3)下图中A~H是初中化学常见的物质。B是最常用的溶剂,E有很好的抗腐蚀性能;D、E、F、H是四种不同类别的物质,且均含有地壳中含量最高的金属元素;四个虚线圈中的反应各属于四个不同的基本反应类型。图中“—”表示两端的物质间能发生化学反应;“→”表示物质间存在转化关系;反应条件、部分反应物和生成物已略去。
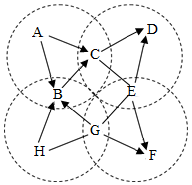
①写出H的化学式:___________ 。
②写出相关的反应的化学方程式:A→C:_____________ ; E—G:______________ 。
③G中一定含有(填元素符号)_______ 元素。

①图2中n的值为
②古代青铜器工艺精湛,但出土的青铜器表面大都锈蚀,锈蚀部分存在CuCl,CuCl的化学名称为
(2)二氧化氯(ClO2)是一种高效净水剂。以粗盐为原料生产ClO2的工艺主要包括:A. 粗盐精制;B. 特殊条件下电解NaCl溶液制NaClO3;C. ClO2的制取。工艺流程如图。

(其中反应Ⅲ制取ClO2的化学方程式为:2NaClO3+4HCl==2ClO2↑+Cl2↑+2NaCl+2H2O)
①试剂X中溶质的化学式为
②分析完成反应Ⅱ的化学方程式:
③我国最近已研究出ClO2的新制法,其反应的微观过程如图所示:

该反应的化学方程式是
(3)下图中A~H是初中化学常见的物质。B是最常用的溶剂,E有很好的抗腐蚀性能;D、E、F、H是四种不同类别的物质,且均含有地壳中含量最高的金属元素;四个虚线圈中的反应各属于四个不同的基本反应类型。图中“—”表示两端的物质间能发生化学反应;“→”表示物质间存在转化关系;反应条件、部分反应物和生成物已略去。

①写出H的化学式:
②写出相关的反应的化学方程式:A→C:
③G中一定含有(填元素符号)
您最近一年使用:0次
综合应用题
|
困难
(0.15)
解题方法
【推荐2】金属的使用是人类社会文明发展的重要标志。金属的冶炼和金属性质的研究是化学研究的重要组成部分。
(1)地壳中含量最丰富的金属元素是______ ;从人类对自然资源利用的技术水平看,人类社会依次经历了石器时代、_____ 、铁器时代:某金属及其合金有很好的抗腐蚀性能,熔点高、密度小,被广泛用于航空航天器和人造关节等的制造,这种金属是______ ;在元素周期表中,有相邻的17种金属元素,被称为“工业的维生素”,它们的性质非常相似,这类金属元素统称为______ 元素。
(2)下列A-G是初中化学中常见的物质,它们之间的转化关系如下图所示(省略了部分反应条件和物质)。其中A→B和D→E需要另加同一种反应物,但该反应物浓度不同:F的稀溶液呈浅绿色,且可与氯化钡溶液反应产生白色沉淀。请回答下列问题:
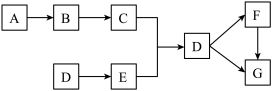
①写出A、D的化学式A________ 。D________ 。
②写出C与E反应生成D的化学方程式________ 。
③写出F转化成G的化学方程式________ 。
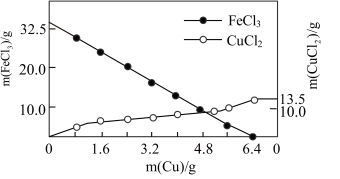
(3)FeCl3溶液常用于印刷电路板的制造,反应原理为: 。向含溶质32.5g的FeCl3溶液中慢慢加入一定量的Cu粉,反应过程中FeCl3、CuCl2的质量随Cu粉质量变化如图所示。则X的化学式为
。向含溶质32.5g的FeCl3溶液中慢慢加入一定量的Cu粉,反应过程中FeCl3、CuCl2的质量随Cu粉质量变化如图所示。则X的化学式为_____ ,方程式中a和b的比为____ ,完全反应后,生成X的质量为_____ g。
(1)地壳中含量最丰富的金属元素是
(2)下列A-G是初中化学中常见的物质,它们之间的转化关系如下图所示(省略了部分反应条件和物质)。其中A→B和D→E需要另加同一种反应物,但该反应物浓度不同:F的稀溶液呈浅绿色,且可与氯化钡溶液反应产生白色沉淀。请回答下列问题:

①写出A、D的化学式A
②写出C与E反应生成D的化学方程式
③写出F转化成G的化学方程式
(3)FeCl3溶液常用于印刷电路板的制造,反应原理为:
 。向含溶质32.5g的FeCl3溶液中慢慢加入一定量的Cu粉,反应过程中FeCl3、CuCl2的质量随Cu粉质量变化如图所示。则X的化学式为
。向含溶质32.5g的FeCl3溶液中慢慢加入一定量的Cu粉,反应过程中FeCl3、CuCl2的质量随Cu粉质量变化如图所示。则X的化学式为
您最近一年使用:0次
综合应用题
|
困难
(0.15)
名校
解题方法
【推荐3】回答下列问题。
(1)某化肥厂以煤、空气、水为原料合成氨,生产流程如图:
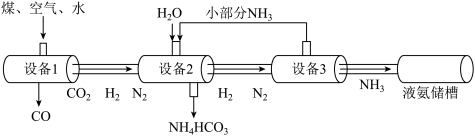
①CO2中碳元素的化合价为________ 。
②设备2中参加反应的物质有______________ 。
③该化肥厂可以生产的肥料有______________ 。
(2)如图是7种常见物质间的反应及转化关系,其中“→”表示转化关系,“一”表示相互反应。已知B、D、E、G是不同类别的物质,物质B是一种红色固体粉末,E、F含有相同的一种元素,请完成下列问题。
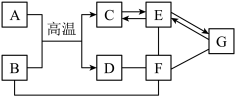
①物质C的化学式为______ ,请写出它的一种用途___________ ;
②写出E→G的化学方程式_______________ ;
③写出D—F反应的实验现象___________ 。
④F—G反应的基本反应类型为_____________ ;
⑤为检验F、G之间恰好完全反应,取反应后的溶液少量于试管中,并使用如下试剂或用品( )
a.铁粉 b.酚酞 c.石蕊 d.pH试纸
(1)某化肥厂以煤、空气、水为原料合成氨,生产流程如图:

①CO2中碳元素的化合价为
②设备2中参加反应的物质有
③该化肥厂可以生产的肥料有
(2)如图是7种常见物质间的反应及转化关系,其中“→”表示转化关系,“一”表示相互反应。已知B、D、E、G是不同类别的物质,物质B是一种红色固体粉末,E、F含有相同的一种元素,请完成下列问题。

①物质C的化学式为
②写出E→G的化学方程式
③写出D—F反应的实验现象
④F—G反应的基本反应类型为
⑤为检验F、G之间恰好完全反应,取反应后的溶液少量于试管中,并使用如下试剂或用品
a.铁粉 b.酚酞 c.石蕊 d.pH试纸
您最近一年使用:0次



