金属材料与人类的生产、生活息息相关。
(1)下列金属制品中,主要利用金属导热性的是_________ (填序号)。

(2)钢铁锈蚀会造成严重的资源浪费,防止或减缓钢铁锈蚀的常用方法有:_________ (写出一条即可)。
(3)“曾青得铁则化为铜”,此即湿法冶铜,这也是世界湿法冶金的先驱。试写出铁和氯化铜溶液反应的化学方程式_____________ ,它属于 _________ 反应(选填“化合”、“分解”、“复分解”、 “置换”之一)。
(4)为了测定某黄铜(铜锌合金)样品的组成,某研究性学习小组称取了该样品20g,向其中逐滴加入9.8%的稀硫酸至刚好不再产生气体为止。反应过程中,生成气体与所用硫酸溶液的质量关系如图所示。
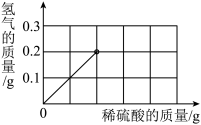
试计算:该黄铜样品中锌的质量_________ ?
(1)下列金属制品中,主要利用金属导热性的是

(2)钢铁锈蚀会造成严重的资源浪费,防止或减缓钢铁锈蚀的常用方法有:
(3)“曾青得铁则化为铜”,此即湿法冶铜,这也是世界湿法冶金的先驱。试写出铁和氯化铜溶液反应的化学方程式
(4)为了测定某黄铜(铜锌合金)样品的组成,某研究性学习小组称取了该样品20g,向其中逐滴加入9.8%的稀硫酸至刚好不再产生气体为止。反应过程中,生成气体与所用硫酸溶液的质量关系如图所示。

试计算:该黄铜样品中锌的质量
更新时间:2019-11-05 11:17:37
|
相似题推荐
综合应用题
|
适中
(0.65)
解题方法
【推荐1】酸、碱、盐是几类重要的化合物,他们之间能发生复分解反应。
(1)复分解反应发生的条件是有沉淀析出、有气体放出或有_____ 生成。
(2)为探究某些酸碱盐之间能否发生反应,进行了如图所示的实验。
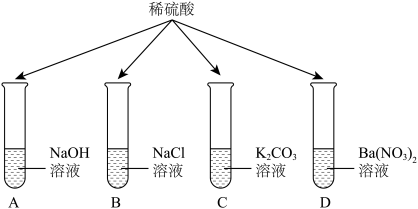
①D试管中的现象是_____ ,另写一个与该反应的微观实质相同的化学方程式_____ 。
②若向试管A中滴入酚酞试液不变色,则证明试管中溶液显_____ 。
③实验结束后,将发生了反应的试管中的所有物质倒入同一烧杯中,充分混合后过滤,得沉淀和滤液。下列说法中不正确的是_____ (填字母)。
A.若倒入烧杯前各试管中发生的反应都是恰好完全反应,则向滤液中滴入紫色石蕊试液不变色
B.若烧杯中有气泡产生,则倒入烧杯前C中溶质可做钾肥
C.若检测滤液的pH为7,则滤液可直接倒入下水道
(3)现有一包NaCl和Na2CO3的混合物20g,加水充分溶解后,加入足量氯化钙溶液,反应结束后称得沉淀的质量为10g,则原混合物中Na2CO3的质量分数为_____ 。
(1)复分解反应发生的条件是有沉淀析出、有气体放出或有
(2)为探究某些酸碱盐之间能否发生反应,进行了如图所示的实验。

①D试管中的现象是
②若向试管A中滴入酚酞试液不变色,则证明试管中溶液显
③实验结束后,将发生了反应的试管中的所有物质倒入同一烧杯中,充分混合后过滤,得沉淀和滤液。下列说法中不正确的是
A.若倒入烧杯前各试管中发生的反应都是恰好完全反应,则向滤液中滴入紫色石蕊试液不变色
B.若烧杯中有气泡产生,则倒入烧杯前C中溶质可做钾肥
C.若检测滤液的pH为7,则滤液可直接倒入下水道
(3)现有一包NaCl和Na2CO3的混合物20g,加水充分溶解后,加入足量氯化钙溶液,反应结束后称得沉淀的质量为10g,则原混合物中Na2CO3的质量分数为
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐2】镁是一种用途广泛的国防金属材料,目前大部分镁都是利用从海水中提取镁盐制得的,工艺流程如下图所示:

请你根据上述材料,回答下列问题:
(1)操作①的名称是_____________ (填“溶解”、“过滤”、“蒸发”之一)。
(2)试剂C中溶质的化学式是_______________ 。
(3)从海水中提取MgCl2时,经历了“MgCl2→Mg(OH)2→MgCl2”的转化过程,请分析这样做的目的是_____________________________ 。
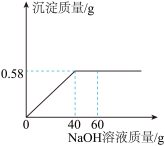
(4)某校化学活动小组在实验室用蒸馏水和氯化镁配制了氯化镁溶液,模仿海水进行氯化镁含量的测定。学习小组的同学取该海水样品190 g,向其中加入氢氧化钠溶液,产生沉淀的质量与所加氢氧化钠溶液质量的关系曲线如图所示。请计算:上述海水样品中氯化镁的溶质质量分数是多少?(精确到0.1%)

请你根据上述材料,回答下列问题:
(1)操作①的名称是
(2)试剂C中溶质的化学式是
(3)从海水中提取MgCl2时,经历了“MgCl2→Mg(OH)2→MgCl2”的转化过程,请分析这样做的目的是
(4)某校化学活动小组在实验室用蒸馏水和氯化镁配制了氯化镁溶液,模仿海水进行氯化镁含量的测定。学习小组的同学取该海水样品190 g,向其中加入氢氧化钠溶液,产生沉淀的质量与所加氢氧化钠溶液质量的关系曲线如图所示。请计算:上述海水样品中氯化镁的溶质质量分数是多少?(精确到0.1%)

您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐3】实验课上,同学们利用下列装置进行气体制备的学习。
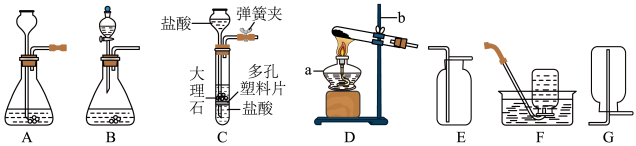
请你用已学的化学知识回答下列问题:
(1)图中仪器a的名称是______ ;仪器b的名称是______ 。
(2)在实验室里常用稀盐酸和块状大理石在装置A中反应制取二氧化碳,不用粉末状大理石的原因是______ ,写出上述反应的化学方程式:______ 。
(3)装置A、B和C都能制取二氧化碳气体,但装置C与前两者相比较,你认为装置C的优势是______ 。
(4)实验室用加热无水乙酸钠固体和氢氧化钠固体制取甲烷气体。在通常情况下甲烷是一种无色无味的气体,难溶于水,密度比空气小。现实验室制取较纯净的甲烷应选用的发生和收集装置是______ 。(填字母编号)
(5)若用装置B制取氢气,原料是锌和稀硫酸,则该反应的化学方程式为______ 。
(6)在实验室用25g大理石与足量的稀盐酸完全反应(杂质不反应),可以生成8.8g的二氧化碳气体,则大理石中碳酸钙的质量分数是多少?

请你用已学的化学知识回答下列问题:
(1)图中仪器a的名称是
(2)在实验室里常用稀盐酸和块状大理石在装置A中反应制取二氧化碳,不用粉末状大理石的原因是
(3)装置A、B和C都能制取二氧化碳气体,但装置C与前两者相比较,你认为装置C的优势是
(4)实验室用加热无水乙酸钠固体和氢氧化钠固体制取甲烷气体。在通常情况下甲烷是一种无色无味的气体,难溶于水,密度比空气小。现实验室制取较纯净的甲烷应选用的发生和收集装置是
(5)若用装置B制取氢气,原料是锌和稀硫酸,则该反应的化学方程式为
(6)在实验室用25g大理石与足量的稀盐酸完全反应(杂质不反应),可以生成8.8g的二氧化碳气体,则大理石中碳酸钙的质量分数是多少?
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐1】金属在生产、生活中有着广泛的用途。
(1)铁可制成铁锅烹调食物,利用了铁的延展性和______ 性。
(2)铁是目前世界上使用最多的金属,生铁的熔点比纯铁的熔点______ (高或低);工业炼铁中焦炭的作用是燃烧提供能量和______ ;
(3)铁制品在潮湿的空气中容易生锈。如图所示是某化学兴趣小组设计的铁钉锈蚀条件的探究实验,要达到实验目的还需补充什么实验?请简要叙述。

(4)实验室可利用如图所示装置模拟工业炼铁。

①写出装置A中硬质玻璃管中反应的化学方程式______ 。
②实验先通一氧化碳后加热的原因是什么?______ 。
③某同学认为该装置还有不足之处,应如何改进?______ 。
(5)某工厂利用废铁屑与废硫酸反应来制取硫酸亚铁。现有废硫酸(其中 的质量为4.9t),与足量的废铁屑起反应,可生产硫酸亚铁的质量是多少?
的质量为4.9t),与足量的废铁屑起反应,可生产硫酸亚铁的质量是多少?
(1)铁可制成铁锅烹调食物,利用了铁的延展性和
(2)铁是目前世界上使用最多的金属,生铁的熔点比纯铁的熔点
(3)铁制品在潮湿的空气中容易生锈。如图所示是某化学兴趣小组设计的铁钉锈蚀条件的探究实验,要达到实验目的还需补充什么实验?请简要叙述。

(4)实验室可利用如图所示装置模拟工业炼铁。

①写出装置A中硬质玻璃管中反应的化学方程式
②实验先通一氧化碳后加热的原因是什么?
③某同学认为该装置还有不足之处,应如何改进?
(5)某工厂利用废铁屑与废硫酸反应来制取硫酸亚铁。现有废硫酸(其中
 的质量为4.9t),与足量的废铁屑起反应,可生产硫酸亚铁的质量是多少?
的质量为4.9t),与足量的废铁屑起反应,可生产硫酸亚铁的质量是多少?
您最近一年使用:0次
综合应用题
|
适中
(0.65)
名校
解题方法
【推荐2】人类的生活和生产都离不开金属材料。
(1)下列用途主要利用金属导电性的是___________(填字母序号)。
(2)下列生活中所用到的材料中,属于金属材料的是___________ (填序号)。
①钢铁 ②氧化铝 ③铝合金
(3)某同学为了验证镁、铁、铜的活动性顺序,他选择了硫酸亚铁溶液,你认为他还需要的另外两种金属是___________ 。请根据选定的试剂写出上述实验中发生反应的一个化学方程式___________ 。
(4)向硝酸银溶液中加入一定质量的锌粉和铜粉的混合物,充分反应后过滤,得到滤渣和滤液。以下推断正确的是___________(填字母)
(5)将8.3g由Al、Zn两种金属组成的混合物加入一定量的稀硫酸中,恰好完全反应,将反应后的溶液小心蒸干,得到无水固体27.5g,则反应中产生氢气的质量为___________ g。
(1)下列用途主要利用金属导电性的是___________(填字母序号)。
| A.铁锅 | B.铜导线 | C.水龙头 |
①钢铁 ②氧化铝 ③铝合金
(3)某同学为了验证镁、铁、铜的活动性顺序,他选择了硫酸亚铁溶液,你认为他还需要的另外两种金属是
(4)向硝酸银溶液中加入一定质量的锌粉和铜粉的混合物,充分反应后过滤,得到滤渣和滤液。以下推断正确的是___________(填字母)
| A.若向滤渣中加入稀盐酸有气泡产生,则滤渣中一定有银、铜、锌 |
| B.若滤液为无色,则滤渣中一定有锌 |
| C.若滤液为蓝色,则滤液中一定有硝酸银、硝酸铜和硝酸锌 |
| D.滤渣的质量一定比反应前锌粉和铜粉混合物质量大 |
您最近一年使用:0次
综合应用题
|
适中
(0.65)
【推荐3】金属材料在国防建设中起着重要的作用,图1为歼一15飞机在辽宁舰上起飞。
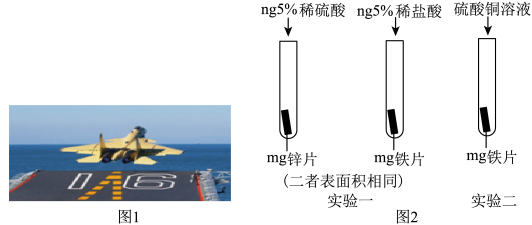

(1)铝合金用于制造飞机的外壳,铝合金材质的主要优点是_______________ 。
(2)钢铁的锈蚀主要是铁与空气中的___________________ 共同作用的结果。
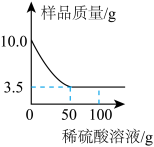
(3)为了避免轮船的钢质外壳被腐蚀,通常在轮船外壳上镶嵌比铁活动性强的金属,小明为探究锌、铁、铜三种金属的活动性顺序,设计了如图2的两个实验:
①实验一中,小明以“金属表面产生气泡的快慢”为标准来判断锌,铁的活动性强弱,有同学认为不够合理,理由是____________________________________________ 。
②实验二中,若出现_______________________ 现象,可证明铁的活动性强于铜。
(4)辽宁舰的建造耗费了大量的钢材,某兴趣小组在实验室用图3所示装置模拟炼铁的化学原理,装置A中生成铁的化学方程式为____________________________ ,装置B中发生反应的化学方程式为________________________________ 。
(5)某化学兴趣小组对某铜锌合金样品进行探究实验。称取样品10.0g,再用100.0g稀硫酸溶液逐滴滴入,实验情况如图所示。求所用稀硫酸溶液中溶质的质量分数。____


(1)铝合金用于制造飞机的外壳,铝合金材质的主要优点是
(2)钢铁的锈蚀主要是铁与空气中的
(3)为了避免轮船的钢质外壳被腐蚀,通常在轮船外壳上镶嵌比铁活动性强的金属,小明为探究锌、铁、铜三种金属的活动性顺序,设计了如图2的两个实验:
①实验一中,小明以“金属表面产生气泡的快慢”为标准来判断锌,铁的活动性强弱,有同学认为不够合理,理由是
②实验二中,若出现
(4)辽宁舰的建造耗费了大量的钢材,某兴趣小组在实验室用图3所示装置模拟炼铁的化学原理,装置A中生成铁的化学方程式为
(5)某化学兴趣小组对某铜锌合金样品进行探究实验。称取样品10.0g,再用100.0g稀硫酸溶液逐滴滴入,实验情况如图所示。求所用稀硫酸溶液中溶质的质量分数。

您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐1】早在春秋战国时期,我国就开始生产和使用铁制品,时至今日,社会快速发展,钢铁仍然是我国使用最多的金属材料,请围绕金属铁开展主题式学习活动。
主题一:铁的性质及应用
(1)铝的抗腐蚀性强于铁,为什么锤子、剪刀等用铁制而不用铝制___________ 。
(2)下列铁制品中,利用了金属导热性的是___________(填字母)。
(3)不能用铁制容器配制农业上使用的波尔多液杀菌剂(成分中含有硫酸铜),原因是___________ (用化学方程式表示)。
主题二:铁的冶炼
【资料卡片】生铁和钢是含碳量不同的两种铁合金,其中生铁含碳量为2%~4.3%,钢含碳量为0.03%~2%。
(4)下图装置可做一氧化碳还原氧化铁的实验,并检验生成的气体产物。请根据下列实验装置图回答问题:___________ ;发生反应的化学方程式为___________ 。
②从环保的角度来看,该装置缺少了什么?请设计方案加以改正___________ 。
主题三:铁的锈蚀和防护
(5)对铁生锈的条件进行探究,设计如图实验装置。___________ 。
②几天之后,只观察到装置C中的铁丝生锈了,说明铁的锈蚀与___________ 有关。
③铁的锈蚀会造成资源浪费,但只要善于利用其原理,也可以将“害”转化为“利”,请举出一个对生活有利的实例:___________ 。
(6)为防止铁的锈蚀,下列采取的措施合理的是___________ (填字母)。
A.为防止学校操场上的健身器材生锈,可在其表面喷漆
B.家中常用的铁锅,使用后洗净擦干,并保持表面洁净干燥
C.化学实验室的铁架台生锈了,保留其表面的铁锈,防止继续生锈
【活动总结】金属资源是自然界为人类提供的宝贵财富,请珍爱我们赖以生存的自然环境。也希望同学们通过不断的学习,今后能在金属的开采、利用及保护等方面为社会作出贡献。
主题一:铁的性质及应用
(1)铝的抗腐蚀性强于铁,为什么锤子、剪刀等用铁制而不用铝制
(2)下列铁制品中,利用了金属导热性的是___________(填字母)。
A.河北沧州铁狮子 | B.不锈钢水壶 | C.铸铁井盖 |
(3)不能用铁制容器配制农业上使用的波尔多液杀菌剂(成分中含有硫酸铜),原因是
主题二:铁的冶炼
【资料卡片】生铁和钢是含碳量不同的两种铁合金,其中生铁含碳量为2%~4.3%,钢含碳量为0.03%~2%。
(4)下图装置可做一氧化碳还原氧化铁的实验,并检验生成的气体产物。请根据下列实验装置图回答问题:

②从环保的角度来看,该装置缺少了什么?请设计方案加以改正
主题三:铁的锈蚀和防护
(5)对铁生锈的条件进行探究,设计如图实验装置。

②几天之后,只观察到装置C中的铁丝生锈了,说明铁的锈蚀与
③铁的锈蚀会造成资源浪费,但只要善于利用其原理,也可以将“害”转化为“利”,请举出一个对生活有利的实例:
(6)为防止铁的锈蚀,下列采取的措施合理的是
A.为防止学校操场上的健身器材生锈,可在其表面喷漆
B.家中常用的铁锅,使用后洗净擦干,并保持表面洁净干燥
C.化学实验室的铁架台生锈了,保留其表面的铁锈,防止继续生锈
【活动总结】金属资源是自然界为人类提供的宝贵财富,请珍爱我们赖以生存的自然环境。也希望同学们通过不断的学习,今后能在金属的开采、利用及保护等方面为社会作出贡献。
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐2】化学与生活密切相关。
(1)煤、石油、天然气属于化石燃料,它们属于___________ (填“可再生”或“不可再生”)能源。
(2)生活中铝制品比铁制品耐腐蚀,原因是___________ ,防止铁制品生锈的方法是___________ (写一种)。
(3)碳﹣氧平衡在自然界中有重要意义,绿色植物进行的___________ 能够吸收CO2,放出O2。
(4)漂白粉是自来水常用的消毒剂,工业上利用氯气与石灰水反应制得,主要成分是次氯酸钙[Ca(ClO)2]和氯化钙,易溶于水,制取漂白粉的工业流程如图:

①步骤中饱和食盐水通电时发生如下反应:2NaCl+2H2O 2X+H2↑+Cl2↑,X的化学式为
2X+H2↑+Cl2↑,X的化学式为___________ 。
②写出步骤Ⅱ高温煅烧石灰石反应的化学方程式:___________ 。
③根据题意可知,步骤Ⅲ加入足量水溶解主要发生的是化学变化,进行操作A时需要用到玻璃仪器有烧杯、玻璃棒、___________ 。
(1)煤、石油、天然气属于化石燃料,它们属于
(2)生活中铝制品比铁制品耐腐蚀,原因是
(3)碳﹣氧平衡在自然界中有重要意义,绿色植物进行的
(4)漂白粉是自来水常用的消毒剂,工业上利用氯气与石灰水反应制得,主要成分是次氯酸钙[Ca(ClO)2]和氯化钙,易溶于水,制取漂白粉的工业流程如图:

①步骤中饱和食盐水通电时发生如下反应:2NaCl+2H2O
 2X+H2↑+Cl2↑,X的化学式为
2X+H2↑+Cl2↑,X的化学式为②写出步骤Ⅱ高温煅烧石灰石反应的化学方程式:
③根据题意可知,步骤Ⅲ加入足量水溶解主要发生的是化学变化,进行操作A时需要用到玻璃仪器有烧杯、玻璃棒、
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐3】铁及其化合物在生产生活中有广泛的应用。
一、铁的应用和防护
(1)铁锈主要成分是Fe2O3·nH2O,铁生锈主要与空气中的__________ 有关;
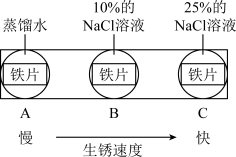
(2)如图实验说明NaCl在铁生锈中的作用是________
(3)铁生锈的次要过程∶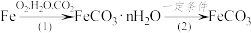 写出Fe转化为FeCO3
写出Fe转化为FeCO3 nH2O的化学方程式
nH2O的化学方程式________
(4)为防止铁生锈,可对铁制品“发蓝”处理,在表面生成致密氧化物(其中Fe、O元素质量比为21:8)保护膜,该氧化物的化学式为________
二、铁锈组分的确定
某铁锈成分为Fe2O3·xH2O和FeCO3。为确定其组成,兴趣小组称取此铁锈样品25.4g,在科研人员的指导下进行实验。

资料:①Fe2O3 xH2O在110℃分解为Fe2O3和H2O,FeCO3在282℃分解为FeO和CO2
②温度高于500℃时铁的氧化物才能被CO还原。
③浓硫酸具有吸水性,碱石灰能吸收水和二氧化碳
(5)装配好实验装置后,首先要________
(6)停止加热后仍需继续通CO,目的是防止生成的铁被再次氧化和_________ ;
(7)控制A装置中的温度为300℃对铁锈进行热分解,直至A装置中剰余固体质量不再变化为止,冷却后装置B增重3.6g,装置C增重2.2g。则样品中Fe2O3 xH2O的x=
xH2O的x=_______
(8)若缺少D装置,测得样品中FeCO3的值会________ (选填偏大”、“偏小”、“不变”)。
三、炼铁过程的探究
资料:CO还原赤铁矿(主要成分Fe2O3)炼铁的过程大致分为三个阶段:
阶段1: 阶段2:
阶段2: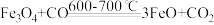
阶段3:
(9)写出工业上用CO和赤铁矿炼铁主要原理的化学方程式________ 。
(10)将上述300℃热分解后的A装置中剩余固体继续分阶段升温,进行CO还原铁的氧化物炼铁过程的探究。加热时测定A中剩余固体质量随温度变化的曲线如图所示。
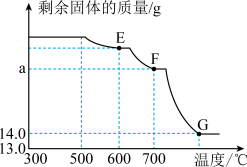
①300℃~500℃装置A中剩余固体质量没有发生变化的原因是______ 。
②图中F点对应的a=_______ 。
一、铁的应用和防护
(1)铁锈主要成分是Fe2O3·nH2O,铁生锈主要与空气中的
(2)如图实验说明NaCl在铁生锈中的作用是

(3)铁生锈的次要过程∶
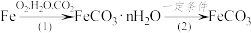 写出Fe转化为FeCO3
写出Fe转化为FeCO3 nH2O的化学方程式
nH2O的化学方程式(4)为防止铁生锈,可对铁制品“发蓝”处理,在表面生成致密氧化物(其中Fe、O元素质量比为21:8)保护膜,该氧化物的化学式为
二、铁锈组分的确定
某铁锈成分为Fe2O3·xH2O和FeCO3。为确定其组成,兴趣小组称取此铁锈样品25.4g,在科研人员的指导下进行实验。

资料:①Fe2O3 xH2O在110℃分解为Fe2O3和H2O,FeCO3在282℃分解为FeO和CO2
②温度高于500℃时铁的氧化物才能被CO还原。
③浓硫酸具有吸水性,碱石灰能吸收水和二氧化碳
(5)装配好实验装置后,首先要
(6)停止加热后仍需继续通CO,目的是防止生成的铁被再次氧化和
(7)控制A装置中的温度为300℃对铁锈进行热分解,直至A装置中剰余固体质量不再变化为止,冷却后装置B增重3.6g,装置C增重2.2g。则样品中Fe2O3
 xH2O的x=
xH2O的x=(8)若缺少D装置,测得样品中FeCO3的值会
三、炼铁过程的探究
资料:CO还原赤铁矿(主要成分Fe2O3)炼铁的过程大致分为三个阶段:
阶段1:
 阶段2:
阶段2: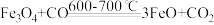
阶段3:

(9)写出工业上用CO和赤铁矿炼铁主要原理的化学方程式
(10)将上述300℃热分解后的A装置中剩余固体继续分阶段升温,进行CO还原铁的氧化物炼铁过程的探究。加热时测定A中剩余固体质量随温度变化的曲线如图所示。

①300℃~500℃装置A中剩余固体质量没有发生变化的原因是
②图中F点对应的a=
您最近一年使用:0次



