尿素[CO(NH2)2]是一种目前使用量较大的一种化学氮肥,适用于各种土壤和植物易保存,使用方便。
(1)尿素是一种含氮量很高的氮肥,它能使作物_____________ ;
(2)溶质质量分数32.5%的尿素溶液可用作柴油汽车尾气处理液,用尿素溶液处理柴油汽车尾气(含NO)时的化学方程式如下(反应条件略去):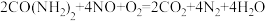 。现用含20Kg上述尿素溶液处理汽车尾气,请你回答下列问题:
。现用含20Kg上述尿素溶液处理汽车尾气,请你回答下列问题:
①配制上述尿素溶液,所需尿素的质量是___________ kg,水的体积是____________ L(水的密度1g/mL);
②计算用上述尿素溶液可除去的NO的质量是________ ?
③上述反应中,若尿素中氮元素为aKg,则生成的氮气中氮元素的质量是否为akg?________ 填“是”或“否”),原因是_______________ 。
(1)尿素是一种含氮量很高的氮肥,它能使作物
(2)溶质质量分数32.5%的尿素溶液可用作柴油汽车尾气处理液,用尿素溶液处理柴油汽车尾气(含NO)时的化学方程式如下(反应条件略去):
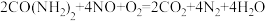 。现用含20Kg上述尿素溶液处理汽车尾气,请你回答下列问题:
。现用含20Kg上述尿素溶液处理汽车尾气,请你回答下列问题:①配制上述尿素溶液,所需尿素的质量是
②计算用上述尿素溶液可除去的NO的质量是
③上述反应中,若尿素中氮元素为aKg,则生成的氮气中氮元素的质量是否为akg?
更新时间:2020-02-03 14:15:58
|
相似题推荐
综合应用题
|
适中
(0.65)
解题方法
【推荐1】人类的生产和生活都离不开金属和金属材料。请回答:
(1)在日常生活中,用于制作导线的紫红色金属是_________ 。
(2)金属材料在生活中普遍使用。铁制品表面的锈要及时除去,这是因为铁锈具有_______ 结构,会加快铁制品的生锈。工业上常用稀盐酸除铁锈(主要成分Fe2O3)。请写出发生反应的化学方程式:_______ 。铝制品不需要除锈,这是因为铝表面能形成_______ ,可以阻止铝进一步氧化。
(3)化学兴趣小组的同学为了测定某赤铁矿石中氧化铁的质量分数,做了如下实验:
Ⅰ甲同学取一定质量的赤铁矿粉与过量的木炭粉混合后,用下图所示装置以合理的操作步骤测定(假设杂质始终不发生变化)。
查阅资料:碳和二氧化碳在高温条件下生成一氧化碳。

①写出B装置内发生反应的化学方程式__________ 。
②实验中持续道入干燥的氮气,停止加热前________ (选填“是”或“否”)需要先断开A和B的连接处以防止倒吸。
③如果氢氧化钠溶液对二氧化碳的吸收是完全的,那么甲同学用氢氧化钠溶液的质量变化测定出氧化铁的质量分数将_______ (选填“偏大”、“偏小”或“准确”),原因是_______ 。
Ⅱ乙同学取矿石样品10g,加入足量稀盐酸,完全反应后,过滤得到滤渣2g(假设杂质既不溶于水也不与酸发生反应)。则赤铁矿石中氧化铁的质量分数_________ ;反应后生成的氯化铁的质量为_______ g(精确到0.01g)。
(1)在日常生活中,用于制作导线的紫红色金属是
(2)金属材料在生活中普遍使用。铁制品表面的锈要及时除去,这是因为铁锈具有
(3)化学兴趣小组的同学为了测定某赤铁矿石中氧化铁的质量分数,做了如下实验:
Ⅰ甲同学取一定质量的赤铁矿粉与过量的木炭粉混合后,用下图所示装置以合理的操作步骤测定(假设杂质始终不发生变化)。
查阅资料:碳和二氧化碳在高温条件下生成一氧化碳。

①写出B装置内发生反应的化学方程式
②实验中持续道入干燥的氮气,停止加热前
③如果氢氧化钠溶液对二氧化碳的吸收是完全的,那么甲同学用氢氧化钠溶液的质量变化测定出氧化铁的质量分数将
Ⅱ乙同学取矿石样品10g,加入足量稀盐酸,完全反应后,过滤得到滤渣2g(假设杂质既不溶于水也不与酸发生反应)。则赤铁矿石中氧化铁的质量分数
您最近一年使用:0次
综合应用题
|
适中
(0.65)
【推荐2】(1)为减少汽车尾气排放,我国将在全国范围内推广车用乙醇气油。
①汽油不完全燃烧会产生CO和碳氢化合物,乙醇(C2H5OH)的燃烧比汽油更充分,乙醇完全燃烧的化学方程式为________________ 。
②汽车尾气中含有CO、NO等污染物,使用三元催化剂可以将它们转化成两种无毒气体,其微观示意图如下图所示,请在方框中补全相应微粒的图示。_________

(2)一种新型“人造树叶”可吸收二氧化碳并转化为乙醇,反应的化学方程式为 。研究显示,IL“人造树叶”每天可以从空气中吸收968g二氧化碳。计算1L“人造树叶”工作一天可得到乙醇的质量
。研究显示,IL“人造树叶”每天可以从空气中吸收968g二氧化碳。计算1L“人造树叶”工作一天可得到乙醇的质量_______________ 。
①汽油不完全燃烧会产生CO和碳氢化合物,乙醇(C2H5OH)的燃烧比汽油更充分,乙醇完全燃烧的化学方程式为
②汽车尾气中含有CO、NO等污染物,使用三元催化剂可以将它们转化成两种无毒气体,其微观示意图如下图所示,请在方框中补全相应微粒的图示。

(2)一种新型“人造树叶”可吸收二氧化碳并转化为乙醇,反应的化学方程式为
 。研究显示,IL“人造树叶”每天可以从空气中吸收968g二氧化碳。计算1L“人造树叶”工作一天可得到乙醇的质量
。研究显示,IL“人造树叶”每天可以从空气中吸收968g二氧化碳。计算1L“人造树叶”工作一天可得到乙醇的质量
您最近一年使用:0次
综合应用题
|
适中
(0.65)
【推荐3】碳和碳的化合物是初中化学学习的重要内容。

(1)金刚石、石墨和C60都是由碳元素组成的单质,下列有关说法正确的___ (填字母代号)。
A 都是黑色固体 B 硬度相同
C 完全燃烧都生成二氧化碳 D 碳原子的排列方式相同
(2)碳酸钠广泛用于玻璃、造纸、纺织和洗涤剂的生产等。
①如何检验一瓶碳酸钠溶液中是否混有氢氧化钠?请简要写出实验步骤、现象和结论。_________ 。
②如图1所示是某趣味实验装置图,其气密性良好。打开分液漏斗的活塞后,可观察到气球胀大的现象。请用化学方程式解释产生此现象的原因。____________
(3)如图2是实验室中制取气体常用到的仪器,请回答下列问题:
①请写出用D装置制取氧气的化学方程式______________________________ 。
②实验室可用碳化钙(CaC2)固体和水反应来制取乙炔气体,该反应必须严格控制加水的速率,以免剧烈反应放热引起发生装置炸裂,则制取乙炔的最适合发生装置是__ ;若用E装置采用排水法来收集乙炔,请简述操作步骤。_________
(4)乙炔(C2H2)是一种重要的化工原料。常用碳化钙(CaC2)与水反应制取乙炔,同时生成氢氧化钙。若要制取6.5g乙炔气体,理论上需要碳化钙的质量是多少?____________

(1)金刚石、石墨和C60都是由碳元素组成的单质,下列有关说法正确的
A 都是黑色固体 B 硬度相同
C 完全燃烧都生成二氧化碳 D 碳原子的排列方式相同
(2)碳酸钠广泛用于玻璃、造纸、纺织和洗涤剂的生产等。
①如何检验一瓶碳酸钠溶液中是否混有氢氧化钠?请简要写出实验步骤、现象和结论。
②如图1所示是某趣味实验装置图,其气密性良好。打开分液漏斗的活塞后,可观察到气球胀大的现象。请用化学方程式解释产生此现象的原因。
(3)如图2是实验室中制取气体常用到的仪器,请回答下列问题:
①请写出用D装置制取氧气的化学方程式
②实验室可用碳化钙(CaC2)固体和水反应来制取乙炔气体,该反应必须严格控制加水的速率,以免剧烈反应放热引起发生装置炸裂,则制取乙炔的最适合发生装置是
(4)乙炔(C2H2)是一种重要的化工原料。常用碳化钙(CaC2)与水反应制取乙炔,同时生成氢氧化钙。若要制取6.5g乙炔气体,理论上需要碳化钙的质量是多少?
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐1】某研究性学习小组为了测定黄铜(铜、锌合金)的组成。在化学老师的帮助下,选用98%的浓硫酸、黄铜样品进行下列实验并计算。
(1)计算:需要浓硫酸约8.2mL;需要水的体积为_________ mL(取整数值)
(2)量取浓硫酸和水:用量筒量取8.2 mL浓硫酸和一定体积的水。如果量取98%的浓硫酸时俯视读数,会导致所配溶液溶质质量分数_________ 9.8%(填“大于”、“小于”或“等于”)。
(3)_________ 。
(4)装瓶贴标签。
实验Ⅱ:用下图1所示装置测定锌铜合金中锌、铜的质量分数。
(4)实验前,先将锌铜合金用砂纸打磨,其目的是:_________ ;
(5)实验操作步骤有:①记录量气管D的液面位置;②检查气密性,将药品和水装入各仪器中,连接好装置。③待B中不再有气体产生并恢复至室温后,记录量气管D的液面位置;④由A向B滴加足量试剂;⑤将B中剩余固体过滤,洗涤,干燥,称重;上述进行的操作的顺序是_________ (填序号);记录量气管D的液面位置时,除视线平视外,还应_________ ;
(6)B中发生反应的化学方程式为_________ ;
(7)若实验中,锌铜合金与稀硫酸充分反应后,测得产生的气体体积为V L,为求出合金中锌、铜的质量分数,还要用到下列数据中的_________ ;
A.加入的稀硫酸的质量分数 B.反应后B中剩余固体的质量
C.实验前反应装置中空气的体积 D.实验条件下氢气的密度

(8)小组同学交流发现上述方法测得的锌的质量分数会偏大,现将装置改为如图2所示,改进的目的是_________ 。
(1)计算:需要浓硫酸约8.2mL;需要水的体积为
(2)量取浓硫酸和水:用量筒量取8.2 mL浓硫酸和一定体积的水。如果量取98%的浓硫酸时俯视读数,会导致所配溶液溶质质量分数
(3)
(4)装瓶贴标签。
实验Ⅱ:用下图1所示装置测定锌铜合金中锌、铜的质量分数。
(4)实验前,先将锌铜合金用砂纸打磨,其目的是:
(5)实验操作步骤有:①记录量气管D的液面位置;②检查气密性,将药品和水装入各仪器中,连接好装置。③待B中不再有气体产生并恢复至室温后,记录量气管D的液面位置;④由A向B滴加足量试剂;⑤将B中剩余固体过滤,洗涤,干燥,称重;上述进行的操作的顺序是
(6)B中发生反应的化学方程式为
(7)若实验中,锌铜合金与稀硫酸充分反应后,测得产生的气体体积为V L,为求出合金中锌、铜的质量分数,还要用到下列数据中的
A.加入的稀硫酸的质量分数 B.反应后B中剩余固体的质量
C.实验前反应装置中空气的体积 D.实验条件下氢气的密度

(8)小组同学交流发现上述方法测得的锌的质量分数会偏大,现将装置改为如图2所示,改进的目的是
您最近一年使用:0次
综合应用题
|
适中
(0.65)
【推荐2】硫酸亚铁可以促进花草生长,现有一包混有少量硫酸铜的硫酸亚铁固体X,从X中获得硫酸亚铁的过程如下:
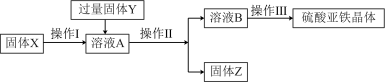
(1)操作Ⅱ的名称是_______ ,此操作中玻璃棒的作用是______ 。
(2)固体Y过量的目的是________ 。
(3)现将160g溶质质量分数为40%的硫酸铜溶液稀释成溶质质量分数为20%的硫酸铜溶液,需要加水______ mL,操作步骤为:计算、________ 、稀释。
(4)向一定量的铁粉中加入20%的硫酸铜溶液,实验数据如图所示。求恰好完全反应时所得溶液中溶质的质量分数________ (计算结果精确到0.1%)。


(1)操作Ⅱ的名称是
(2)固体Y过量的目的是
(3)现将160g溶质质量分数为40%的硫酸铜溶液稀释成溶质质量分数为20%的硫酸铜溶液,需要加水
(4)向一定量的铁粉中加入20%的硫酸铜溶液,实验数据如图所示。求恰好完全反应时所得溶液中溶质的质量分数

您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐3】2015年3月22日是第二十三届“世界水日”,主题是“水与可持续发展”。

(1)根据下图回答问题。
①A图所示的是水的电解实验,试管2中收集的气体是_______ (填名称)。
②B图所示的是活性炭净水器的示意图,其中活性炭的作用是_______ 。
③C、D图所示的是探究铁生锈条件的实验,一段时间后发现C中铁片变红,D中铁片依然光亮,对比C、D中的现象,说明决定铁生锈快慢的一个重要因素是:_______ 。
④E图所示的是探究燃烧条件实验,其中热水作用_______ 。
(2)若用质量分数为10%的氢氧化钠溶液(密度为1.1g/cm3)配制110g质量分数为5%的氢氧化钠溶液。
①计算:需10%的氢氧化钠溶液体积为_______ mL。
②量取:用量筒量取氢氧化钠溶液和水,均倒入烧杯中。若量取氢氧化钠溶液读数时俯视,而其余操作均正确,这样配得的溶液的溶质质量分数会_______ (填“偏高”、“偏低”或“无影响”);用量筒量取水。
③混匀:用玻璃棒搅拌,使氢氧化钠溶液和水混合均匀。
④装瓶并贴上标签。
(3)某化学兴趣小组为了测定某工厂废水中硫酸的质量分数,取100g废水于烧杯中,加入上述配制好的氢氧化钠溶液80g,恰好完全反应(废水中无不溶物,其它成分不与氢氧化钠反应)。请计算废水中硫酸的质量分数。(写出计算过程)

(1)根据下图回答问题。
①A图所示的是水的电解实验,试管2中收集的气体是
②B图所示的是活性炭净水器的示意图,其中活性炭的作用是
③C、D图所示的是探究铁生锈条件的实验,一段时间后发现C中铁片变红,D中铁片依然光亮,对比C、D中的现象,说明决定铁生锈快慢的一个重要因素是:
④E图所示的是探究燃烧条件实验,其中热水作用
(2)若用质量分数为10%的氢氧化钠溶液(密度为1.1g/cm3)配制110g质量分数为5%的氢氧化钠溶液。
①计算:需10%的氢氧化钠溶液体积为
②量取:用量筒量取氢氧化钠溶液和水,均倒入烧杯中。若量取氢氧化钠溶液读数时俯视,而其余操作均正确,这样配得的溶液的溶质质量分数会
③混匀:用玻璃棒搅拌,使氢氧化钠溶液和水混合均匀。
④装瓶并贴上标签。
(3)某化学兴趣小组为了测定某工厂废水中硫酸的质量分数,取100g废水于烧杯中,加入上述配制好的氢氧化钠溶液80g,恰好完全反应(废水中无不溶物,其它成分不与氢氧化钠反应)。请计算废水中硫酸的质量分数。(写出计算过程)
您最近一年使用:0次
综合应用题
|
适中
(0.65)
名校
解题方法
【推荐1】黑龙江省是农业大省和粮食主产区。庄稼一枝花,全靠肥当家,施肥是使农业增产的重要手段。

(1)根据你所学的化肥知识连线:
(2)含氮量最高的铵态氮肥的化学式是 ________________ ;长期施用硫酸钾的土壤需要撒入适量的________________ (填俗称)进行改良后再种植农作物。

(1)根据你所学的化肥知识连线:
| 对植物的作用 | 化肥种类 | 缺乏后的症状 |
| ①提高蛋白质含量 a.氮肥 Ⅰ.叶边发黄 ②增强抗倒伏抗病虫害能力 b.磷肥 Ⅱ.植株矮小 ③增强抗寒抗旱能力 c.钾肥 Ⅲ.叶片发黄 | ||
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐2】今年两会期间,习近平总书记强调:农业强国是社会主义强国的根基,粮食生产则是“三农”工作的重中之重。使用化肥是农业生产中重要的增产手段。
(1)三种常见的氮肥:①硝酸铵 ②尿素[CO(NH2)2] ③氯化铵,含氮量由大到小的顺序是___ (填序号)。
(2)取上述三种氮肥分别加熟石灰研磨,可快速检出尿素,依据的现象是_______ 。要将硝酸铵转化为一种复合肥料,可选用的反应物是_______ 。
(3)某化肥包装袋标签上的部分内容如图。化学兴趣小组为测定该化肥的纯度,取12.5g样品配制成溶液,向其中滴加AgNO3溶液至不再产生沉淀为止。过滤、洗涤、干燥,得到的沉淀质量为28.7g。通过计算判断该化肥是否合格____ 。

(1)三种常见的氮肥:①硝酸铵 ②尿素[CO(NH2)2] ③氯化铵,含氮量由大到小的顺序是
(2)取上述三种氮肥分别加熟石灰研磨,可快速检出尿素,依据的现象是
(3)某化肥包装袋标签上的部分内容如图。化学兴趣小组为测定该化肥的纯度,取12.5g样品配制成溶液,向其中滴加AgNO3溶液至不再产生沉淀为止。过滤、洗涤、干燥,得到的沉淀质量为28.7g。通过计算判断该化肥是否合格

您最近一年使用:0次
综合应用题
|
适中
(0.65)
【推荐3】空气是宝贵的自然资源,图 1 是以空气和其他必要的原料合成氮肥(NH4HCO3)的流程,图 2 是某化肥碳酸氢铵包装袋上的部分说明。请按要求回答下列问题。
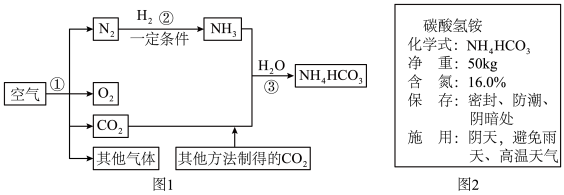
(1)空气属于___________ (填“纯净物”或“混合物”),图 1 是以空气和其他必要的原料合成氮肥(NH4HCO3)的流程,步骤① ___________ (填“是”或“不是”)分解反应。
(2)用“ ”表示氮原子
”表示氮原子  ”表示氧原子。
”表示氧原子。
①用 ”可表示的微粒是
”可表示的微粒是 ___________ (填化学符号)。
②同温同压下,气体的体积比等于分子数目比。若空气中其它成分忽略不计,图 3 可表示空气微观模型的是___________ (填字母)。

(3)用化学用语表示:
①氖气___________
②步骤②的反应中没有改变的微粒是___________
③铵根离子___________
④标出 NH3中氮元素的化合价___________
⑤步骤②反应的化学方程式是___________ 。
⑥步骤③反应的化学方程式是___________ 。
(4)图 2 为某碳酸氢铵化肥样品的标签
①从标签上看碳酸氢铵具有的化学性质是___________ (填字母)。
A 易溶于水B 有挥发性C 受热易分解
②该袋化肥中氮元素的质量至少为___________ kg。
③若杂质中不含氮元素,图 2 所示的化肥中碳酸氢铵的质量分数为___________ (计算结果精确到 0.1%)。

(1)空气属于
(2)用“
 ”表示氮原子
”表示氮原子  ”表示氧原子。
”表示氧原子。①用
 ”可表示的微粒是
”可表示的微粒是 ②同温同压下,气体的体积比等于分子数目比。若空气中其它成分忽略不计,图 3 可表示空气微观模型的是

(3)用化学用语表示:
①氖气
②步骤②的反应中没有改变的微粒是
③铵根离子
④标出 NH3中氮元素的化合价
⑤步骤②反应的化学方程式是
⑥步骤③反应的化学方程式是
(4)图 2 为某碳酸氢铵化肥样品的标签
①从标签上看碳酸氢铵具有的化学性质是
A 易溶于水B 有挥发性C 受热易分解
②该袋化肥中氮元素的质量至少为
③若杂质中不含氮元素,图 2 所示的化肥中碳酸氢铵的质量分数为
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐1】对于农作物来说,科学合理的施肥有助于作物增产增收。
(1)草木灰(主要成分是K2CO3) 是农村里常见的一种肥料,它是植物体燃烧后所产生的灰烬。K2CO3和Na2CO3具有相似的化学性质,其水溶液显碱性。下列有关草木灰的说法中,不正确的是 (填下列选项序号之一)。
(2)干净的烧杯中盛有K2CO3和 KCl的固体混合物样品20g,加入一定质量的水使其完全溶解,然后向所得溶液中逐滴加入溶质质量分数为7.3%的稀盐酸,烧杯中溶液的质量与滴入稀盐酸的质量关系如图所示。试回答下列问题:
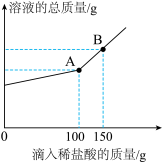
①当滴入上述稀盐酸至图中B 点时,烧杯中溶液里的溶质为_____ (写化学式)。
②当滴入上述稀盐酸至100g(即图中A 点)时,恰好完全反应。试通过计算,求原固体混合物样品中KCl 的质量_____ (计算结果精确到0.1g)。
(1)草木灰(主要成分是K2CO3) 是农村里常见的一种肥料,它是植物体燃烧后所产生的灰烬。K2CO3和Na2CO3具有相似的化学性质,其水溶液显碱性。下列有关草木灰的说法中,不正确的是 (填下列选项序号之一)。
| A.草木灰与铵态氮肥混合使用效果更好 |
| B.草木灰在农业生产中,主要作为钾肥使用 |
| C.草木灰可促使植株生长健壮,增强其抗病虫和抗倒伏的能力 |
(2)干净的烧杯中盛有K2CO3和 KCl的固体混合物样品20g,加入一定质量的水使其完全溶解,然后向所得溶液中逐滴加入溶质质量分数为7.3%的稀盐酸,烧杯中溶液的质量与滴入稀盐酸的质量关系如图所示。试回答下列问题:

①当滴入上述稀盐酸至图中B 点时,烧杯中溶液里的溶质为
②当滴入上述稀盐酸至100g(即图中A 点)时,恰好完全反应。试通过计算,求原固体混合物样品中KCl 的质量
您最近一年使用:0次
综合应用题
|
适中
(0.65)
【推荐2】我国拥有地球上7%的耕地,但化肥使用量却占全球总量的35%,认识化肥,科学施肥至关重要.
(1)下列物质中,可用作磷肥的是_______________ :
A.K2SO4 B.CO(NH2)2 C.KNO3 D.Ca(H2PO4)
(2)NH4Cl是常见的氮肥,不能与碱性物质混用,否则会因释放出________ 而损失肥效;
(3)过度使用化肥造成的后果有:①____________________ ;②水体富营养化等;
(4)“雷雨发庄稼”现象涉及的化学反应较为复杂,其中一个反应是NO3与H2O反应生成HNO2和NO,写出该反应的化学方程式:__________________________ ;该反应中.化合价发生改变的元素是________ (填元素符号).
(1)下列物质中,可用作磷肥的是
A.K2SO4 B.CO(NH2)2 C.KNO3 D.Ca(H2PO4)
(2)NH4Cl是常见的氮肥,不能与碱性物质混用,否则会因释放出
(3)过度使用化肥造成的后果有:①
(4)“雷雨发庄稼”现象涉及的化学反应较为复杂,其中一个反应是NO3与H2O反应生成HNO2和NO,写出该反应的化学方程式:
您最近一年使用:0次
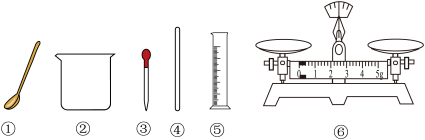
【推荐3】几种作物的无土栽培营养液部分溶质的质量分数如表,配制溶液的仪器如图。
几种作物营养液溶质的质量分数(%)
______ 。
(2)硝酸钾和磷酸二氢铵均属于______ 肥。
(3)配制质量分数为7.08%的硝酸钾溶液200g,需要硝酸钾______ g(精确到0.1g)。
(4)将质量分数为7.08%的硝酸钾溶液稀释为4.04%,需选择图1中的烧杯和______ (填序号)。
(5)利用化学方程式计算。磷酸二氢铵与熟石灰混合使用会降低肥效,其原理是: ,产生3.4g氨气消耗熟石灰的质量是多少?
,产生3.4g氨气消耗熟石灰的质量是多少?
几种作物营养液溶质的质量分数(%)
番茄 | 甜瓜 | 茄子 | |
硝酸钾(KNO3) | 4.04 | 6.07 | 7.08 |
磷酸二氢铵(NH4H2PO4) | 0.77 | 1.53 | 1.15 |
(2)硝酸钾和磷酸二氢铵均属于
(3)配制质量分数为7.08%的硝酸钾溶液200g,需要硝酸钾
(4)将质量分数为7.08%的硝酸钾溶液稀释为4.04%,需选择图1中的烧杯和
(5)利用化学方程式计算。磷酸二氢铵与熟石灰混合使用会降低肥效,其原理是:
 ,产生3.4g氨气消耗熟石灰的质量是多少?
,产生3.4g氨气消耗熟石灰的质量是多少?
您最近一年使用:0次



