九年级课外活动小组的同学们在期末复习时,来到化学实验室亲自对“质量守恒定律”进行了再次探究,如图是他们根据这一学期学过的化学反应分别设计的实验,请你一起参与他们的探究活动,并回答相关问题
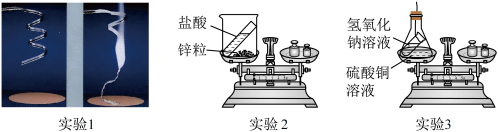
实验1:称量镁条,点燃,待反应结束后,再称量。
实验2:将盛有稀盐酸的小试管放入盛有锌粒的烧杯中称量,然后使稀盐酸与锌粒接触,充分反应后再称量实验3:将盛有氢氧化钠溶液的小试管放入盛有硫酸铜溶液的锥形瓶中称量,然后使氢氧化钠溶液与硫酸铜溶液混合,充分反应后再称量。
(1)实验1观察到的现象是_______________ ;
(2)写出实验3反应的化学方程式________________ ;
(3)上述三个反应______________ (填“符合”或“不符合”)质量守恒定律,实验___________ 正确反映了反应物与生成物的质量关系;
(4)由上述实验我们得到启示,探究_______________ 的反应验证质量守恒定律,实验必须在密闭的装置中进行;
(5)由质量守恒定律可知,化学反应前后,一定不变的是_____________ (填序号);
①物质种类 ②元素种类 ③原子种类 ④分子种类 ⑤分子数目 ⑥原子数目

实验1:称量镁条,点燃,待反应结束后,再称量。
实验2:将盛有稀盐酸的小试管放入盛有锌粒的烧杯中称量,然后使稀盐酸与锌粒接触,充分反应后再称量实验3:将盛有氢氧化钠溶液的小试管放入盛有硫酸铜溶液的锥形瓶中称量,然后使氢氧化钠溶液与硫酸铜溶液混合,充分反应后再称量。
| 编号 | 实验1 | 实验2 | 实验3 |
| 反应前称重质量 | 9.6g | 212.6g | 118.4g |
| 反应后称重质量 | 16.0g | 212.4g | 118.4g |
(2)写出实验3反应的化学方程式
(3)上述三个反应
(4)由上述实验我们得到启示,探究
(5)由质量守恒定律可知,化学反应前后,一定不变的是
①物质种类 ②元素种类 ③原子种类 ④分子种类 ⑤分子数目 ⑥原子数目
更新时间:2020-01-31 22:32:18
|
【知识点】 实验探究质量守恒定律解读
相似题推荐
科学探究题
|
适中
(0.65)
解题方法
【推荐1】某化学课外小组同学用如图所示实验探究质量守恒定律。

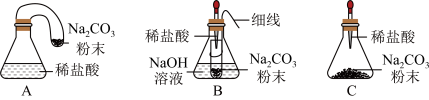
(1)甲同学用图A所示实验进行探究,在瓶中先铺一层细沙,再引燃白磷,为什么?_______ ,玻璃管的作用是_______ ,白磷燃烧生成五氧化二磷(P2O5)试写出该反应的化学方程式________ ,如果引燃白磷后,立即将锥形瓶放在天平上并平衡,在燃烧过程中天平上的指针如何偏转________ ,试验结束,冷却到室温,天平_______ 平衡。(填“是”或“否”)
(2)乙同学用B装置研究质量守恒定律时(反应方程式为Na2CO3+2HCl = 2NaCl+H2O+CO2↑),一段时间后发现天平的指针偏右。造成天平的指针向右偏转的原因是_______ 。
(3)丙同学用C实验说明了质量守恒定律,C实验(Fe + CuSO4 = Cu + FeSO4)能在敞口容器中进行的原因是______ 。
(4)丁同学用图D中镁带在空气中燃烧的实验来探究质量守恒定律时,发现一定质量的镁完全燃烧后留下的固体质量比反应前镁带的质量轻,联系实验现象,可能的原因是_______ 。
(5)金属镁是化学性质非常活泼的金属,在空气中不但能与氧气反应,还能与二氧化碳、氮气等反应产生黑色和淡黄色的固体,但是在实验中很少看到黑色和黄色固体的原因是_______ 。

(1)甲同学用图A所示实验进行探究,在瓶中先铺一层细沙,再引燃白磷,为什么?
(2)乙同学用B装置研究质量守恒定律时(反应方程式为Na2CO3+2HCl = 2NaCl+H2O+CO2↑),一段时间后发现天平的指针偏右。造成天平的指针向右偏转的原因是
(3)丙同学用C实验说明了质量守恒定律,C实验(Fe + CuSO4 = Cu + FeSO4)能在敞口容器中进行的原因是
(4)丁同学用图D中镁带在空气中燃烧的实验来探究质量守恒定律时,发现一定质量的镁完全燃烧后留下的固体质量比反应前镁带的质量轻,联系实验现象,可能的原因是
(5)金属镁是化学性质非常活泼的金属,在空气中不但能与氧气反应,还能与二氧化碳、氮气等反应产生黑色和淡黄色的固体,但是在实验中很少看到黑色和黄色固体的原因是
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐2】以下是老师引导学生探究“质量守恒定律”的教学片段,请你参与探究并帮忙填写空格(包括表中的空格)。
【提出问题】化学反应前后各物质的质量总和是否相等?
【猜想与假设】猜想 1:不相等;猜想 2:相等.
【实验探究】甲、乙两组同学用托盘天平分别称量反应前后物质的质量.
【反思评价】究竟哪种猜想正确?通过讨论,同学们发现甲组中有气体逸出。得到启示: 在探究化学反应前后各物质的质量总和是否相等时,凡有气体生成或参加的反应一定要在_____ 中进行。
【优化装置】同学们对甲组左盘中的反应装置进行了如下三种改进,你认为最佳装置是_____ (填序号),从另外两种装置中任选一种指出其不足 _____ .(已知二氧 化碳能与氢氧化钠发生化学反应)
| 甲组 | 乙组 | |
实验方案 | 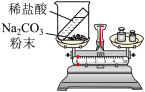 |  |
实验现象 | 铁钉表面有红色物质析出,溶液颜色发生改变,天平保持平衡 | |
结论 | 猜想 1 正确 | 猜想 2 正确,反应的化学方程式为 |
【猜想与假设】猜想 1:不相等;猜想 2:相等.
【实验探究】甲、乙两组同学用托盘天平分别称量反应前后物质的质量.
【反思评价】究竟哪种猜想正确?通过讨论,同学们发现甲组中有气体逸出。得到启示: 在探究化学反应前后各物质的质量总和是否相等时,凡有气体生成或参加的反应一定要在
【优化装置】同学们对甲组左盘中的反应装置进行了如下三种改进,你认为最佳装置是

您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐3】为验证质量守恒定律,我们做了镁条在空气中燃烧的实验。点燃前,先将镁条用_____ 打磨光亮,再用_____ (填仪器名称) 夹持镁条点燃,观察到的现象是剧烈燃烧、_____ 、放热、冒出白烟、生成白色固体。充分燃烧后发现石棉网上剩余固体的质量小于反应前镁条的质量,原因可能是_____ 。某同学还发现产物中有少量黄色固体。
【查阅资料】
镁能与氮气反应生成黄色的氮化镁固体(Mg3N2),反应的化学方程式是_____ 。
【反思与交流】
空气中N2的含量远大于O2的含量,而镁条在空气中燃绕生成的氧化镁却远多于氮化镁,原因是_____ 。
【拓展与迁移】
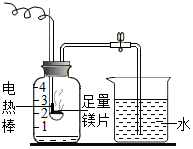
测量空气中氧气含量的实验中,如果装置气密性良好,将红磷换成镁片,反应停止后,冷却至室温,打开止水夹,发现集气瓶内液面_____ (填“高于”、“等于”或“低于”) 集气瓶的刻度1。
【查阅资料】
镁能与氮气反应生成黄色的氮化镁固体(Mg3N2),反应的化学方程式是
【反思与交流】
空气中N2的含量远大于O2的含量,而镁条在空气中燃绕生成的氧化镁却远多于氮化镁,原因是
【拓展与迁移】
测量空气中氧气含量的实验中,如果装置气密性良好,将红磷换成镁片,反应停止后,冷却至室温,打开止水夹,发现集气瓶内液面

您最近一年使用:0次



