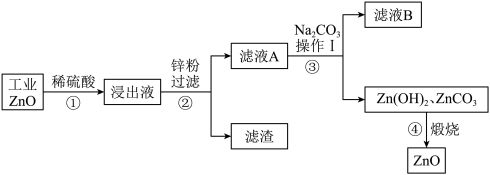
氧化锌为白色粉末,可用于湿疹、癣等皮肤病的治疗。用工业氧化锌(含有FeO、CuO杂质)生产纯氧化锌的流程如下:
请回答下列问题:
(1)写出浸出液中的阳离子:______ ;
(2)步骤②中发生了两个反应,都属于______ (填基本反应类型)。
(3)从除杂原理分析,步骤②中得到的滤渣含有的金属有______ 种。
(4)步骤③操作I中用到的玻璃容器为_______ (填仪器名称)。
(5)已知步骤④中发生分解反应,写出有二氧化碳气体产生的化学方程式______ 。

请回答下列问题:
(1)写出浸出液中的阳离子:
(2)步骤②中发生了两个反应,都属于
(3)从除杂原理分析,步骤②中得到的滤渣含有的金属有
(4)步骤③操作I中用到的玻璃容器为
(5)已知步骤④中发生分解反应,写出有二氧化碳气体产生的化学方程式
更新时间:2020/03/31 08:48:12
|
相似题推荐
填空与简答-填空题
|
适中
(0.65)
名校
解题方法
【推荐1】针对网上流传的“能燃烧的面条不安全,是因为含有添加剂”的消息,从化学的视角分析缺乏科学依据。
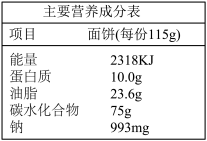
(1)表中“钠”指的是___________ (填序号)。
a 元素 b 分子 c 原子
(2)碳原子的结构示意图为_________ 。
(3)面条是以面粉为原料制作而成的。
①为避免面粉厂车间发生爆炸事故,生产过程不可采取的措施有_______ (填序号)。
A 严禁吸烟,杜绝火源
B 密封门窗,隔绝氧气
C 轻拿轻放,减少粉尘扬起
②面粉的主要成分是淀粉【化学式为(C6H10O5)n】,类比乙醇的燃烧,写出淀粉在空气中完全燃烧的产物____ (填化学式)。

(1)表中“钠”指的是
a 元素 b 分子 c 原子
(2)碳原子的结构示意图为
(3)面条是以面粉为原料制作而成的。
①为避免面粉厂车间发生爆炸事故,生产过程不可采取的措施有
A 严禁吸烟,杜绝火源
B 密封门窗,隔绝氧气
C 轻拿轻放,减少粉尘扬起
②面粉的主要成分是淀粉【化学式为(C6H10O5)n】,类比乙醇的燃烧,写出淀粉在空气中完全燃烧的产物
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
名校
解题方法
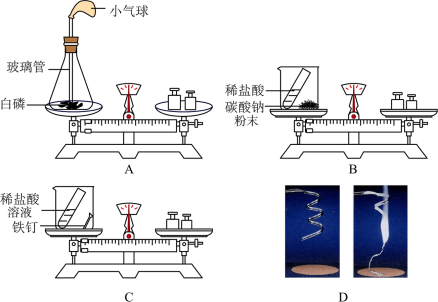
【推荐2】某化学课外小组同学用如图所示实验探究质量守恒定律:______ 。
(2)乙同学用B装置探究质量守恒定律时,一段时间后发现天平的指针偏右。造成天平的指针向右偏转的原因是______ 。
(3)丙同学用C实验探究质量守恒定律,C实验能在敞口容器中进行实验的原因是______ 。
(4)丁同学用图D中的镁条在空气中燃烧的实验来探究质守恒定律时,发现一定质量的镁条完全燃烧后留下的固体质量比反应前镁条的质量轻,如果在燃着的镁条上方罩上罩,使生成物全部收集起来称量,出现的结果是______ (填“偏大”“偏小”或“不变”)。
(5)综上所述,A、B、C、D所示四个实验中能用来验证质量守恒定律的实验是______ (选填字母序号)。
(2)乙同学用B装置探究质量守恒定律时,一段时间后发现天平的指针偏右。造成天平的指针向右偏转的原因是
(3)丙同学用C实验探究质量守恒定律,C实验能在敞口容器中进行实验的原因是
(4)丁同学用图D中的镁条在空气中燃烧的实验来探究质守恒定律时,发现一定质量的镁条完全燃烧后留下的固体质量比反应前镁条的质量轻,如果在燃着的镁条上方罩上罩,使生成物全部收集起来称量,出现的结果是
(5)综上所述,A、B、C、D所示四个实验中能用来验证质量守恒定律的实验是
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐3】废旧电路板中主要含有塑料、铜和锡(Sn)等,为实现对锡的绿色回收,设计如下工艺流程:
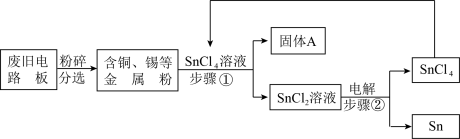
(1)废旧电路板粉碎的目的是__________ 。
(2)写出步骤②发生反应的化学方程式__________ ,该反应属于基本反应类型中的__________ 。
(3)步骤①②均需采取过滤操作,此操作中玻璃棒的作用是__________ 。
(4)该流程中可以循环再利用的物质是__________ 。
(5)理论推算,最终获得纯金属锡的质量__________ 处理废旧电路板中锡的质量(填“>”、“<”或“=”)。

(1)废旧电路板粉碎的目的是
(2)写出步骤②发生反应的化学方程式
(3)步骤①②均需采取过滤操作,此操作中玻璃棒的作用是
(4)该流程中可以循环再利用的物质是
(5)理论推算,最终获得纯金属锡的质量
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
名校
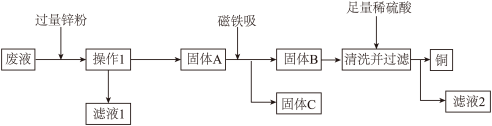
【推荐1】实验结束时,同学们将含有CuSO4、ZnSO4、FeSO4的废液倒在废液缸里,如果将废液直接排放就会造成水污染。于是几位同学利用课余处理废液,回收工业重要原料硫酸锌和有关金属。实验过程如下:
请回答:
(1)操作1是_______ ,固体A的成分_______ 。
(2)固体C是_______ 。滤液1和滤液2中溶质相同,该溶质是_______ 。
(3)写出加入过量锌粉的其中一个反应的化学方程式______ ; 加入足量稀硫酸发生反应的化学方程式__________ 。

请回答:
(1)操作1是
(2)固体C是
(3)写出加入过量锌粉的其中一个反应的化学方程式
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
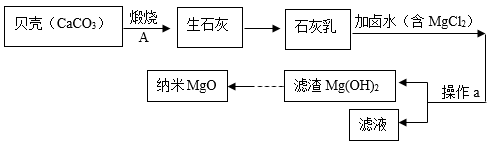
【推荐2】利用合金黄铜制造各种物品的过程中,会产生大量的黄铜渣,主要成分有Zn、Cu、CuO和ZnO,某化学小组利用该金属废料回收Cu并制取ZnO,设计了如下实验:
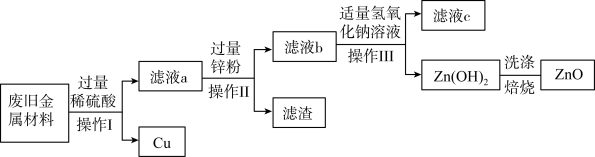
(1)下列关于合金的说法正确的是______。
(2)操作I的名称是______ 。
(3)在废旧金属材料中加入过量稀硫酸,生成气体的化学反应方程式为______ 。
(4)操作I中所得滤液a的溶质成分是______ 。
(5)向滤液b中加入适量氢氧化钠溶液的目的是______ 。
(6)将分离出来的Cu加入到稀硝酸中,溶液变蓝,生成一氧化氮气体,请写出该反应的化学方程式______ 。

(1)下列关于合金的说法正确的是______。
| A.合金的硬度一般比组成它们的纯金属高 |
| B.生铁和钢都是铁合金,但钢中的含碳量比生铁中的高 |
| C.武德合金的熔点比其组分金属低,可用于制作保险丝 |
(2)操作I的名称是
(3)在废旧金属材料中加入过量稀硫酸,生成气体的化学反应方程式为
(4)操作I中所得滤液a的溶质成分是
(5)向滤液b中加入适量氢氧化钠溶液的目的是
(6)将分离出来的Cu加入到稀硝酸中,溶液变蓝,生成一氧化氮气体,请写出该反应的化学方程式
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
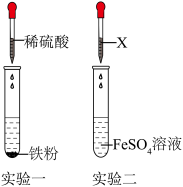
【推荐1】铁是生产、生活中广泛应用的金属材料,“铁的循环”如图所示。其中,箭号的朝向表示能一步实现的物质转化方向,X、Y、Z是初中化学常见的物质。___________ (写一个)。
(2)实验二:在FeSO4溶液中滴加X溶液,可观察到溶液中产生白色沉淀,但又迅速变成灰绿色,最终变成红棕色。这是因为白色的氢氧化亚铁不稳定,其会与氧气、水等物质反应生成红棕色的氢氧化铁。
I.X的化学式是___________ (写一个)。
II.要使实验二产生的氢氧化亚铁白色保持的时间长一些,可采取的措施___________ 。(写一个)
(3)实验二中最后得到的浊液通过过滤、___________ 和烘焙等实验操作可制得Y(红色粉末)。
(4)工业上用Y与Z反应生产铁,反应⑤的化学方程式为___________ 。
(5)已知在化学反应中,若有元素的化合价升高或降低,该化学反应可判定为氧化还原反应,则“铁的循环”中的五个化学反应中,属于氧化还原反应的是①和___________ (填序号)。
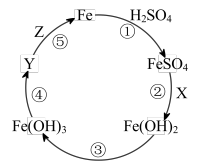
(2)实验二:在FeSO4溶液中滴加X溶液,可观察到溶液中产生白色沉淀,但又迅速变成灰绿色,最终变成红棕色。这是因为白色的氢氧化亚铁不稳定,其会与氧气、水等物质反应生成红棕色的氢氧化铁。
I.X的化学式是
II.要使实验二产生的氢氧化亚铁白色保持的时间长一些,可采取的措施
(3)实验二中最后得到的浊液通过过滤、
(4)工业上用Y与Z反应生产铁,反应⑤的化学方程式为
(5)已知在化学反应中,若有元素的化合价升高或降低,该化学反应可判定为氧化还原反应,则“铁的循环”中的五个化学反应中,属于氧化还原反应的是①和
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
名校
解题方法
【推荐2】“文明城市共创建,垃圾分类我先行”。我校化学兴趣小组进行垃圾分类社会实践活动时,在垃圾处理厂发现一些含铜锌合金的废料(主要含Cu、Zn)。查阅资料后,兴趣小组的同学们在老师的指导下,设计利用此铜锌合金的废料回收铜并制取ZnSO4晶体的工艺流程如图(反应条件已略去):
(2)加入稀硫酸之前要先将合金粉碎,目的是_____________________ 。
(3)步骤②向反应池中加入Zn粉,目的是与过量的硫酸反应,该反应属于_______ 反应(填基本反应类型);
(4)兴趣小组的同学们取此铜锌合金废料20g,通过上述工艺流程后得到ZnSO4晶体(不考虑含结晶水)质量为16.1g,则该废料中含锌的质量分数不超过_______ 。

| A.厨余垃圾 | B.有害垃圾 | C.可回收垃圾 | D.其他垃圾 |
(2)加入稀硫酸之前要先将合金粉碎,目的是
(3)步骤②向反应池中加入Zn粉,目的是与过量的硫酸反应,该反应属于
(4)兴趣小组的同学们取此铜锌合金废料20g,通过上述工艺流程后得到ZnSO4晶体(不考虑含结晶水)质量为16.1g,则该废料中含锌的质量分数不超过
您最近一年使用:0次
填空与简答-推断题
|
适中
(0.65)
名校
【推荐3】如图中A、B、C、D、E、F为六种初中化学常见的物质,其中B是胃液的主要成分,D可用于配制农药波尔多液,F为红棕色固体,各物质间的反应及部分转化关系如图所示(图中用“-”表示两种物质间能发生反应,用“→”表示一种物质能转化为另一种物质,部分反应物、生成物、反应条件已略去,有些反应需在溶液中进行)。
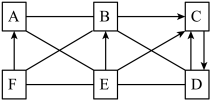
请回答下列问题:
(1)分别写出A、D物质的化学式A:_______ D:_______ 。
(2)写出E→B的化学方程式为_______ 。
(3)写出F与过量B反应的实验现象为_______ 。

请回答下列问题:
(1)分别写出A、D物质的化学式A:
(2)写出E→B的化学方程式为
(3)写出F与过量B反应的实验现象为
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐1】过氧化钙(CaO2)能杀菌消毒,广泛用于果蔬保鲜、空气净化、污水处理等领域。CaO2可由鸡蛋壳(含90%CaCO3)为原料,实验室可按以下流程制得:
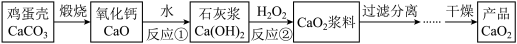
查阅资料:CaO2在潮湿空气及水中会缓慢放出O2,温度较高时会分解生成CaO和O2。
回答下列问题:
(1)鸡蛋壳属于_____ (填“纯净物”或“混合物”),煅烧前要把鸡蛋壳碾碎,其目的是_______ 。
(2)氧化钙俗称_______ ,反应①的化学方程式为_______ ,该反应属于_______ (填基本反应类型)。
(3)反应②需在低温条件下进行,主要原因是_______ 。
(4)过滤CaO2料浆时,玻璃棒的作用是_______ 。所用到的玻璃仪器是漏斗、玻璃棒、___ 。
(5)结合以上信息,保存CaO2需注意的是_______ 。
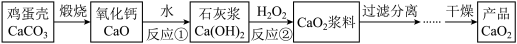
查阅资料:CaO2在潮湿空气及水中会缓慢放出O2,温度较高时会分解生成CaO和O2。
回答下列问题:
(1)鸡蛋壳属于
(2)氧化钙俗称
(3)反应②需在低温条件下进行,主要原因是
(4)过滤CaO2料浆时,玻璃棒的作用是
(5)结合以上信息,保存CaO2需注意的是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
名校
解题方法
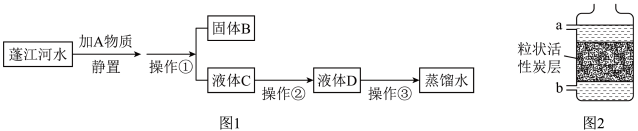
【推荐2】重庆实验外国语学校一初三化学兴趣小组收集到一瓶浑浊的嘉陵江水,并在化学实验室对江水进行净化,最终制成蒸馏水。其实验过程如图所示,请回答以下问题:
(2)操作②应选用图2所示装置,该操作中待净化的水应该从______ (填“a”或“b”)端通入。
(3)操作③能够降低水的硬度,而在生活中可以采用______ 方法来降低水的硬度。
(4)在自来水厂的净水过程中,氯气( )是常用的消毒剂。工业上,通过电解食盐水可制得氯气,反应物为食盐水中的氯化钠和水,生成物除了氯气,还有氢氧化钠和相对分子质量最小的气体,该反应的化学反应方程式为
)是常用的消毒剂。工业上,通过电解食盐水可制得氯气,反应物为食盐水中的氯化钠和水,生成物除了氯气,还有氢氧化钠和相对分子质量最小的气体,该反应的化学反应方程式为______
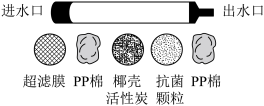
(5)“生命吸管”是一种户外净水装置(如下图),其中椰壳活性炭消除异味、提升口感,利用的是活性炭的______ 性。
| A.带铁圈的铁架台 |
| B.酒精灯 |
| C.漏斗 |
| D.玻璃棒 |
| E.量筒 |
| F.烧杯 |
(2)操作②应选用图2所示装置,该操作中待净化的水应该从
(3)操作③能够降低水的硬度,而在生活中可以采用
(4)在自来水厂的净水过程中,氯气(
 )是常用的消毒剂。工业上,通过电解食盐水可制得氯气,反应物为食盐水中的氯化钠和水,生成物除了氯气,还有氢氧化钠和相对分子质量最小的气体,该反应的化学反应方程式为
)是常用的消毒剂。工业上,通过电解食盐水可制得氯气,反应物为食盐水中的氯化钠和水,生成物除了氯气,还有氢氧化钠和相对分子质量最小的气体,该反应的化学反应方程式为(5)“生命吸管”是一种户外净水装置(如下图),其中椰壳活性炭消除异味、提升口感,利用的是活性炭的
您最近一年使用:0次