解题方法
1 . 请你结合下列装置图回答问题。

(1)写出a的仪器名称______ ;
(2)海口市五公祠中五公铜像,随着时间推移,铜像表面有一部分覆盖着一层绿色固体。小强带着浓厚的兴趣对绿色固体的元素组成进行研究。
查阅资料: 金属铜长时间放置在空气中,与氧气等物质发生复杂的化学反应,形成“铜绿”。空气中氮气和稀有气体的化学性质稳定,常温下难与其他物质反应。
猜想与假设:经过思考和推理,小强认为“铜绿”的组成元素可能是铜、氧、氢、碳元素。
实验过程:小强按实验设计连接A→______ →______ 装置(填装置代号),在检查装置气密性后进行相关实验。请你帮助小强完成下列实验报告:
(3)反思与应用:通过实验探井得知“铜绿”是由铜、氧、氢、碳四种元素组成。大多数金属的锈蚀与铁、铜的锈蚀相似,金属的锈蚀给人类带来了巨大的损失,请写出防止金属锈蚀的一种方法________ 。

(1)写出a的仪器名称
(2)海口市五公祠中五公铜像,随着时间推移,铜像表面有一部分覆盖着一层绿色固体。小强带着浓厚的兴趣对绿色固体的元素组成进行研究。
查阅资料: 金属铜长时间放置在空气中,与氧气等物质发生复杂的化学反应,形成“铜绿”。空气中氮气和稀有气体的化学性质稳定,常温下难与其他物质反应。
猜想与假设:经过思考和推理,小强认为“铜绿”的组成元素可能是铜、氧、氢、碳元素。
实验过程:小强按实验设计连接A→
| 实验操作 | 实验现象 | 实验结论 |
| 实验Ⅰ:将一定量绿色固体装入反应容器中,进行实验 | 绿色固体变黑色;白色无水硫酸铜变蓝色;澄清的石灰水变浑浊 | 产物中有 |
| 实验Ⅱ:取反应后的黑色固体放入试管中,加入足量的稀硫酸 | 黑色固体完全溶解,溶液变蓝色 | 黑色固体是氧化铜反应的化学方程式: |
(3)反思与应用:通过实验探井得知“铜绿”是由铜、氧、氢、碳四种元素组成。大多数金属的锈蚀与铁、铜的锈蚀相似,金属的锈蚀给人类带来了巨大的损失,请写出防止金属锈蚀的一种方法
您最近一年使用:0次
解题方法
2 . 松花蛋是我国特有的一种传统美食。学习小组同学进行了“松花蛋制作”的项目研究。同学们品尝松花蛋时,发现松花蛋略有涩味,加入食醋涩味减轻,同学们联想到碱性物质通常有涩味,推测松花蛋中含有碱性物质。
【实验验证】取适量松花蛋粉(用于制作松花蛋泥的原料),加入适量水,搅拌、过滤。测得滤液pH=12,证明滤液中含有碱性物质。
【提出问题】滤液中的碱性物质是什么?
【查阅资料】松花蛋粉中主要含有生石灰、食盐、纯碱等。
【分析推理】
(1)松花蛋粉加水调和时发生如下反应: ;
;___________ (写化学方程式)。
【猜想与假设】同学们根据上述分析推理,对滤液中的碱性物质做出猜想:
猜想一:只有NaOH; 猜想二:NaOH和Ca(OH)2; 猜想三:NaOH和Na2CO3
【实验探究】
(2)
通过以上探究,同学们找到了松花蛋粉加水后滤液显碱性的原因,寻到了涩味的缘由。
【反思总结】
(3)判断化学反应后溶液的成分时,既要考虑生成物、又要考虑_________ 。
【项目拓展】
(4)为了使松花蛋产生美丽的松花,传统工艺中加入密陀僧(主要成分为氧化铅),目前密陀僧已被硫酸锌取代,制得无铅松花蛋。从人体健康角度分析这一工艺改进的原因是________ 。
【实验验证】取适量松花蛋粉(用于制作松花蛋泥的原料),加入适量水,搅拌、过滤。测得滤液pH=12,证明滤液中含有碱性物质。
【提出问题】滤液中的碱性物质是什么?
【查阅资料】松花蛋粉中主要含有生石灰、食盐、纯碱等。
【分析推理】
(1)松花蛋粉加水调和时发生如下反应:
 ;
;【猜想与假设】同学们根据上述分析推理,对滤液中的碱性物质做出猜想:
猜想一:只有NaOH; 猜想二:NaOH和Ca(OH)2; 猜想三:NaOH和Na2CO3
【实验探究】
(2)
| 实验操作 | 实验现象 | 实验结论 |
| 取滤液少许,向其中加入氯化钙溶液 | 猜想二正确 | |
| 另取滤液少许,向其中加入 | 产生白色沉淀 |
【反思总结】
(3)判断化学反应后溶液的成分时,既要考虑生成物、又要考虑
【项目拓展】
(4)为了使松花蛋产生美丽的松花,传统工艺中加入密陀僧(主要成分为氧化铅),目前密陀僧已被硫酸锌取代,制得无铅松花蛋。从人体健康角度分析这一工艺改进的原因是
您最近一年使用:0次
解题方法
3 . 观察和推理是重要的学习方法。
利用图1装置进行实验,烧瓶内是滴有酚酞的氢氧化钠溶液,实验时将注射器内的液体逐滴注入烧瓶内,用pH传感器等电子设备采集信息,测得烧瓶中溶液的pH随时间变化的关系如图2所示。

回答下列问题:
(1)图2中c点所示溶液中含有的溶质是______ 。
(2)盐酸与氢氧化钠恰好完全反应时,对应图2中______ 点。
(3)能说明盐酸和氢氧化钠发生化学反应的现象是:①______ 、②______ 。
(4)测量溶液的温度,氢氧化钠和盐酸反应时放出热量。有同学认为,反应中溶液温度的变化也可能是由溶液稀释引起的。为了验证这一想法,在室温下应进行的实验是:
实验1:______ 。
实验2:______ 。
实验3:取10mL10%的NaOH溶液与10mL10%的盐酸混合,测量溶液温度的变化。经实验测量,溶液稀释时温度无明显变化。
利用图1装置进行实验,烧瓶内是滴有酚酞的氢氧化钠溶液,实验时将注射器内的液体逐滴注入烧瓶内,用pH传感器等电子设备采集信息,测得烧瓶中溶液的pH随时间变化的关系如图2所示。

回答下列问题:
(1)图2中c点所示溶液中含有的溶质是
(2)盐酸与氢氧化钠恰好完全反应时,对应图2中
(3)能说明盐酸和氢氧化钠发生化学反应的现象是:①
(4)测量溶液的温度,氢氧化钠和盐酸反应时放出热量。有同学认为,反应中溶液温度的变化也可能是由溶液稀释引起的。为了验证这一想法,在室温下应进行的实验是:
实验1:
实验2:
实验3:取10mL10%的NaOH溶液与10mL10%的盐酸混合,测量溶液温度的变化。经实验测量,溶液稀释时温度无明显变化。
您最近一年使用:0次
解题方法
4 . NaOH固体长时间露置在空气中易吸收CO2变质而生成Na2CO3。
【提出问题】测定长期存放的氢氧化钠中Na2CO3的质量分数。
【实验设计】通过测定碳酸钠与稀盐酸反应生成CO2的质量可求出Na2CO3的质量,从而得到Na2CO3的质量分数。
【实验过程】用气密性良好的装置(如图)装好样品,然后通一会儿N2后关闭止水夹,再打开分液漏斗活塞,待甲装置中反应结束后打开止水夹再通入一会儿N2。(碱石灰是氧化钙和氢氧化钠的混合物,可以吸收CO2和H2O。实验中碱石灰和浓硫酸均足量。)
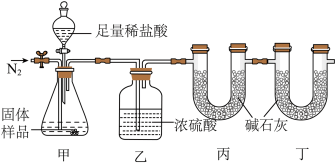
【分析推理】
(1)试写出甲中发生反应的化学方程式____ 。
(2)乙中浓硫酸的作用是____ 。
(3)反应开始时通入N2的目的是____ ,反应结束后通入N2的目的是____ 。或实验中使用的盐酸浓度过大,则测得的Na2CO3的质量分数____ (填“偏大”或“偏小”或“不变”或“无法确定”)
(4)丁装置的作用是____ 。
(5)测定Na2CO3的含量需要测定两个物理量,其中一个物理量为样品的质量m1。
①另一个物理量为____ (填序号)。
A.滴下的稀盐酸质量 B.反应前后乙装置增加的质量
C.反应前后丙装置增加的质量 D.反应前后丁装置增加的质量
②若上述①中所选的物理量为m2,则样品中Na2CO3的质量分数为____ 。(列出含有m1、m2的计算式即可)
【拓展反思】实验室保存氢氧化钠固体要注意的问题是____ 。
【提出问题】测定长期存放的氢氧化钠中Na2CO3的质量分数。
【实验设计】通过测定碳酸钠与稀盐酸反应生成CO2的质量可求出Na2CO3的质量,从而得到Na2CO3的质量分数。
【实验过程】用气密性良好的装置(如图)装好样品,然后通一会儿N2后关闭止水夹,再打开分液漏斗活塞,待甲装置中反应结束后打开止水夹再通入一会儿N2。(碱石灰是氧化钙和氢氧化钠的混合物,可以吸收CO2和H2O。实验中碱石灰和浓硫酸均足量。)

【分析推理】
(1)试写出甲中发生反应的化学方程式
(2)乙中浓硫酸的作用是
(3)反应开始时通入N2的目的是
(4)丁装置的作用是
(5)测定Na2CO3的含量需要测定两个物理量,其中一个物理量为样品的质量m1。
①另一个物理量为
A.滴下的稀盐酸质量 B.反应前后乙装置增加的质量
C.反应前后丙装置增加的质量 D.反应前后丁装置增加的质量
②若上述①中所选的物理量为m2,则样品中Na2CO3的质量分数为
【拓展反思】实验室保存氢氧化钠固体要注意的问题是
您最近一年使用:0次
2022-06-18更新
|
111次组卷
|
2卷引用:2022年福建省南平市初中毕业班综合练习化学试题(二)
5 . 小刚和小洁以“化学反应中,反应物和生成物的质量关系”为课题进行科学探究,请填写以下探究过程中的空格:(提示:稀盐酸与石灰石反应生成二氧化碳和水、氯化钙;与氢氧化钠生成水和氯化钠)
(1)写出稀盐酸与氢氧化钠反应的化学方程式_________
提出假设:化学反应中,反应物的总质量与生成物的总质量相等。
研究方法:分析推理,查阅资料,实验探究。
进行实验:小刚设计的实验装置和选用药品如图A所示,小洁的如图B所示,他们在反应前后都进行了规范的操作,准确的称量和细致的观察。

(2)实验结论:通过实验,小刚认为:在化学反应中,生成物的总质量与反应物的总质量不相等,小洁认为:在化学反应中,生成物的总质量与反应物的总质量相等,你认为结论正确的是_____ ,请你谈谈导致另一种结论错误的原因:_________ 。
(3)结论分析:请从原子的角度,简要分析你认为正确的结论:_______ 。
(1)写出稀盐酸与氢氧化钠反应的化学方程式
提出假设:化学反应中,反应物的总质量与生成物的总质量相等。
研究方法:分析推理,查阅资料,实验探究。
进行实验:小刚设计的实验装置和选用药品如图A所示,小洁的如图B所示,他们在反应前后都进行了规范的操作,准确的称量和细致的观察。

(2)实验结论:通过实验,小刚认为:在化学反应中,生成物的总质量与反应物的总质量不相等,小洁认为:在化学反应中,生成物的总质量与反应物的总质量相等,你认为结论正确的是
(3)结论分析:请从原子的角度,简要分析你认为正确的结论:
您最近一年使用:0次
解题方法
6 . 镁条能在氧气中燃烧,镁条能不能在其它气体中燃烧呢?
为探究此问题,小平同学用坩埚钳夹持镁条在空气中加热后,伸入盛满氯气(C12)的集气瓶内,看到镁条剧烈燃烧,发出耀眼白光,产生白烟,并放出大量的热。在此过种中,小平运用的科学方法有________ 。推理也是常用的一种科学方法,是根据乙有的知识和经验,对观察的现象做出解释,小平根据已有的知识,推断产生的白烟是氯化镁固体,她做出推理的理论依据是_____________ 。
为探究此问题,小平同学用坩埚钳夹持镁条在空气中加热后,伸入盛满氯气(C12)的集气瓶内,看到镁条剧烈燃烧,发出耀眼白光,产生白烟,并放出大量的热。在此过种中,小平运用的科学方法有
您最近一年使用:0次



