解题方法
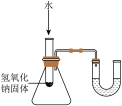
1 . 下列实验,不能 达到实验目的的是
A.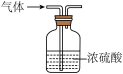 干燥氧气 干燥氧气 | B.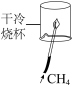 验证甲烷中含有氢元素 验证甲烷中含有氢元素 |
C.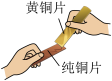 比较黄铜和纯铜的硬度 比较黄铜和纯铜的硬度 | D. 验证质量守恒定律 验证质量守恒定律 |
您最近一年使用:0次
名校
解题方法
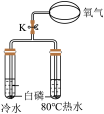
2 . 实验设计的严谨性会直接影响实验结论的准确性。下列设计不能达到实验目的的是
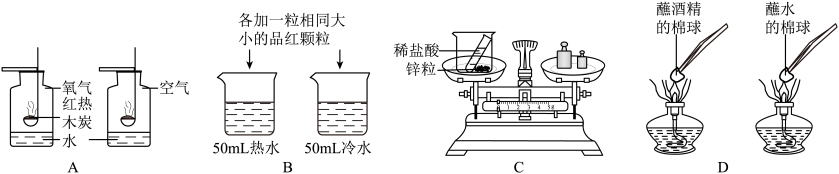
| A.探究木炭燃烧的剧烈程度与氧气浓度有关 | B.探究温度对分子运动速率的影响 |
| C.验证质量守恒定律 | D.探究燃烧的条件之一是可燃物 |
您最近一年使用:0次
解题方法
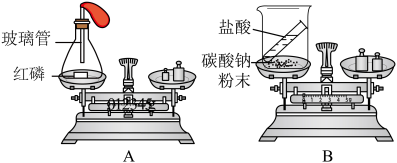
3 . 某化学小组同学用如图所示的实验探究质量守恒定律;________________ ;
(2)在红磷燃烧时,小气球会膨胀,红磷燃烧完并冷却后,小气球会变得比实验前更瘪.小气球变得更瘪的原因是________________ ;
(3)B实验中天平不能保持平衡的原因是________________ ;
(2)在红磷燃烧时,小气球会膨胀,红磷燃烧完并冷却后,小气球会变得比实验前更瘪.小气球变得更瘪的原因是
(3)B实验中天平不能保持平衡的原因是
您最近一年使用:0次
解题方法
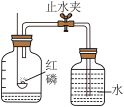
4 . 下列实验不是利用气压差原理达到目的的是
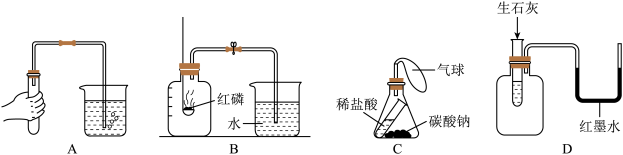
| A.检查装置气密性 | B.测定空气中氧气含量 |
| C.验证质量守恒定律 | D.验证生石灰与水是放热反应 |
您最近一年使用:0次
名校
解题方法
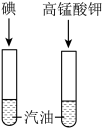
5 . 下列实验方案与其对应实验目的或结论正确的是
|
|
|
|
| A.验证质量守恒定律 | B.说明氢氧化钠与水反应放热 | C.探究可燃物燃烧的条件 | D.说明同一种物质在不同溶剂中的溶解性不同 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
6 . 下列实验能达到实验目的的是
| A | B | C | D |
|
|
|
|
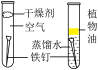
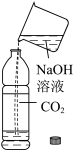
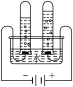
| 测定空气中O2含量 | 验证质量守恒定律 | 验证铁生需要O2 | 验证CO2能和NaOH反应 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
7 . 如图,下列实验方案能达到实验目的的是
A.探究氧气浓度对燃烧剧烈程度的影响 |
B.验证质量守恒定律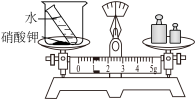 |
C.检验蜡烛中是否含有氢元素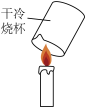 |
D.除去NaCl溶液中的Na2SO4 |
您最近一年使用:0次
解题方法
8 . 读史可知兴替,冶金展现智慧。
(1)晋朝葛洪《抱朴子》中记载“丹砂烧之成水银,积变又还成丹砂”。文中“积变”过程发生的是_______ (填“物理”或“化学)变化。
(2)《宋史》中提到用胆水浸铁炼铜,并有“用铁二斤四两得铜一斤”的记载。
①“胆水”指硫酸铜溶液,浸铁炼铜的化学方程式是______ 。
②斤是我国古代常用的质量单位,一斤为十六两。欲得铜一斤,所用铁中参加反应的铁的质量是______ 两。
(3)19世纪末,霍尔在电解熔融氧化铝制备金属铝的过程中,发现冰晶石在电解过程中不被分解且会影响电解的进行,如表所示。
①冰晶石(Na3AlF6)中氟元素的化合价是_______ 。
②电解时,加入冰晶石可起到的作用是______ 。
(1)晋朝葛洪《抱朴子》中记载“丹砂烧之成水银,积变又还成丹砂”。文中“积变”过程发生的是
(2)《宋史》中提到用胆水浸铁炼铜,并有“用铁二斤四两得铜一斤”的记载。
①“胆水”指硫酸铜溶液,浸铁炼铜的化学方程式是
②斤是我国古代常用的质量单位,一斤为十六两。欲得铜一斤,所用铁中参加反应的铁的质量是
(3)19世纪末,霍尔在电解熔融氧化铝制备金属铝的过程中,发现冰晶石在电解过程中不被分解且会影响电解的进行,如表所示。
| 是否加冰晶石 | 加冰晶石 | 不加冰晶石 |
| 熔化氧化铝的温度/℃ | 980 | 2050 |
②电解时,加入冰晶石可起到的作用是
您最近一年使用:0次
解题方法
9 . 下列实验中,实验装置与现象、结论完全正确的是
| 选项 | A | B | C | D |
| 装置 |
|
|
|
|
| 现象 | 白烟引燃了烛芯 | 铁钉表面有红色固体生成,天平依然平衡 | 正极产生的气体能使带火星木条复燃,负极产生的气体能燃烧发出淡蓝色火焰 | 水中白磷燃烧 |
| 结论 | 白烟可能是二氧化碳 | 证明化学反应前后质 量守恒 | 水是由氢元素和氧元 素组成的 | 证明燃烧需要温度达到着火点 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
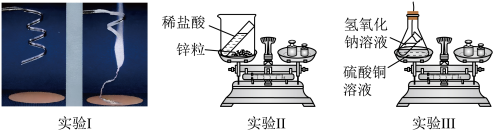
10 . 某课外兴趣小组的同学设计了如图四个实验来验证质量守恒定律。
实验Ⅱ:将装有稀盐酸的小试管放入装有锌粒的烧杯中,称量,然后将盐酸与锌粒接触,生成氢气和氯化锌,过一会在称量。
实验Ⅲ:将装有氢氧化钠溶液的试管放入盛有硫酸铜的锥形瓶中,并在锥形瓶口塞上橡皮塞,称量,然后设法将两种溶液接触,过一会再称量。
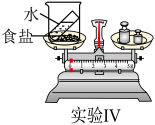
实验Ⅳ:将装水的试管放入盛有食盐的烧杯中,称量,然后设法将两种物质接触,过一会再称量。
(1)在实验I中,反应后的质量比反应前明显增加,请用质量守恒定律加以解释_______ 。
(2)实验Ⅱ中天平指针如何变化_______ (“向左偏”,或“向右偏”,或“指在中间”),原因是_______ 。
(3)实验Ⅳ中天平指针如何变化_______ (“向左偏”,或“向右偏”,或“指在中间”)。
(4)这三个实验中,实验Ⅲ正确反映了反应物与生成物之间的质量关系。请从微观的角度解释反应前后质量相等的原因_______ 。该反应表示为:2NaOH+CuSO4=Cu(OH)2↓+X,X的化学式为_______ 。
(5)以上四个实验,能用质量守恒定律来解释的是( ) 。
(6)根据质量守恒定律可知,化学反应前后一定不变的是_______。
实验Ⅱ:将装有稀盐酸的小试管放入装有锌粒的烧杯中,称量,然后将盐酸与锌粒接触,生成氢气和氯化锌,过一会在称量。
实验Ⅲ:将装有氢氧化钠溶液的试管放入盛有硫酸铜的锥形瓶中,并在锥形瓶口塞上橡皮塞,称量,然后设法将两种溶液接触,过一会再称量。
实验Ⅳ:将装水的试管放入盛有食盐的烧杯中,称量,然后设法将两种物质接触,过一会再称量。
(1)在实验I中,反应后的质量比反应前明显增加,请用质量守恒定律加以解释
(2)实验Ⅱ中天平指针如何变化
(3)实验Ⅳ中天平指针如何变化
(4)这三个实验中,实验Ⅲ正确反映了反应物与生成物之间的质量关系。请从微观的角度解释反应前后质量相等的原因
(5)以上四个实验,能用质量守恒定律来解释的是
(6)根据质量守恒定律可知,化学反应前后一定不变的是_______。
| A.分子的种类 |
| B.原子的种类 |
| C.元素的种类 |
| D.物质的种类 |
| E.元素的质量 |
| F.原子的质量 |
| G.分子的个数 |
您最近一年使用:0次