名校
解题方法
1 . 推理和归纳是化学学习和研究中常用的思维方法,下列推理正确的是
| A.单质是由一种元素组成的物质,所以一种元素组成的物质一定是单质 |
| B.分子、原子都是不带电的微粒,但不带电的微粒不一定都是分子、原子 |
| C.氦原子和镁原子的最外层电子数相同,则氦原子和镁原子的化学性质相似 |
| D.二氧化锰是过氧化氢分解的催化剂,所以二氧化锰可以作任何反应的催化剂 |
您最近半年使用:0次
名校
解题方法
2 . 元素周期表是学习和研究化学的重要工具。如表是元素周期表的一部分。
(1)查阅上表可知,氟的相对原子质量为_______ 。
(2)硅元素与磷元素的本质区别是_______ 。
(3)第11号元素与第17号元素组成的化合物是_______ (填化学式),构成该物质的微粒是_______ (选填“分子”、“原子”或“离子”)。
(4)下列各组元素具有相似化学性质的是_____(填字母序号)。
| 族 周期 | IA | 0 | ||||||
| 1 | 1H 1.008 | ⅡA | ⅢA | IVA | VA | VIA | VIIA | 2He 4.003 |
| 2 | 3Li 6.941 | 4Be 9.012 | 5B 10.81 | 6C 12.01 | 7N 14.01 | 8O 16.00 | 9F 19.00 | 10H 20.81 |
| 3 | 11Na 22.99 | 12Mg 24.31 | 13Al 26.98 | 14Si 28.09 | 15P 30.97 | 16S 32.06 | 17Cl 35.45 | 18Ar 39.95 |
(2)硅元素与磷元素的本质区别是
(3)第11号元素与第17号元素组成的化合物是
(4)下列各组元素具有相似化学性质的是_____(填字母序号)。
| A.C和Ne | B.He和Mg | C.Al和Si | D.F和Cl |
您最近半年使用:0次
名校
解题方法
3 . 下列现象或事实,用分子、原子的相关知识加以解释,其中错误的是
| 现象或事实 | 解释 | |
| A | 稀有气体化学性质稳定 | 原子最外层电子达到相对稳定结构 |
| B | 水和过氧化氢化学性质不同 | 构成物质的分子不同 |
| C | 降温能使水结成冰 | 低温导致水分子静止不动 |
| D | 氧气加压降温可以变成液氧 | 分子之间有间隔 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
23-24九年级下·山东济宁·阶段练习
解题方法
4 . 在宏观、微观和符号之间建立联系是学习化学的重要思维方式。根据下列原子结构示意图,回答问题。______ 。
(2)在化学反应中,锂原子容易______ 电子(填“得到”或“失去”)。
(3)锂和钠属于不同种元素,是因为它们的原子中______ 不同。
(4)在盛有水的烧杯中滴入几滴酚酞试液,把一块绿豆大小的金属钠投入烧杯中,观察到钠浮在水面上,熔化成闪亮的小球且在水面上迅速游动,发出“嘶嘶”的响声,反应后溶液呈红色,经测定知金属钠与水反应生成氢气和另外一种物质,写出金属钠与水反应的化学方程式______ 。
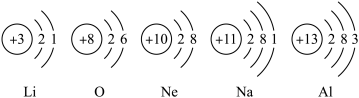
(2)在化学反应中,锂原子容易
(3)锂和钠属于不同种元素,是因为它们的原子中
(4)在盛有水的烧杯中滴入几滴酚酞试液,把一块绿豆大小的金属钠投入烧杯中,观察到钠浮在水面上,熔化成闪亮的小球且在水面上迅速游动,发出“嘶嘶”的响声,反应后溶液呈红色,经测定知金属钠与水反应生成氢气和另外一种物质,写出金属钠与水反应的化学方程式
您最近半年使用:0次
2024·安徽合肥·一模
解题方法
5 . “中国高铁”已成为我国外交的新名片,高铁车身主要采用镍铬奥氏体不锈钢制成,如图为铬元素在元素周期表中的信息及原子结构示意图,下列说法不正确的是
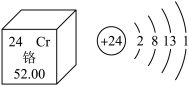
| A.铬元素位于第四周期 | B.铬原子的中子数为24 |
C.若碳12原子的质量为a,则铬原子的质量为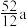 | D.铬原子在化学反应中易失去电子 |
您最近半年使用:0次
解题方法
6 . 图1是四种元素在元素周期表中的部分信息,回答下列问题:___________ 。
(2)钠原子在化学反应中易___________ (选填“得到”或“失去”)电子。
(3)铝元素的一种微粒结构示意图如图2,该微粒的符号为___________ 。
(4)钠、铝、氯位于同一周期的原因是___________ 。
(5)由钠和氯形成的化合物的化学式是___________ 。

(2)钠原子在化学反应中易
(3)铝元素的一种微粒结构示意图如图2,该微粒的符号为
(4)钠、铝、氯位于同一周期的原因是
(5)由钠和氯形成的化合物的化学式是
您最近半年使用:0次
解题方法
7 . 元素周期表是学习化学的重要工具,下表为元素周期表中部分元素的相关信息,利用下表回答相关问题。___________ (填“质子数”或“电子层数”或“最外层电子数”)相同;
(2)He和Mg的化学性质___________ (填“相似”或“不相似”);
(3)钠离子核外电子排布与___________ (填元素名称)原子核外电子排布相同;
(4)一个 含有
含有___________ 个电子;
(5)一般地说,电子层数相同的原子,原子的半径随原子序数的递增而减小(稀有气体除外);最外层电子数相同的原子,原子的半径随电子层数的增加而增大。请比较:氮原子半径___________ (填“>”或“<”)磷原子半径。

(2)He和Mg的化学性质
(3)钠离子核外电子排布与
(4)一个
 含有
含有(5)一般地说,电子层数相同的原子,原子的半径随原子序数的递增而减小(稀有气体除外);最外层电子数相同的原子,原子的半径随电子层数的增加而增大。请比较:氮原子半径
您最近半年使用:0次
名校
解题方法
8 . 有下列五种粒子的结构示意图。回答下列问题:________ 种元素,属同种元素的是_______ 。(填字母序号,下同)。
(2)E原子在化学反应中易___________ (填得到或失去)电子。
(3)A粒子中的质子数为___________ ,A离子的符号为___________ 。
(4)上述五种粒子中,最外层电子数相同的原子是___________ 。
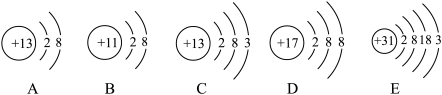
(2)E原子在化学反应中易
(3)A粒子中的质子数为
(4)上述五种粒子中,最外层电子数相同的原子是
您最近半年使用:0次
2024-04-21更新
|
59次组卷
|
2卷引用:广西南宁市三美学校2023-2024学年八年级下学期期中学业质量监测化学试卷
解题方法
9 . 元素周期表是学习和研究化学的重要工具。图一是元素周期表的一部分,图二是34号元素硒(元素符号为Se)的原子结构示意图:
(1)原子序数为9的元素的相对原子质量为_______ ,它属于______ (填“金属”或“非金属”)元素,在化学反应中容易______ (填“得到”或“失去”)电子。
(2)钠离子的质子数是11,则钠离子的核外电子数是_______ 。
(3)根据图二所示,请推测硒元素在元素周期表中的位置应在______ (填元素符号)的正下方。
(4)由第7号元素和第12号元素的原子形成化合物的化学式为_______ 。

(1)原子序数为9的元素的相对原子质量为
(2)钠离子的质子数是11,则钠离子的核外电子数是
(3)根据图二所示,请推测硒元素在元素周期表中的位置应在
(4)由第7号元素和第12号元素的原子形成化合物的化学式为
您最近半年使用:0次
名校
解题方法
10 . 铥离子(Tm3+)具有优良的发光性能,故可用作光纤激光器。稀土元素Tm在元素周期表中的信息如图,下列有关Tm的判断正确的是
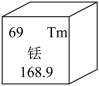
| A.铥属于金属元素 |
| B.一个铥原子易得到3个电子 |
| C.原子的中子数为69 |
| D.相对原子质量为168.9g |
您最近半年使用:0次



