解题方法
1 . 下列推理正确的是
| A.氢氧化钠溶液能使酚酞溶液变红,则碱一定能使酚酞溶液变红 |
| B.同种元素质子数相同,则质子数相同的原子一定是同种元素 |
| C.活泼金属与稀硫酸反应放出气体,则与酸反应放出气体的物质一定是活泼金属 |
| D.复分解反应中元素的化合价都不变,则元素化合价不变的反应一定是复分解反应 |
您最近一年使用:0次
解题方法
2 . 使用天然气做饭,点火后,发现炉火火焰呈现黄色,锅底出现黑色,这时就需要调大灶具的进风口;使用完毕,关闭开关,火焰熄灭。下列说法错误的是
| A.关闭开关火焰熄灭,原因是温度降到了着火点以下 |
| B.点火是为了使温度达到天然气的着火点 |
| C.天然气会燃烧,因为它是可燃物 |
| D.调大进风口的目的是提供足够的空气,使燃烧更充分 |
您最近一年使用:0次
解题方法
3 . 化肥对促进农作物增产具有重要作用。下列物质属于氮肥的是
| A.KCl | B. | C.磷矿粉 | D. |
您最近一年使用:0次
名校
解题方法
4 . 下列物质在氧气中燃烧能生成黑色固体的是
| A.硫 | B.红磷 | C.铁丝 | D.木炭 |
您最近一年使用:0次
名校
5 . 学校环保小组检测发现实验室的某酸性废液中含有 。该小组取
。该小组取 废液,为了测定废液中
废液,为了测定废液中 的质量分数,逐滴加入
的质量分数,逐滴加入 溶液至过量。测得生成沉淀(无其它沉淀)的质量与所加
溶液至过量。测得生成沉淀(无其它沉淀)的质量与所加 溶液的质量关系如图所示:
溶液的质量关系如图所示:______ g。
(2)计算废液中 的质量分数。
的质量分数。
 。该小组取
。该小组取 废液,为了测定废液中
废液,为了测定废液中 的质量分数,逐滴加入
的质量分数,逐滴加入 溶液至过量。测得生成沉淀(无其它沉淀)的质量与所加
溶液至过量。测得生成沉淀(无其它沉淀)的质量与所加 溶液的质量关系如图所示:
溶液的质量关系如图所示: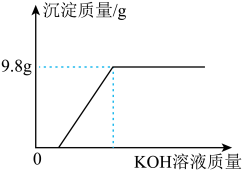
(2)计算废液中
 的质量分数。
的质量分数。
您最近一年使用:0次
名校
解题方法
6 . 化学兴趣小组学习完复分解反应后,进行酸碱盐之间反应的项目式实验探客。
【实验一】小组同学做了如图所示的三个实验:
【查阅资料】 溶液呈磩性;
溶液呈磩性; 溶液呈中性,且
溶液呈中性,且 有毒。
有毒。 的俗称是
的俗称是______ 。
(2)写出试管②中反应的化学方程式______ 。
(3)试管③反应的微观实质是______ (填离子名称)和碳酸根离子结合生成水分子和二氧化碳分子。
【实验二】甲同学完成试管①和②中的两个实验后,接着进行如图探究:______ (填化学式)。
【实验三】
(5)乙同学把沉淀 混合后加入过量的稀硝酸,观察到的实验现象是
混合后加入过量的稀硝酸,观察到的实验现象是______ ,充分反应后所得溶液中含有的离子是______ 。
【处理废液】
(6)实验完毕后,甲同学将滤液 倒入废液缸。为了使废液安全排放,向其中加入适量的______(填序号),对废液进行处理。
倒入废液缸。为了使废液安全排放,向其中加入适量的______(填序号),对废液进行处理。
【实验一】小组同学做了如图所示的三个实验:
【查阅资料】
 溶液呈磩性;
溶液呈磩性; 溶液呈中性,且
溶液呈中性,且 有毒。
有毒。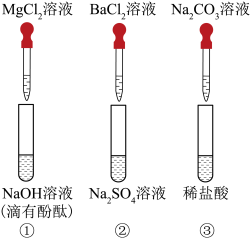
 的俗称是
的俗称是(2)写出试管②中反应的化学方程式
(3)试管③反应的微观实质是
【实验二】甲同学完成试管①和②中的两个实验后,接着进行如图探究:
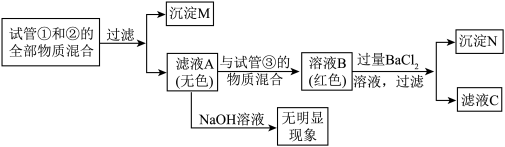
【实验三】
(5)乙同学把沉淀
 混合后加入过量的稀硝酸,观察到的实验现象是
混合后加入过量的稀硝酸,观察到的实验现象是【处理废液】
(6)实验完毕后,甲同学将滤液
 倒入废液缸。为了使废液安全排放,向其中加入适量的______(填序号),对废液进行处理。
倒入废液缸。为了使废液安全排放,向其中加入适量的______(填序号),对废液进行处理。A. 溶液 溶液 | B. 溶液 溶液 | C.稀硝酸 | D. 溶液 溶液 |
您最近一年使用:0次
名校
解题方法
7 . 如图为实验室常用仪器和装置的示意图,根据题意回答问题。______ 。
(2)用装置A制取氧气,反应的化学方程式为______ 。
(3)用装置B制取氢气,反应的化学方程式为______ 。
(4)用装置E收集二氧化碳,则气体从______ 端(填“b”或“c”)进入。
(5)装置 可用来测量生成
可用来测量生成 的体积,其中在水面上放一层植物油的目的是
的体积,其中在水面上放一层植物油的目的是______ 。
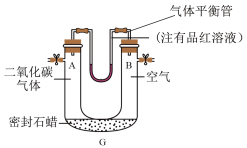
(6)装置G可探究二氧化碳对环境温度的影响。太阳照射装置一段时间后,观察到气体平衡管中液面______ 的现象能证明二氧化碳比空气的吸热效果更好。
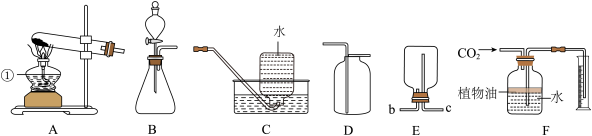
(2)用装置A制取氧气,反应的化学方程式为
(3)用装置B制取氢气,反应的化学方程式为
(4)用装置E收集二氧化碳,则气体从
(5)装置
 可用来测量生成
可用来测量生成 的体积,其中在水面上放一层植物油的目的是
的体积,其中在水面上放一层植物油的目的是(6)装置G可探究二氧化碳对环境温度的影响。太阳照射装置一段时间后,观察到气体平衡管中液面
您最近一年使用:0次
名校
解题方法
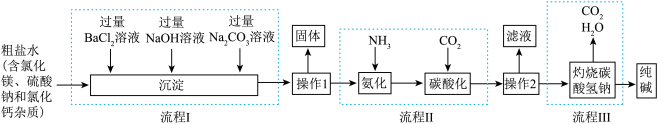
8 . 某化学小组参观制碱厂后,绘制了该厂生产纯碱的工艺流程图,据图回答。
【查阅资料】①该厂采用“侯氏制碱法”生产的化工产品为纯碱和氯化铵
②生产原料粗盐中含有少量可溶性杂质: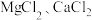 和
和
③生产原理:
⑤在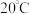 时碳酸氢钠的溶解度为
时碳酸氢钠的溶解度为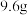 ,氯化铵的溶解度为
,氯化铵的溶解度为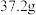
______ 。
(2)流程I中加入过量 溶液的目的是
溶液的目的是______ 。
(3)流程II中先通入氨气,后通二氧化碳的作用是______ 。
(4)工业生产纯碱的流程中,碳酸化时溶液中析出碳酸氢钠而没有析出氯化铵的原因是______ 。
(5)流程III中灼烧碳酸氢钠的化学方程式为______ 。
【查阅资料】①该厂采用“侯氏制碱法”生产的化工产品为纯碱和氯化铵
②生产原料粗盐中含有少量可溶性杂质:
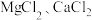 和
和
③生产原理:

⑤在
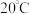 时碳酸氢钠的溶解度为
时碳酸氢钠的溶解度为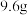 ,氯化铵的溶解度为
,氯化铵的溶解度为
(2)流程I中加入过量
 溶液的目的是
溶液的目的是(3)流程II中先通入氨气,后通二氧化碳的作用是
(4)工业生产纯碱的流程中,碳酸化时溶液中析出碳酸氢钠而没有析出氯化铵的原因是
(5)流程III中灼烧碳酸氢钠的化学方程式为
您最近一年使用:0次
名校
解题方法
9 . 阅读科普短文,回答相关问题。
制氢的技术有多种,其中煤气化制氢约占 、天然气重整制氢约占
、天然气重整制氢约占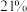 ,电解水制氢约占
,电解水制氢约占 。此外,在一定温度下,利用
。此外,在一定温度下,利用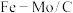 作催化剂裂解乙醇也可以制备氢气。科研人员研究相同温度下裂解乙醇制备氢气时,催化剂中
作催化剂裂解乙醇也可以制备氢气。科研人员研究相同温度下裂解乙醇制备氢气时,催化剂中 与
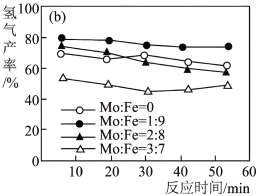
与 最佳质量比的实验结果如图,氢气产率越高,说明倠化剂效果越好。
最佳质量比的实验结果如图,氢气产率越高,说明倠化剂效果越好。
氢气的储存方式主要有高压气态储氢、低温液态储氢、固态材料储氢。科研人员研究出镁基固态储氢技术,实现了氢气安全、高效及大规模储运,原理是利用金属镁和氢气在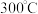 和高压条件下发生反应生成氢化镁
和高压条件下发生反应生成氢化镁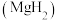 。
。
随着低耗能制氢及高效储氢问题的解决,氢能终将在各领域实现大规模的应用。______ 。
(2)对比图1中的曲线,得到的实验结论是______ 。
(3)氢气的储存方式主要有低温液态储氢、固态材料储氢和______ ;写出镁基固态储氢技术的原理______ (用化学方程式表示)。
(4)下列说法中不正确的是______ (填序号)。
a.现阶段氢能已经大规模使用
b.目前制氢的原料主要来源于化石燃料
c.裂解乙醇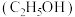 制氢指将乙醇分解成
制氢指将乙醇分解成 和
和
氢能
氢能是一种理想的清洁能源,其制取和储存是科学研究的重要方向。制氢的技术有多种,其中煤气化制氢约占
 、天然气重整制氢约占
、天然气重整制氢约占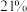 ,电解水制氢约占
,电解水制氢约占 。此外,在一定温度下,利用
。此外,在一定温度下,利用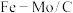 作催化剂裂解乙醇也可以制备氢气。科研人员研究相同温度下裂解乙醇制备氢气时,催化剂中
作催化剂裂解乙醇也可以制备氢气。科研人员研究相同温度下裂解乙醇制备氢气时,催化剂中 与
与 最佳质量比的实验结果如图,氢气产率越高,说明倠化剂效果越好。
最佳质量比的实验结果如图,氢气产率越高,说明倠化剂效果越好。氢气的储存方式主要有高压气态储氢、低温液态储氢、固态材料储氢。科研人员研究出镁基固态储氢技术,实现了氢气安全、高效及大规模储运,原理是利用金属镁和氢气在
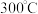 和高压条件下发生反应生成氢化镁
和高压条件下发生反应生成氢化镁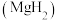 。
。随着低耗能制氢及高效储氢问题的解决,氢能终将在各领域实现大规模的应用。
(2)对比图1中的曲线,得到的实验结论是
(3)氢气的储存方式主要有低温液态储氢、固态材料储氢和
(4)下列说法中不正确的是
a.现阶段氢能已经大规模使用
b.目前制氢的原料主要来源于化石燃料
c.裂解乙醇
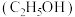 制氢指将乙醇分解成
制氢指将乙醇分解成 和
和
您最近一年使用:0次
名校
解题方法
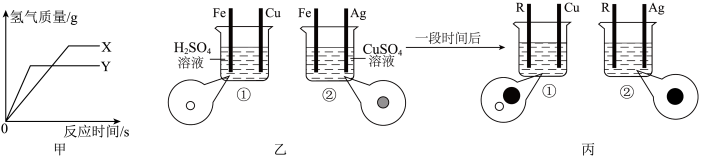
10 . 化学兴趣小组进行金属部分化学性质的探究。 和
和 的烧杯中分别加入等质量、等质量分数的稀盐酸,反应过程中生成氢气的质量如图甲所示。
的烧杯中分别加入等质量、等质量分数的稀盐酸,反应过程中生成氢气的质量如图甲所示。 表示的金属是
表示的金属是______ (填“Zn”或“Fe”下同),反应后可能有剩余的金属是______ 。
(2)实验二:探究Fe、Cu、Ag、R(R为未知金属)四种金属的金属活动性顺序。如图乙所示,将四根金属丝同时插入烧杯中的溶液里,只观察到①中铁丝表面出现气泡,②中铁丝表面有紫红色物质。一段时间后,如图丙所示,将烧杯中铁丝替换为R丝进行实验,观察到①中R丝表面出现气泡,②中R丝表面无明显现象。“ ”“
”“ ”“
”“ ”为相应金属丝插入烧杯前,烧杯中溶液里的阳离子。
”为相应金属丝插入烧杯前,烧杯中溶液里的阳离子。
①写出图乙烧杯②中发生反应的化学方程式______ 。______ 。
 和
和 的烧杯中分别加入等质量、等质量分数的稀盐酸,反应过程中生成氢气的质量如图甲所示。
的烧杯中分别加入等质量、等质量分数的稀盐酸,反应过程中生成氢气的质量如图甲所示。 表示的金属是
表示的金属是(2)实验二:探究Fe、Cu、Ag、R(R为未知金属)四种金属的金属活动性顺序。如图乙所示,将四根金属丝同时插入烧杯中的溶液里,只观察到①中铁丝表面出现气泡,②中铁丝表面有紫红色物质。一段时间后,如图丙所示,将烧杯中铁丝替换为R丝进行实验,观察到①中R丝表面出现气泡,②中R丝表面无明显现象。“
 ”“
”“ ”“
”“ ”为相应金属丝插入烧杯前,烧杯中溶液里的阳离子。
”为相应金属丝插入烧杯前,烧杯中溶液里的阳离子。①写出图乙烧杯②中发生反应的化学方程式
②“ ”表示的阳离子是
”表示的阳离子是
您最近一年使用:0次



