解题方法
1 . 钢铁在生产、生活中有广泛的用途。
(1)钢铁属于______ (填“纯净物”或“混合物”);
(2)炼铁厂常以焦炭、赤铁矿(主要成分是氧化铁Fe2O3)、空气等为主要原料炼铁,请写出一氧化碳与氧化铁在高温下反应的化学方程式:______ ;
(3)为了防止钢铁锈蚀,人们常采用______ 的方法(任写一种)来达到目的。
(4)从金属的原子结构看,你认为金属易与其它物质发生反应的根本原因是______ 。
(1)钢铁属于
(2)炼铁厂常以焦炭、赤铁矿(主要成分是氧化铁Fe2O3)、空气等为主要原料炼铁,请写出一氧化碳与氧化铁在高温下反应的化学方程式:
(3)为了防止钢铁锈蚀,人们常采用
(4)从金属的原子结构看,你认为金属易与其它物质发生反应的根本原因是
您最近一年使用:0次
2 . 科学家利用新方法设计出超轻铝晶体,全新超轻铝结构未来将广泛应用于研制更轻便的航天飞机和汽车部件等方面。
(1)铝是地壳中含量最高的______ (填“金属”或“非金属”)元素。铝元素的原子结构示意图如图所示,则铝原子的最外层电子数为_____ 。容易______ (选“失去”或“得到”),形成的离子符号为______ 。
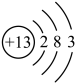
(2)飞机机身选用铝合金材料制造而不选用纯铝,主要原因是铝合金材料的硬度和强度_____ (填“大于”或“小于”)纯铝。
(3)铝制品要比铁更耐腐蚀的原因是(用化学方程式表示)________________________ ,反应的基本类型为____ 反应。
(4)对Al、Cu、Ag三种金属的活动性顺序进行探究,下列所选无法达到目的的一组试剂是________ (填序号)
A Al、Ag、CuSO4溶液 B AlCl3溶液、Cu、AgNO3溶液
C Al、Cu、稀盐酸、AgNO3溶液 D Cu、Ag、AlCl3溶液
(1)铝是地壳中含量最高的

(2)飞机机身选用铝合金材料制造而不选用纯铝,主要原因是铝合金材料的硬度和强度
(3)铝制品要比铁更耐腐蚀的原因是(用化学方程式表示)
(4)对Al、Cu、Ag三种金属的活动性顺序进行探究,下列所选无法达到目的的一组试剂是
A Al、Ag、CuSO4溶液 B AlCl3溶液、Cu、AgNO3溶液
C Al、Cu、稀盐酸、AgNO3溶液 D Cu、Ag、AlCl3溶液
您最近一年使用:0次
3 . Ⅰ.我国自行研发的大型客机C919于今年5月成功试飞,请根据所学知识回答问题。
(1)飞机所用的下列材料属于合成材料的是_______ (填序号)。
A.塑料扶手 B.纯羊毛毯 C.真皮座套 D.铜制扣件
(2)飞机上的镀铬铁制品能防锈蚀,其防锈原理是阻止了铁与______ 接触。
(3)若要验证飞机材料中的Fe、Cu和Al的金属活动性顺序,只需一种试剂直接与上述三种金属反应就能达到目的,该试剂是_______ (填序号)。
A.硫酸铝溶液 B.硫酸亚铁溶液 C.硫酸铜溶液
Ⅱ. 硒(Se)是人体必需的微量元素,它可有效调节免疫功能,迅速增强人体抵抗力,有延缓衰老的神奇作用.已知硒的原子结构示意图如图所示。请回答:
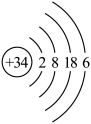
(1)硒原子的核外电子数是________
(2)它的化学性质与硫元素________ (填相似或不相似),硒离子的符号________ .
(1)飞机所用的下列材料属于合成材料的是
A.塑料扶手 B.纯羊毛毯 C.真皮座套 D.铜制扣件
(2)飞机上的镀铬铁制品能防锈蚀,其防锈原理是阻止了铁与
(3)若要验证飞机材料中的Fe、Cu和Al的金属活动性顺序,只需一种试剂直接与上述三种金属反应就能达到目的,该试剂是
A.硫酸铝溶液 B.硫酸亚铁溶液 C.硫酸铜溶液
Ⅱ. 硒(Se)是人体必需的微量元素,它可有效调节免疫功能,迅速增强人体抵抗力,有延缓衰老的神奇作用.已知硒的原子结构示意图如图所示。请回答:

(1)硒原子的核外电子数是
(2)它的化学性质与硫元素
您最近一年使用:0次
解题方法
4 . 2023年5月30日,“神舟十六号”载人飞船成功发射。
(1)航天员工作的核心舱使用了第三代半导体砷化镓(GaAs)太阳能电池翼,如图为砷和镓的微粒结构示意图。
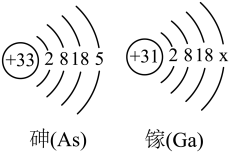
①在化学反应中,砷原子易___________ (选填“得到”或“失去”)电子。
②若图中是镓的原子结构示意图,则x的值为___________ 。
(2)航天员在核心舱的饮用水来自“水处理”系统,“水处理”系统将核心舱内产生的污水收集后,通过RO反渗透膜(只允许水分子和少部分离子通过)进行渗透净化处理,实现污水变净水,达到饮用水的标准。RO反渗透膜利用的净化方法相当于化学实验中的___________ 操作。
(1)航天员工作的核心舱使用了第三代半导体砷化镓(GaAs)太阳能电池翼,如图为砷和镓的微粒结构示意图。

①在化学反应中,砷原子易
②若图中是镓的原子结构示意图,则x的值为
(2)航天员在核心舱的饮用水来自“水处理”系统,“水处理”系统将核心舱内产生的污水收集后,通过RO反渗透膜(只允许水分子和少部分离子通过)进行渗透净化处理,实现污水变净水,达到饮用水的标准。RO反渗透膜利用的净化方法相当于化学实验中的
您最近一年使用:0次
解题方法
5 . 铯(Cs)原子钟是一种精密的计时工具。中国计量科学研究院研制的第二代铯原子钟是获得国际计量局认可的“世界上最好的基准原子钟”之一,其准确度达到2000万年不差一秒。饱原子结构示意图如图1所示。
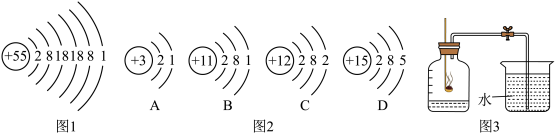
回答下列问题:
(1)Cs属于______ (填“金属”或“非金属”)元素,在周期表中属于第______ 周期,
(2)图2表示的微粒中,与铯原子化学性质相似的是______ (填字母标号)。
(3)图2中由D所示原子构成的某种单质可用于测定空气中氧气的含量(如图3所示),该实验集气瓶底部的水作用为______ ,写出该单质发生反应的化学方______ 。

回答下列问题:
(1)Cs属于
(2)图2表示的微粒中,与铯原子化学性质相似的是
(3)图2中由D所示原子构成的某种单质可用于测定空气中氧气的含量(如图3所示),该实验集气瓶底部的水作用为
您最近一年使用:0次
解题方法
6 . 2023年5月30日,“神舟十六号”载人飞船成功发射。
(1)航天员工作的核心舱使用了第三代半导体砷化镓(GaAs)太阳能电池翼,右图为砷和镓的微粒结构示意图。

①在化学反应中,砷原子易______ (选填“得到”或“失去”)电子。
②若图中是镓的原子结构示意图,则x的值为______ 。
(2)航天员在“天和”核心舱中生活所需要的氧气来自水的电解,核心舱内电解水的文字表达式为______ 。
(3)航天员在核心舱的饮用水来自“水处理”系统,“水处理”系统将核心舱内产生的污水收集后,通过RO反渗透膜(只允许水分子和少部分离子通过)进行渗透净化处理,实现污水变净水,达到饮用水的标准。
①RO反渗透膜利用的净化方法相当于化学实验中的______ 操作,可实现污水变净水。
②该净水过程属于______ (选填“物理”或“化学”)变化。
(1)航天员工作的核心舱使用了第三代半导体砷化镓(GaAs)太阳能电池翼,右图为砷和镓的微粒结构示意图。

①在化学反应中,砷原子易
②若图中是镓的原子结构示意图,则x的值为
(2)航天员在“天和”核心舱中生活所需要的氧气来自水的电解,核心舱内电解水的文字表达式为
(3)航天员在核心舱的饮用水来自“水处理”系统,“水处理”系统将核心舱内产生的污水收集后,通过RO反渗透膜(只允许水分子和少部分离子通过)进行渗透净化处理,实现污水变净水,达到饮用水的标准。
①RO反渗透膜利用的净化方法相当于化学实验中的
②该净水过程属于
您最近一年使用:0次
7 . 化学是研究物质及其变化的学科,质量守恒定律是化学反应的基本规律之一。
(1)从微观角度认识化学变化:
①如图是金属钠与氯气反应生成氯化钠的微观示意图,
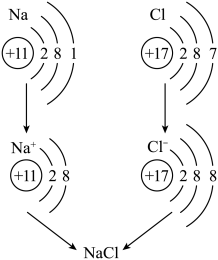
据图可知, 元素的化学性质与_____ ( 选填字母)密切相关。
A 最外层电子数
B 内层电子数
C 电子层数
②同一种元素的原子和离子相比较,质子数一定相同,核外电子数一定_____ (选填字母,下同),电子层数_____ 。
A 相同
B 不同
C 可能相同也可能不同
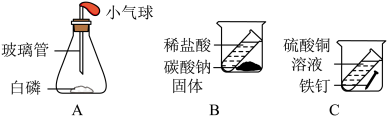
(2)某同学设计了如国所示的3个实验用来验证质量守恒定律,其中不能达到实验目的是_____ (选填字时)
(3)A、B、C、D表示4种物质,A和B在一定条件下反应生成C和D。其化学式和分子微观示意图见下表。
①D的化学式为_____ ;
②若17g A参加反应,则生成C的质量为_____ g。
(1)从微观角度认识化学变化:
①如图是金属钠与氯气反应生成氯化钠的微观示意图,

据图可知, 元素的化学性质与
A 最外层电子数
B 内层电子数
C 电子层数
②同一种元素的原子和离子相比较,质子数一定相同,核外电子数一定
A 相同
B 不同
C 可能相同也可能不同
(2)某同学设计了如国所示的3个实验用来验证质量守恒定律,其中不能达到实验目的是

(3)A、B、C、D表示4种物质,A和B在一定条件下反应生成C和D。其化学式和分子微观示意图见下表。
| 物质 | A | B | C | D | 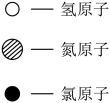 |
| 化学式 | NH3 | Cl2 | N2 | ||
| 微观示意图 | 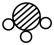 |  |  |  |
①D的化学式为
②若17g A参加反应,则生成C的质量为
您最近一年使用:0次
8 . 科学方法对化学学习起着事半功倍的作用。
(一) 微观粒子模型化是研究化学变化的重要方法。
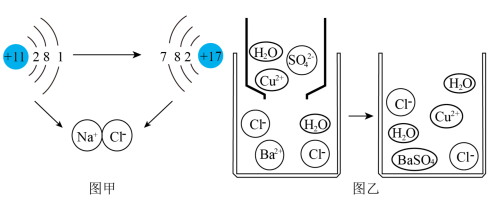
(1) 图甲是钠与氯气反应生成氯化钠示意图。该图说明在化学反应过程中一定发生变化的是_____ (填序号)。
a.原子核 b.原子的最外层电子数 c.原子的电子层数
(2)图乙是硫酸铜溶液与氯化钡溶液反应的示意图。该反应的实质是A+B→C,请用微粒符号表示该反应的实质_________________________________________________________ 。
(二) 控制变量、设计对比实验是实验探究的重要方法。
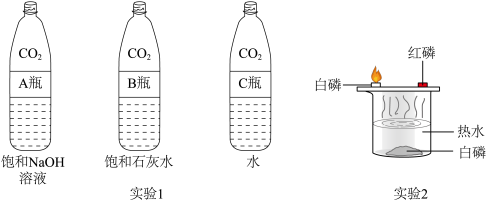
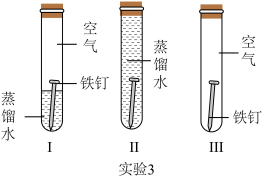
(3)实验1振荡3个塑料瓶,观察到塑料瓶变瘪的程度由大到小为_______________________ (用A、B、C填写),其中变浑浊的瓶内发生反应的化学方程式为 __________ ;对比A瓶与______ (填“B”或”C”)瓶的实验现象,可证明CO2能与NaOH发生反应。
(4)实验2探究物质燃烧的条件。将大小相同的红磷和白磷放在薄铜片的两侧,加热铜片的中部,观察现象。通过此实验,可说明燃烧的条件之一的是_____________ (填序号)。
A.可燃物 B.空气 C.温度达到着火点
(5)实验3是探究铁钉条件的实验,会出现明显现象的是试管______ (填“I”“II”或“III”),说明铁生锈实际上是铁与____________________________________ 发生反应。
(一) 微观粒子模型化是研究化学变化的重要方法。

(1) 图甲是钠与氯气反应生成氯化钠示意图。该图说明在化学反应过程中一定发生变化的是
a.原子核 b.原子的最外层电子数 c.原子的电子层数
(2)图乙是硫酸铜溶液与氯化钡溶液反应的示意图。该反应的实质是A+B→C,请用微粒符号表示该反应的实质
(二) 控制变量、设计对比实验是实验探究的重要方法。


(3)实验1振荡3个塑料瓶,观察到塑料瓶变瘪的程度由大到小为
(4)实验2探究物质燃烧的条件。将大小相同的红磷和白磷放在薄铜片的两侧,加热铜片的中部,观察现象。通过此实验,可说明燃烧的条件之一的是
A.可燃物 B.空气 C.温度达到着火点
(5)实验3是探究铁钉条件的实验,会出现明显现象的是试管
您最近一年使用:0次
2018-05-22更新
|
168次组卷
|
3卷引用:【全国市级联考】山东省潍坊市安丘市2018届九年级一模化学试题
解题方法
9 . “见著知微”是化学学科的重要特点。下列宏观事实的微观解释错误的是
| 选项 | 宏观事实 | 微观解释 |
| A | 石蜡在氧气中燃烧比在空气中剧烈 | 分子接触碰撞几率越大,反应越剧烈 |
| B | 氢气和液氢都可以燃烧 | 同种分子,化学性质相同 |
| C | 酒精温度计受热,液面升高 | 温度升高,酒精分子体积变大 |
| D | 稀有气体化学性质稳定,常作保护气 | 原子最外层达到稳定结构 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
10 . 2021年4月16日,我国自主研发出超流氦大型低温制冷装备技术达到国际先进水平,当温度低到-271℃时,液氦就会变成超流氦。根据图中信息判断,下列说法正确的是
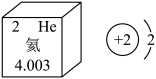
| A.氦属于金属元素 |
| B.He既可表示氦元素,也可表示氦分子 |
| C.氦原子的质量是4.003g |
| D.氦原子化学性质活泼 |
您最近一年使用:0次



