名校
解题方法
1 . 分类、归纳等是化学学习的常用方法。下列分类归纳正确的是
| A.碱:纯碱、一水合氨 | B.复合材料:钢筋混凝土、玻璃钢 |
| C.合金:黄铜、铁锈 | D.溶液:糖水、石灰浆 |
您最近一年使用:0次
2 . 下列图像与反应过程的变化趋势相对应的有
| 图像 |
|
|
|
|
| 反应过程 |  受热分解 受热分解 | 向NaOH和 混合溶液中滴加过量稀硫酸 混合溶液中滴加过量稀硫酸 | 一定温度下,向饱和 溶液中加入NaOH固体 溶液中加入NaOH固体 | 向 和 和 的混合溶液中加入过量锌粉 的混合溶液中加入过量锌粉 |
| A.0个 | B.1个 | C.2个 | D.3个 |
您最近一年使用:0次
3 . “垃圾是放错地方的资源”。印刷电路板由高分子材料和铜箔复合面成,印刷电路时要用 溶液做“腐蚀液”。现从某含有
溶液做“腐蚀液”。现从某含有 、
、 、
、 的工业废液中回收铜并制备氯化铁晶体的流程如图。
的工业废液中回收铜并制备氯化铁晶体的流程如图。 。
。
(1)试剂a的名称是________ ,加入过量a的目的是________ 。
(2)写出试剂b与滤渣Y反应的化学方程式________ ,该基本反应类型是________ 。
(3)试剂c为过氧化氢溶液,滤液Z中的溶质成分与过氧化氢溶液恰好完全反应,生成W和最常见的溶剂写出化学方程式________ 。
(4)操作Ⅲ的名称是________ ,该操作中玻璃棒的作用是________ 。
 溶液做“腐蚀液”。现从某含有
溶液做“腐蚀液”。现从某含有 、
、 、
、 的工业废液中回收铜并制备氯化铁晶体的流程如图。
的工业废液中回收铜并制备氯化铁晶体的流程如图。
 。
。(1)试剂a的名称是
(2)写出试剂b与滤渣Y反应的化学方程式
(3)试剂c为过氧化氢溶液,滤液Z中的溶质成分与过氧化氢溶液恰好完全反应,生成W和最常见的溶剂写出化学方程式
(4)操作Ⅲ的名称是
您最近一年使用:0次
4 . 下列选项与图示中所反映的变化关系不对应的是

| A.等质量且过量的锌粉、锌粒分别与等质量、等浓度的稀盐酸反应 |
| B.向一定量NaOH溶液中加水稀释 |
| C.在相同温度下,等质量等浓度的H2O2溶液分解制O2 |
| D.向一定体积的Ba(OH)2溶液中,逐滴滴入一定浓度的稀硫酸 |
您最近一年使用:0次
昨日更新
|
117次组卷
|
2卷引用:2024年湖南省衡阳市4月中考适应性考试化学试题
名校
解题方法
5 .  溶液是初中化学常见的一种试剂。
溶液是初中化学常见的一种试剂。
(1)农业上常用它配制波尔多液杀菌剂:
①波尔多液杀菌剂是用硫酸铜和石灰乳混合配制的,请写出反应的化学方程式:______ 。
②在烧杯中放入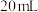 硫酸铜溶液,逐滴加入某浓度的澄清石灰水,测定混合液
硫酸铜溶液,逐滴加入某浓度的澄清石灰水,测定混合液 随滴入
随滴入 溶液体积的变化,结果如下图。下列说法正确的是
溶液体积的变化,结果如下图。下列说法正确的是______ (填字母)
(已知:溶液中自由移动离子的浓度越小,溶液的导电性越差)
B.a点烧杯内溶液中溶质只有1种
C.ab段烧杯内溶液的导电性逐渐降低
D.bc段烧杯内沉淀质量不断增加
(2)硫酸铜溶液性质的探究:
某研究小组的同学设计了如图所示的实验。他们在实验过程中观察到:镁条表面逐渐失去光泽,同时有大量气泡冒出,有黑色固体析打磨光亮的镁条出,一段时间后黑色固体变成棕褐色;溶液出现浑浊,浑浊物呈现10%硫酸铜溶液淡淡的蓝绿色。
镁条表面气泡究竟是什么气体?棕褐色物质是什么成分?蓝绿色沉淀又是什么物质?
【查阅资料】
①碱式硫酸铜【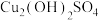 】呈绿色,在水中溶解度极小,向碱式硫酸铜中加入20%的
】呈绿色,在水中溶解度极小,向碱式硫酸铜中加入20%的 溶液,能得到深蓝色溶液,该溶液与乙醛在加热的条件下能生成砖红色的沉淀。②颗粒大小不同的铜会呈现不同的颜色,如黑色、棕褐色、红色等。
溶液,能得到深蓝色溶液,该溶液与乙醛在加热的条件下能生成砖红色的沉淀。②颗粒大小不同的铜会呈现不同的颜色,如黑色、棕褐色、红色等。
【方案设计】
方案一:镁条表面冒出的气体成分
小组同学共提出如下几种猜想:① ;②
;② ;③
;③ ;④
;④ 。经讨论同学们一致认为猜想④是错误的,理由是
。经讨论同学们一致认为猜想④是错误的,理由是______ 。
为验证其他猜想,小组同学设计如表实验:
方案二:棕褐色物质成分
作出猜想:棕褐色物质可能是铜。为验证其猜想,小组同学设计如下实验:
方案三:蓝绿色沉淀成分
作出猜想:蓝绿色沉淀可能是碱式硫酸铜。设计实验并验证其猜想,写出实验方案______ 。
(3)硫酸铜晶体的制备与生长实验
小组同学向100克的70℃热水中加入80克硫酸铜晶体,实验过程如图所示。______ 。
②请判断图丙是否为饱和溶液并说明理由______ 。
 溶液是初中化学常见的一种试剂。
溶液是初中化学常见的一种试剂。(1)农业上常用它配制波尔多液杀菌剂:
①波尔多液杀菌剂是用硫酸铜和石灰乳混合配制的,请写出反应的化学方程式:
②在烧杯中放入
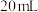 硫酸铜溶液,逐滴加入某浓度的澄清石灰水,测定混合液
硫酸铜溶液,逐滴加入某浓度的澄清石灰水,测定混合液 随滴入
随滴入 溶液体积的变化,结果如下图。下列说法正确的是
溶液体积的变化,结果如下图。下列说法正确的是(已知:溶液中自由移动离子的浓度越小,溶液的导电性越差)

B.a点烧杯内溶液中溶质只有1种
C.ab段烧杯内溶液的导电性逐渐降低
D.bc段烧杯内沉淀质量不断增加
(2)硫酸铜溶液性质的探究:
某研究小组的同学设计了如图所示的实验。他们在实验过程中观察到:镁条表面逐渐失去光泽,同时有大量气泡冒出,有黑色固体析打磨光亮的镁条出,一段时间后黑色固体变成棕褐色;溶液出现浑浊,浑浊物呈现10%硫酸铜溶液淡淡的蓝绿色。

镁条表面气泡究竟是什么气体?棕褐色物质是什么成分?蓝绿色沉淀又是什么物质?
【查阅资料】
①碱式硫酸铜【
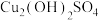 】呈绿色,在水中溶解度极小,向碱式硫酸铜中加入20%的
】呈绿色,在水中溶解度极小,向碱式硫酸铜中加入20%的 溶液,能得到深蓝色溶液,该溶液与乙醛在加热的条件下能生成砖红色的沉淀。②颗粒大小不同的铜会呈现不同的颜色,如黑色、棕褐色、红色等。
溶液,能得到深蓝色溶液,该溶液与乙醛在加热的条件下能生成砖红色的沉淀。②颗粒大小不同的铜会呈现不同的颜色,如黑色、棕褐色、红色等。【方案设计】
方案一:镁条表面冒出的气体成分
小组同学共提出如下几种猜想:①
 ;②
;② ;③
;③ ;④
;④ 。经讨论同学们一致认为猜想④是错误的,理由是
。经讨论同学们一致认为猜想④是错误的,理由是为验证其他猜想,小组同学设计如表实验:
| 操作过程 | 现象 | 结论 |
向 溶液中加入足量打磨光亮的镁条,收集生成的气体,并点燃 溶液中加入足量打磨光亮的镁条,收集生成的气体,并点燃 | 说明猜想②是正确的 |
作出猜想:棕褐色物质可能是铜。为验证其猜想,小组同学设计如下实验:
| 操作过程 | 现象 | 结论 |
| 取镁条表面的棕褐色物质于试管加热,颜色变黑,再往黑色物质中滴加足量的 | 溶液变蓝色 | 说明棕褐色物质是铜 |
作出猜想:蓝绿色沉淀可能是碱式硫酸铜。设计实验并验证其猜想,写出实验方案
(3)硫酸铜晶体的制备与生长实验
小组同学向100克的70℃热水中加入80克硫酸铜晶体,实验过程如图所示。

②请判断图丙是否为饱和溶液并说明理由
您最近一年使用:0次
2024·湖北武汉·模拟预测
解题方法
6 . 某兴趣小组对“一氧化碳还原氧化铁”实验进行拓展研究。
【查阅资料】①加热MgCO3和Zn的混合物,产生三种氧化物。
②氯化亚铜溶液吸收CO产生红色固体:2CuCl+2CO+2H2O═Cu2Cl2(CO)2•2H2O↓,氨水能加速反应。
【设计方案】根据上述资料设计如图实验装置。
(1)①装配好实验装置后,先要检查装置的气密性,再装入药品。
②打开活塞,通入适量氮气的目的是_____________________ 。
③关闭活塞,点燃酒精灯和酒精喷灯。
④观察实验现象,B处现象是_________________ ,D处出现红色固体。
⑤熄灭酒精灯和酒精喷灯。
【实验分析】
(2)写出A处反应的化学方程式______________________ 。
(3)下列关于该实验说法正确的是_____ (选填序号)。
a.B处固体质量减少
b.D处现象证明A、B处发生了反应
c.E处应放置一只燃着的酒精灯
d.实验结束后应继续通氮气至玻璃管冷却
(4)已知A处参加反应的MgCO3质量为3.36g,C处白色沉淀的质量为2g,从环保角度考虑D处CuCl的质量至少需要_______ g。
【查阅资料】①加热MgCO3和Zn的混合物,产生三种氧化物。
②氯化亚铜溶液吸收CO产生红色固体:2CuCl+2CO+2H2O═Cu2Cl2(CO)2•2H2O↓,氨水能加速反应。
【设计方案】根据上述资料设计如图实验装置。

(1)①装配好实验装置后,先要检查装置的气密性,再装入药品。
②打开活塞,通入适量氮气的目的是
③关闭活塞,点燃酒精灯和酒精喷灯。
④观察实验现象,B处现象是
⑤熄灭酒精灯和酒精喷灯。
【实验分析】
(2)写出A处反应的化学方程式
(3)下列关于该实验说法正确的是
a.B处固体质量减少
b.D处现象证明A、B处发生了反应
c.E处应放置一只燃着的酒精灯
d.实验结束后应继续通氮气至玻璃管冷却
(4)已知A处参加反应的MgCO3质量为3.36g,C处白色沉淀的质量为2g,从环保角度考虑D处CuCl的质量至少需要
您最近一年使用:0次
名校
解题方法
7 . 我国早在商代时期就开始使用铜器,到春秋战国时期,开始生产和使用铁器。
(1)铁锅用于烹饪食物主要是利用铁具有良好的______ 性。
(2)下列文物中不属于金属制品的是______(填字母序号)。
(3)《本草纲目拾遗》中记载:“舶上铁日久起销(锈)…刮下之销末,名铁线粉”。铁丝“日久起销”的原因是铁与空气中的______ (填化学式)同时接触而导致。
(4)我国古代曾用“湿法炼铜”和“火法炼铜”,其原理分别为:
①湿法炼铜:Fe+CuSO4=Cu+FeSO4
②火法炼铜:Cu2S+O2 2Cu+SO2
2Cu+SO2
上述两种方案中较优的是______ (填数字序号),理由是______ 。
(5)将一定量的铜粉和锌粉的混合物放入一定量的硝酸银溶液中,使其充分反应后过滤,得到滤渣和滤液。下列判断正确的是______(填字母序号)。
(6)某金属粉末含有Mg、Al、Cu、Ag中的一种或几种,取24g该金属粉末与足量的稀盐酸反应产生2g氢气,则该金属粉末的组成情况有_______ 种。
(1)铁锅用于烹饪食物主要是利用铁具有良好的
(2)下列文物中不属于金属制品的是______(填字母序号)。
A.鎏金骑士铜贮贝器 | B.鸡形陶壶 |
C.牛虎铜案 | D.滇王金印 |
(3)《本草纲目拾遗》中记载:“舶上铁日久起销(锈)…刮下之销末,名铁线粉”。铁丝“日久起销”的原因是铁与空气中的
(4)我国古代曾用“湿法炼铜”和“火法炼铜”,其原理分别为:
①湿法炼铜:Fe+CuSO4=Cu+FeSO4
②火法炼铜:Cu2S+O2
 2Cu+SO2
2Cu+SO2上述两种方案中较优的是
(5)将一定量的铜粉和锌粉的混合物放入一定量的硝酸银溶液中,使其充分反应后过滤,得到滤渣和滤液。下列判断正确的是______(填字母序号)。
| A.滤液中一定有Zn(NO3)2 |
| B.滤渣的质量一定大于所加入固体的质量 |
| C.向滤渣中加入稀硫酸,有气泡产生,则滤渣中一定有Zn,一定不含Ag |
| D.若滤液为蓝色、则滤液中一定含有硝酸锌和硝酸铜,一定役有硝酸银 |
(6)某金属粉末含有Mg、Al、Cu、Ag中的一种或几种,取24g该金属粉末与足量的稀盐酸反应产生2g氢气,则该金属粉末的组成情况有
您最近一年使用:0次
解题方法
8 . 《天工开物》是我国古代科技发展的智慧结晶。书中记载了有关金属铜及铜合金的工艺:“凡铜供世用,出山与出炉只有赤铜。以炉甘石或倭铅参和,转色为黄铜;以砒霜等药制炼为白铜;矾、硝等药制炼为青铜……。”
(1)青铜是金属冶铸史上最早的合金,如图所示的青铜鬲流行于商代至春秋,鬲是中国古代的一种炊具。青铜制成的鬲能做炊具是利用了金属的_______ 性。_______ (写一点)。为了鉴别黄铜和黄金,将真假黄金分别放入稀硫酸中,黄金表面没有明显变化,而观察到黄铜表面有气泡产生,其反应的化学方程式为_______ 。
(3)人类发现铁和铜的时期相差不大,但出土文物中铁制品很少,原因是铁制品容易与空气中_______ 的反应而生锈,生活中常采用_______ (写一种)的方法防止铁制品锈蚀。
(4)“倭铅”是锌的古称。
①化学兴趣小组将一定量的锌粉加入含有FeCl2和CuCl2的废液中,充分反应后过滤,得到滤液和滤渣,向滤渣中滴加稀盐酸,有气泡产生,则滤液中一定含有的溶质是_______ (填化学式)。
②实验室有一定质量含锌的两种金属混合物,加入过量的稀盐酸,充分反应,测得生成H2的质量为0.2g,将反应后的溶液蒸发,得到11.1g固体。则金属混合物中的另一种金属可能是_______ (填标号)。
A.Mg B.Al C.Fe D.Cu
(1)青铜是金属冶铸史上最早的合金,如图所示的青铜鬲流行于商代至春秋,鬲是中国古代的一种炊具。青铜制成的鬲能做炊具是利用了金属的

(3)人类发现铁和铜的时期相差不大,但出土文物中铁制品很少,原因是铁制品容易与空气中
(4)“倭铅”是锌的古称。
①化学兴趣小组将一定量的锌粉加入含有FeCl2和CuCl2的废液中,充分反应后过滤,得到滤液和滤渣,向滤渣中滴加稀盐酸,有气泡产生,则滤液中一定含有的溶质是
②实验室有一定质量含锌的两种金属混合物,加入过量的稀盐酸,充分反应,测得生成H2的质量为0.2g,将反应后的溶液蒸发,得到11.1g固体。则金属混合物中的另一种金属可能是
A.Mg B.Al C.Fe D.Cu
您最近一年使用:0次
2024·陕西·模拟预测
解题方法
9 . 实验小组从X、银、铜、锌四种金属的混合物中分离某贵重金属丙。流程如下:(X在化合物中为+2价)_____ 种。
(2)写出③中发生反应的化学方程式___________ 。
(3)用下列各组物质进行实验,不能验证银、X、锌三种金属活动性强弱的是 (填字母)。

(2)写出③中发生反应的化学方程式
(3)用下列各组物质进行实验,不能验证银、X、锌三种金属活动性强弱的是 (填字母)。
| A.锌、XSO4溶液、银 | B.ZnSO4溶液、X、银 |
| C.ZnSO4溶液、X、AgNO3溶液 | D.锌、X、稀盐酸、AgNO3溶液 |
您最近一年使用:0次
2024·山东济南·模拟预测
解题方法
10 . 下图所示为实验室中常见气体制备、净化、干燥、收集和进行实验探究的部分仪器(组装实验装置时,可重复选择仪器),某化学小组的同学欲利用其进行下列化学实验。
①所选装置的连接顺序为___________ (从左至右填写装置序号字母)。
②把带火星的木条伸入盛满氧气的集气瓶中,会观察到木条___________ 的现象。
③制取氧气所发生反应的化学方程式为___________ 。
④下列有关氧气制取和性质的叙述中,不正确的是___________ (填选项序号之一)。
A.实验室制氧气时,应先检查装置的气密性,再加入药品
B.在此反应前后,二氧化锰的质量和化学性质都不发生改变
C.当氧气参与化学反应时,单位体积空间里氧分子越多,反应越剧烈
D.木炭在空气中燃烧不如在氧气中燃烧剧烈,因此属于缓慢氧化
(2)用一氧化碳气体(含有少量二氧化碳和水蒸气)测定某氧化铁样品(含少量固体杂质,杂质不发生反应)的纯度。所选装置按“混合气体→A1→B→D→A2→F”的顺序连接(A1、A2为盛有澄清石灰水的洗气瓶,实验前检验装置的气密性)
①洗气瓶A1中看到的现象是___________ 。
②洗气瓶B的作用是___________ 。
③仪器D大玻璃管中,发生反应的化学方程式为___________ 。
④若所发生的化学反应都充分反应,实验过程中记录实验数据,如下表所示:
选择___________ (填“a组”“b组”“c组”之一)数据进行计算,原氧化铁样品纯度是___________ (计算结果精确到0.1%)。
⑤某同学用反应前后A2处的质量变化来计算样品的纯度,但是计算出的样品纯度与实际值相比偏大,其原因可能是___________ (填选项序号之一)。
A.实验开始时,在没有加热之前,就通了一会儿一氧化碳
B.实验过程中,空气中混有的二氧化碳和水蒸气进入A2,被A2吸收
C.反应结束熄灭酒精灯后,继续通入一氧化碳气体,直至大玻璃管冷却
D.装置D中玻璃管内的氧化铁样品未完全变黑,反应不完全

①所选装置的连接顺序为
②把带火星的木条伸入盛满氧气的集气瓶中,会观察到木条
③制取氧气所发生反应的化学方程式为
④下列有关氧气制取和性质的叙述中,不正确的是
A.实验室制氧气时,应先检查装置的气密性,再加入药品
B.在此反应前后,二氧化锰的质量和化学性质都不发生改变
C.当氧气参与化学反应时,单位体积空间里氧分子越多,反应越剧烈
D.木炭在空气中燃烧不如在氧气中燃烧剧烈,因此属于缓慢氧化
(2)用一氧化碳气体(含有少量二氧化碳和水蒸气)测定某氧化铁样品(含少量固体杂质,杂质不发生反应)的纯度。所选装置按“混合气体→A1→B→D→A2→F”的顺序连接(A1、A2为盛有澄清石灰水的洗气瓶,实验前检验装置的气密性)
①洗气瓶A1中看到的现象是
②洗气瓶B的作用是
③仪器D大玻璃管中,发生反应的化学方程式为
④若所发生的化学反应都充分反应,实验过程中记录实验数据,如下表所示:
| 组别 | a组:A1装置总质量 | b组:B中溶液质量 | c组:D中玻璃管内固体质量 |
| 反应前质量 | 750.0g | 200.0g | 14.96g |
| 反应后质量 | 750.22g | 200.9g | 11.12g |
⑤某同学用反应前后A2处的质量变化来计算样品的纯度,但是计算出的样品纯度与实际值相比偏大,其原因可能是
A.实验开始时,在没有加热之前,就通了一会儿一氧化碳
B.实验过程中,空气中混有的二氧化碳和水蒸气进入A2,被A2吸收
C.反应结束熄灭酒精灯后,继续通入一氧化碳气体,直至大玻璃管冷却
D.装置D中玻璃管内的氧化铁样品未完全变黑,反应不完全
您最近一年使用:0次