解题方法
1 . 低钠盐是在氯化钠中加入适量的氯化钾和硫酸镁,来降低其中钠元素的含量,从而改善人体钠钾平衡。化学小组为测定某品牌低钠盐中硫酸镁的质量分数,进行了下图所示实验。________ 。
(2)加过量 溶液的目的是
溶液的目的是________ 。
(3)计算低钠盐中硫酸镁的质量分数(写出计算过程)。
(4)追求健康生活,共“盐”美好未来。下列有关说法正确的是_______(填字母,双选)

(2)加过量
 溶液的目的是
溶液的目的是(3)计算低钠盐中硫酸镁的质量分数(写出计算过程)。
(4)追求健康生活,共“盐”美好未来。下列有关说法正确的是_______(填字母,双选)
| A.加锌盐可以预防佝偻病 |
| B.加铁盐可以预防缺铁性贫血 |
| C.加碘盐可以预防甲状腺疾病 |
| D.为补充人体所需钙元素,可大量吃加钙盐 |
您最近一年使用:0次
解题方法
2 . 对实验现象所做的解释错误的是

| A.图甲:A、B试管分别收集到氢气和氧气,说明水由氢元素和氧元素组成 |
| B.图乙:碘几乎不溶于水而溶于汽油,得出影响物质溶解性的因素之一是溶剂的种类 |
| C.图丙:左侧液面高于右侧,说明在电流、通电时间相同的情况下,电阻越大产生的热量越少 |
| D.图丁:棉球被压燃,说明做功可以改变物体的内能 |
您最近一年使用:0次
3 . 小格在家中自制了一杯饮品,过程如下。通过观察与实验,推理与判断,得出的结论正确的是

| A.①中充分溶解形成蔗糖饱和溶液 |
B.②中食盐在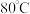 比在室温下溶解得快 比在室温下溶解得快 |
| C.③中下层饮品比上层甜 |
| D.③中有晶体析出 |
您最近一年使用:0次
解题方法
4 . 学们对实验室的某铵态氮肥进行了如图甲实验。氯化钡的溶解度随温度的变化曲线如图乙、下列说法正确的是
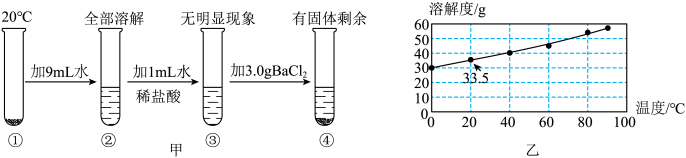
| A.该铵态氮肥可能是硫酸铵 | B.③中溶液能用于给植物施肥 |
C.④中固体成分中含有 | D.实验证明该铵态氮肥易溶于水 |
您最近一年使用:0次
解题方法
5 . 制作面包常用到泡打粉,碳酸氢钠是泡打粉的主要成分之一、学习小组通过学习知道碳酸钠与碳酸氢钠性质相似,开展了“能否用碳酸钠替代碳酸氢钠作泡打粉”的探究。某品牌泡打粉标签如下图所示。
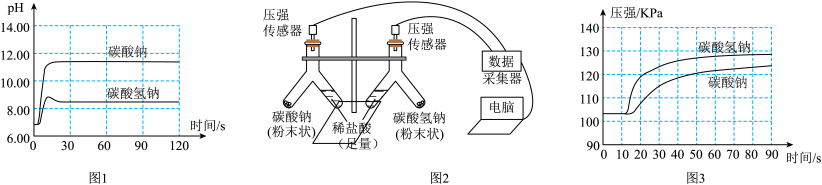
【实验2】取1g碳酸氢钠与1g碳酸钠分别置于各盛有10mL蒸馏水的两个烧杯中,边搅拌边用pH传感器进行测量,实验结果如图1。
【实验3】如图2,各取1g的碳酸氢钠与碳酸钠粉末分别放在两支Y形管(容量均为100mL)一端,另一端装足量的等量等浓度稀盐酸,倾斜铁架台,让盐酸缓缓流向粉末。实验过程中,Y形管塞子被冲出。
【实验4】另各取0.5g的碳酸氢钠与碳酸钠粉末,重新按实验3操作步骤进行,用压强传感器测量管内气压变化如图3。___________ 。
(2)实验2中两个烧杯内碳酸氢钠溶液的浓度___________ (填“大于”、“等于”或“小于”)碳酸钠溶液的浓度。
(3)实验3中盐酸流向粉末后发生反应的化学方程式为___________ (写一个);Y形管塞子被冲出的原因是___________ 。
(4)根据实验4中可知等质量的碳酸氢钠比碳酸钠发酵效果更好,其原因是___________ 。
(5)项目式学习小组模仿制作面包时利用面粉、泡打粉、水等设计如下实验。
该实验的目的是___________ 。
(6)已知碱性较强的物质会使食物带有苦涩味、口感较差。根据实验结果分析,一般不用碳酸钠替代碳酸氢钠作泡打粉,简要说明理由。
答:___________ 。

【实验2】取1g碳酸氢钠与1g碳酸钠分别置于各盛有10mL蒸馏水的两个烧杯中,边搅拌边用pH传感器进行测量,实验结果如图1。
【实验3】如图2,各取1g的碳酸氢钠与碳酸钠粉末分别放在两支Y形管(容量均为100mL)一端,另一端装足量的等量等浓度稀盐酸,倾斜铁架台,让盐酸缓缓流向粉末。实验过程中,Y形管塞子被冲出。
【实验4】另各取0.5g的碳酸氢钠与碳酸钠粉末,重新按实验3操作步骤进行,用压强传感器测量管内气压变化如图3。
(2)实验2中两个烧杯内碳酸氢钠溶液的浓度
(3)实验3中盐酸流向粉末后发生反应的化学方程式为
(4)根据实验4中可知等质量的碳酸氢钠比碳酸钠发酵效果更好,其原因是
(5)项目式学习小组模仿制作面包时利用面粉、泡打粉、水等设计如下实验。
| 组别 | 面粉/g | 泡打粉/g | 水/g | 感官评定 |
| ① | 50 | 0.5 | 25 | 待评 |
| ② | 50 | 1 | 25 | 待评 |
| ③ | 50 | 2 | 25 | 待评 |
(6)已知碱性较强的物质会使食物带有苦涩味、口感较差。根据实验结果分析,一般不用碳酸钠替代碳酸氢钠作泡打粉,简要说明理由。
答:
您最近一年使用:0次
解题方法
6 . “溶解”是化学学科的核心概念之一。兴趣小组同学对固体物质的溶解展开探究。
Ⅰ.溶解过程探究
按图1所示进行实验。闭合开关,观察到电珠不亮。再将10克氯化钠放入水中,观察现象。______ (选填“变亮”或“不亮”),说明氯化钠在溶解过程中是以______ 的形式分散到水中。
(2)将氯化钠改成蔗糖重复实验,可观察到实验现象与氯化钠溶解______ (选填“相同”或“不同”)。
Ⅱ.溶解性影响因素探究
【初步探究】按图2所示进行实验。______ 。
(4)B中观察到固体不再减少,此时溶液为______ (选填“饱和”或“不饱和”)状态。
(5)图2实验可得出结论:物质的溶解性与______ 有关。
【深入思考】同学们讨论后认为通过加热或增加溶剂的量也能使B中固体溶解,物质的溶解性可能与这两个因素有关。
【查阅资料】硫酸铜溶液能吸收红、黄光而使溶液呈现蓝色。当一束平行单色光照射硫酸铜溶液时,溶液浓度越大,对于红、黄光的吸收能力越强,透过溶液的光强度越小。
【实验探究】
①取试管a加入2药匙硫酸铜晶体和10mL饱和CuSO4溶液;另取试管b重复上述操作。
②将试管a、b分别装入光强度采集装置(图3为装置原理图)。
③加热试管a并持续测量透过溶液光线的光强度,复制数据导入软件中绘制出“光强度—时间”曲线如图4所示。
④在试管b内加入3mL水并持续测量透过溶液光线的光强度,复制数据导入软件中绘制“光强度一时间”曲线如图5所示。______ (选填“强”或“弱”)。
(7)图5中,一开始光强度数值增强的原因是______ 。
(8)依据图5,请写出硫酸铜的溶解性与溶剂水质量的关系及判断依据:______ 。
Ⅰ.溶解过程探究
按图1所示进行实验。闭合开关,观察到电珠不亮。再将10克氯化钠放入水中,观察现象。

(2)将氯化钠改成蔗糖重复实验,可观察到实验现象与氯化钠溶解
Ⅱ.溶解性影响因素探究
【初步探究】按图2所示进行实验。

(4)B中观察到固体不再减少,此时溶液为
(5)图2实验可得出结论:物质的溶解性与
【深入思考】同学们讨论后认为通过加热或增加溶剂的量也能使B中固体溶解,物质的溶解性可能与这两个因素有关。
【查阅资料】硫酸铜溶液能吸收红、黄光而使溶液呈现蓝色。当一束平行单色光照射硫酸铜溶液时,溶液浓度越大,对于红、黄光的吸收能力越强,透过溶液的光强度越小。
【实验探究】
①取试管a加入2药匙硫酸铜晶体和10mL饱和CuSO4溶液;另取试管b重复上述操作。
②将试管a、b分别装入光强度采集装置(图3为装置原理图)。
③加热试管a并持续测量透过溶液光线的光强度,复制数据导入软件中绘制出“光强度—时间”曲线如图4所示。
④在试管b内加入3mL水并持续测量透过溶液光线的光强度,复制数据导入软件中绘制“光强度一时间”曲线如图5所示。

(7)图5中,一开始光强度数值增强的原因是
(8)依据图5,请写出硫酸铜的溶解性与溶剂水质量的关系及判断依据:
您最近一年使用:0次
解题方法
7 . 过碳酸钠(2Na2CO3•3H2O2)是某些洗涤剂的有效成分,它是一种白色固体、易溶于水,受热易分解生成碳酸钠、水和氧气。某种制备过碳酸钠的方法如图所示(反应器中,过氧化氢和碳酸钠在一定条件下反应生成过碳酸钠)。_______ 。
(2)加入乙醇可以使生成的过碳酸钠在常温条件下从溶液中结晶析出,这说明加入乙醇使过碳酸钠的溶解性变_______ (选填“强”或“弱”);操作M是______ (填操作名称)。
(3)某小组开展实验,探究温度、加入过氧化氢溶液所用时间对该反应收率的影响。(收率指每投入1mol碳酸钠,实际得到的过碳酸钠固体与理论计算值的比值)_______ 次实验;结合图中数据分析,可以得出的结论是______ 。向反应器中加入过氧化氢溶液应使用的仪器是_______ (选填图二中的仪器编号)。
②如表所示,滴加等量、等浓度过氧化氢溶液所用时间相同的条件下,温度在20-25℃时收率较低,可能的原因是_______ 。

(2)加入乙醇可以使生成的过碳酸钠在常温条件下从溶液中结晶析出,这说明加入乙醇使过碳酸钠的溶解性变
(3)某小组开展实验,探究温度、加入过氧化氢溶液所用时间对该反应收率的影响。(收率指每投入1mol碳酸钠,实际得到的过碳酸钠固体与理论计算值的比值)

②如表所示,滴加等量、等浓度过氧化氢溶液所用时间相同的条件下,温度在20-25℃时收率较低,可能的原因是
| 反应器温度(℃) | 收率 |
| 5-10 | 85.5% |
| 10-15 | 85.8% |
| 15-20 | 88.4% |
| 20-25 | 83.0% |
您最近一年使用:0次
名校
解题方法
8 . 用Y型试管做化学实验有的可以简化操作步骤,有的增强了对比性。关于以下四个实验的分析不正确的是

| A.甲实验将右侧溶液倒入左侧后可以分离出木炭和氧化铜 |
| B.乙实验验证了铁的锈蚀与水有关 |
| C.丙实验Y型管中的白磷与红磷对比说明燃烧的条件是达到着火点 |
| D.丁实验高锰酸钾与碘对比说明不同物质在水中溶解性不同 |
您最近一年使用:0次
9 . 小明同学通过家庭实验探究影响糖溶解速率的因素,实验设计见下表。(方糖与白砂糖成分相同)
(1)X、Y的数值分别为___________ 和___________ 。
(2)实验③中的糖比实验①中溶解得快,说明_______ ,溶解速率越快。通过对比实验______ 和_______ ,说明搅拌可以加速溶解。
(3)请写出探究温度影响糖的溶解速率的实验方案:___________ 。
(4)t℃时,蔗糖的溶解度为300g,小明准备将t℃时蔗糖的饱和溶液400g加水稀释为10%的蔗糖溶液,需要加水___________ g。
| 实验① | 实验② | 实验③ | |
| 糖的颗粒大小 | 块状方糖 | 块状方糖 | 粉状白砂糖 |
| 糖的质量/g | 5 | 5 | Y |
| 温度/℃ | 20 | X | 20 |
| 是否搅拌 | 是 | 否 | 是 |
| 水的质量/g | 20 | 20 | 20 |
(2)实验③中的糖比实验①中溶解得快,说明
(3)请写出探究温度影响糖的溶解速率的实验方案:
(4)t℃时,蔗糖的溶解度为300g,小明准备将t℃时蔗糖的饱和溶液400g加水稀释为10%的蔗糖溶液,需要加水
您最近一年使用:0次
解题方法
10 . “某品牌碳酸钙D3颗粒,每袋含钙量为500mg”是真的吗?实验小组展开了一系列项目式学习。
(1)【实验原理】测出每袋碳酸钙D3颗粒与足量稀盐酸反应生成二氧化碳的质量或体积,从而推算出含钙量。该反应的化学方程式为______ 。
(2)方案一:如图a所示,利用向上排空气法把二氧化碳收集到瓶内,盖好玻璃片,小心地放到电子天平上称重,扣除原集气瓶的质量,即生成的二氧化碳的质量。某同学认为该方案不合理,可能的原因是______ 。
(3)方案二:小组同学经过讨论,改进成如图b所示的装置进行实验,你认为该装置的优点是______ 。这套装置______ (填“需要”或“不需要”)检查装置的气密性。
【任务二】体积法
(4)小组同学利用图c所示装置,向一袋碳酸钙D3颗粒中,加入20mL稀盐酸,通过测定排出液体的体积来确定二氧化碳的体积。用饱和碳酸氢钠溶液替代水可使实验结果更精确,说明二氧化碳在饱和碳酸氢钠溶液中的溶解性______ (填“强”或“弱”)。
(5)小组同学又经过认真讨论认为排出液体的体积并不等于收集到的二氧化碳的体积,理由是______ 。(注:图c实验中注射器栓塞始终未向上移动)
【任务三】数据处理
(6)第7小组同学并未测到二氧化碳的体积,你认为原因可能是______ 。
(7)按照第9组的数据计算每袋碳酸钙D3颗粒中含钙质量为______ g。
【实验反思】
(8)对比质量法与体积法,我们发现质量法测定结果均小于体积法,试分析出现这一结果的原因可能是______ 。
小组同学还想到了用碱液吸收二氧化碳的方法,该项目有待进一步完善……
(1)【实验原理】测出每袋碳酸钙D3颗粒与足量稀盐酸反应生成二氧化碳的质量或体积,从而推算出含钙量。该反应的化学方程式为
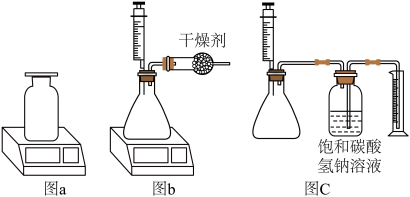
(2)方案一:如图a所示,利用向上排空气法把二氧化碳收集到瓶内,盖好玻璃片,小心地放到电子天平上称重,扣除原集气瓶的质量,即生成的二氧化碳的质量。某同学认为该方案不合理,可能的原因是
(3)方案二:小组同学经过讨论,改进成如图b所示的装置进行实验,你认为该装置的优点是
【任务二】体积法
(4)小组同学利用图c所示装置,向一袋碳酸钙D3颗粒中,加入20mL稀盐酸,通过测定排出液体的体积来确定二氧化碳的体积。用饱和碳酸氢钠溶液替代水可使实验结果更精确,说明二氧化碳在饱和碳酸氢钠溶液中的溶解性
(5)小组同学又经过认真讨论认为排出液体的体积并不等于收集到的二氧化碳的体积,理由是
【任务三】数据处理
质量法 | |||
组序 | 反应前药品+装置质量(g) | 反应后药品+装置质量(g) | 二氧化碳质量 |
1 | 252.778 | 252.366 | 0.414 |
2 | 238.123 | 237.710 | 0.413 |
3 | 220.419 | 220.000 | 0.419 |
4 | 232.060 | 231.620 | 0.440 |
体积法(二氧化碳密度按2g·L-1计算) | ||
组序 | 换算后二氧化碳体积 | 二氧化碳的质量 |
6 | 270 | 0.54 |
7 | 0 | 0 |
8 | 265 | 0.53 |
9 | 275 | 0.55 |
(6)第7小组同学并未测到二氧化碳的体积,你认为原因可能是
(7)按照第9组的数据计算每袋碳酸钙D3颗粒中含钙质量为
【实验反思】
(8)对比质量法与体积法,我们发现质量法测定结果均小于体积法,试分析出现这一结果的原因可能是
小组同学还想到了用碱液吸收二氧化碳的方法,该项目有待进一步完善……
您最近一年使用:0次



