1 . 下列有关二氧化碳的制取及性质实验方案设计中,能达到实验目的的是
A.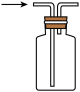 收集 收集 | B.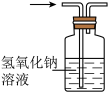 检验 检验 |
C.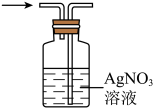 证明 证明 中混入HCl 中混入HCl | D.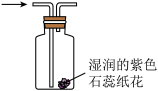 探究 探究 能与 能与 反应 反应 |
您最近一年使用:0次
名校
解题方法
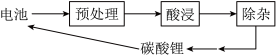
2 . 我国新能源汽车产销量全球第一,汽车废旧锂离子电池是“城市矿山”,回收利用方法有火法和湿法。磷酸铁锂电池湿法回收流程如图所示。 )中Fe和O的元素质量比为
)中Fe和O的元素质量比为______ 。
(2)“预处理”中,拆解电池所得材料中含铁片、铜箔、铝箔等,采用硫酸“酸浸”,反应的化学方程式为______ (任写一条),该反应属于______ (填反应类型)。
(3)“除杂”中,除铁主要发生反应: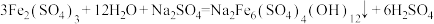 ,该反应中,铁元素的化合价
,该反应中,铁元素的化合价______ (填“升高”“降低”或“不变”,下同),反应后溶液pH______ ,影响除铁效果。“除杂”后得 溶液,加
溶液,加______ (写化学式)发生复分解反应可得碳酸锂沉淀。
(4)火法回收是将电池拆解煅烧后提取金属,与湿法对比,火法的缺点是____________ (写一点)。
 )中Fe和O的元素质量比为
)中Fe和O的元素质量比为(2)“预处理”中,拆解电池所得材料中含铁片、铜箔、铝箔等,采用硫酸“酸浸”,反应的化学方程式为
(3)“除杂”中,除铁主要发生反应:
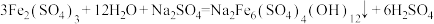 ,该反应中,铁元素的化合价
,该反应中,铁元素的化合价 溶液,加
溶液,加(4)火法回收是将电池拆解煅烧后提取金属,与湿法对比,火法的缺点是
您最近一年使用:0次
3 . 科学使用化学物质,可以保障人体健康。
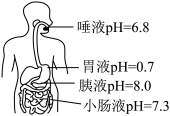
(1)某同学的部分体液的pH如图所示。_______ 。
②该同学胃酸(主要成分为盐酸)过多,可服用胃舒平[主要成分为Al(OH)3]治疗,其原理是_______ (用化学方程式表示)。
(2)某84消毒液产品的部分说明如下表。
①NaClO中氯元素的化合价是_____ ,NaClO属于______ 类。(填酸、碱或盐)
②依据表中信息,将有效氯的质量分数为6.0%的84消毒液10g,配制有效氯的质量分数为0.04%的消毒浸泡液,需要水的质量为_____ 。
③洁厕灵(主要成分为盐酸)与84消毒液混合会产生有毒的氯气(Cl2)。请将该反应的化学方程式补充完整:2HCl + NaClO =_____ + Cl2↑+ H2O。
(1)某同学的部分体液的pH如图所示。
②该同学胃酸(主要成分为盐酸)过多,可服用胃舒平[主要成分为Al(OH)3]治疗,其原理是
(2)某84消毒液产品的部分说明如下表。
| 84消毒液 [产品特点] 主要成分为次氯酸钠(NaClO),有效氯的质量分数为5.1%~6.9%。 [餐具消毒] 用有效氯的质量分数为0.04%的消毒液浸泡,20min后用生活饮用水冲净。 [注意事项] ①外用消毒剂,须稀释后使用。 ②不得将本产品与酸性产品(如洁厕类清洁产品)同时使用。 |
②依据表中信息,将有效氯的质量分数为6.0%的84消毒液10g,配制有效氯的质量分数为0.04%的消毒浸泡液,需要水的质量为
③洁厕灵(主要成分为盐酸)与84消毒液混合会产生有毒的氯气(Cl2)。请将该反应的化学方程式补充完整:2HCl + NaClO =
您最近一年使用:0次
解题方法
4 . 爆炸盐具有强力去污功能,是家庭的好帮手,某市售爆炸盐助洗剂的标签如下图所示。请和小组同学一起研究。
(1)爆炸盐溶于水时会分解成碳酸钠和过氧化氢,过氧化氢进一步分解产生大量气泡,验证气泡中的气体为氧气的方法是________ ;无气泡产生时,往溶液中加入澄清石灰水,产生白色沉淀,反应的化学方程式为________ 。
(2)各取少量羊毛和棉花的布料点燃,能闻到烧焦羽毛气味的是________ 。
(3)厕所清洁剂为含氯清洁剂,与爆炸盐同时使用会造成危险,反应的化学方程式为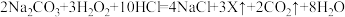 ,则X的化学式为
,则X的化学式为________ 。
(4)爆炸盐置于阴凉干燥处保存的原因是________ 。
| 爆炸盐助洗剂 主要成分: 过碳酸钠(  ) )注意事项: 1.不适合丝、毛和彩棉等衣物 2.若需长时间接触本品,建议带上手套 3.不要与含氯清洁剂同时使用 4.请置于阴凉、干燥处密封存放 |
(2)各取少量羊毛和棉花的布料点燃,能闻到烧焦羽毛气味的是
(3)厕所清洁剂为含氯清洁剂,与爆炸盐同时使用会造成危险,反应的化学方程式为
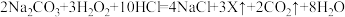 ,则X的化学式为
,则X的化学式为(4)爆炸盐置于阴凉干燥处保存的原因是
您最近一年使用:0次
5 . 实验室对含有 的粗盐进行提纯,步骤如图:
的粗盐进行提纯,步骤如图:______ 。
(2)步骤②中,玻璃棒的作用是__________________ 。
(3)步骤③中,滴加过量 溶液除去
溶液除去 ,反应的化学方程式是
,反应的化学方程式是__________________
(4)步骤⑤中,为除去过量的 ,滴加试剂a后发生的化学反应方程式为
,滴加试剂a后发生的化学反应方程式为__________________ 。
(5)步骤⑥的操作,当__________________ 时,停止加热。
 的粗盐进行提纯,步骤如图:
的粗盐进行提纯,步骤如图: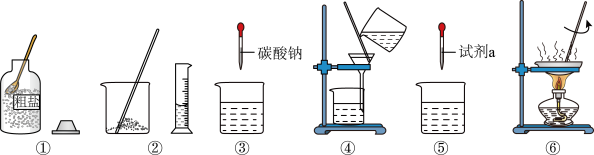
(2)步骤②中,玻璃棒的作用是
(3)步骤③中,滴加过量
 溶液除去
溶液除去 ,反应的化学方程式是
,反应的化学方程式是(4)步骤⑤中,为除去过量的
 ,滴加试剂a后发生的化学反应方程式为
,滴加试剂a后发生的化学反应方程式为(5)步骤⑥的操作,当
您最近一年使用:0次
解题方法
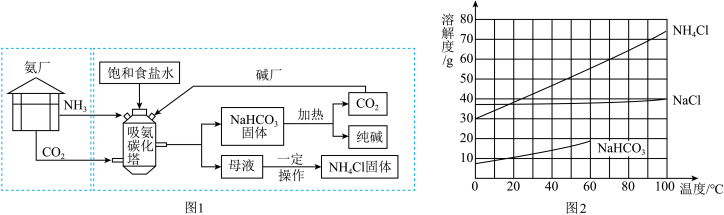
6 . 我国化学家侯德榜先生创立的联合制碱法,将碱厂与氨厂联合,既提高效益,又减少污染,促进了世界制碱工业的发展。联合制碱法的模拟流程如图1所示。三种盐的溶解度随温度变化的曲线如图2所示。吸氨碳化塔中温度控制在30℃~35℃,其中主要发生的反应是: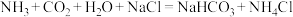
 的溶解度远大于
的溶解度远大于 的溶解度。为了提高产率,吸氨碳化塔中应该先通入的是
的溶解度。为了提高产率,吸氨碳化塔中应该先通入的是______ (填“ ”或“
”或“ ”)。
”)。
(2)加热 制得纯碱的化学方程式是
制得纯碱的化学方程式是__________________ 。
(3)结合图2分析,吸氨碳化塔中析出 固体的主要原因是
固体的主要原因是__________________ 。
(4)氨厂生产的 溶于水后得到的氨水可以做氮肥。碱厂与氨厂联合后,用
溶于水后得到的氨水可以做氮肥。碱厂与氨厂联合后,用 (固体)代替氨水做氮肥,其优势是
(固体)代替氨水做氮肥,其优势是__________________ (答一点即可)。
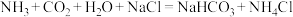
 的溶解度远大于
的溶解度远大于 的溶解度。为了提高产率,吸氨碳化塔中应该先通入的是
的溶解度。为了提高产率,吸氨碳化塔中应该先通入的是 ”或“
”或“ ”)。
”)。(2)加热
 制得纯碱的化学方程式是
制得纯碱的化学方程式是(3)结合图2分析,吸氨碳化塔中析出
 固体的主要原因是
固体的主要原因是(4)氨厂生产的
 溶于水后得到的氨水可以做氮肥。碱厂与氨厂联合后,用
溶于水后得到的氨水可以做氮肥。碱厂与氨厂联合后,用 (固体)代替氨水做氮肥,其优势是
(固体)代替氨水做氮肥,其优势是
您最近一年使用:0次
解题方法
7 . 鉴别、检验、除杂与分离提纯是进行化学研究的重要方法。下列实验方案能达到实验目的的是
选项 | 实验目的 | 实验方案 |
A | 鉴别稀盐酸和稀硫酸 | 取样,分别加入氯化钡溶液观察是否有沉淀 |
B | 检验敞口放置的 溶液是否变质 溶液是否变质 | 取样,滴加酚酞溶液,观察颜色 |
C | 除去 溶液中少量的 溶液中少量的 杂质 杂质 | 加入适量的 溶液,过滤 溶液,过滤 |
D | 硝酸钾中混有少量氯化钠,提纯硝酸钾 | 加热水配成硝酸钾热饱和溶液,降温结晶、过滤、洗涤、干燥 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
8 . 中国传统文化包罗万象,如《天工开物》中记载了丰富的化学知识,下列有关说法正确的是
| A.“石胆(注:硫酸铜),故绿色带宝光”描述的是含硫酸根物质的颜色 |
| B.“凡石灰,经火焚炼为用”,其中的“石灰”指的是氢氧化钙 |
| C.“凡金箔每金七分造方寸金一千片”说明金具有良好的延展性 |
| D.“欲去杂还纯,再入水煎炼…倾入盆中,经宿结成白雪”描述的是粗盐提纯过程 |
您最近一年使用:0次
解题方法
9 . 化学反应是化学研究的重要范畴,但是有的实验会伴随明显现象,有的实验并无明显现象,某兴趣小组对某些化学变化进行研究,根据实验内容,回答问题:
(1)实验一:向装有CuO的试管中加入一定量的稀硫酸,会观察到明显的______ 现象,可见该反应已发生。
【实验内容二】探究某些溶液相互反应后的溶质成分
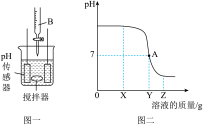
(2)实验二:为了证明氢氧化钠溶液和稀硫酸发生了反应,其反应的方程式为______ ,该组同学设计了如下图一所示实验 传感器测定的pH随溶液质量变化情况如图二所示 则B溶液是______ 溶液。
【提出问题】氢氧化钠溶液和稀硫酸反应后溶液中的溶质成分有哪些?
【实验猜想】
猜想一:只有Na2SO4
猜想二:Na2SO4和NaOH
猜想三:Na2SO4和H2SO4
猜想四: Na2SO4、H2SO4和NaOH
兴趣小组成员一致认为猜想四不合理,理由是氢氧化钠和硫酸反应,不能共存 。
【实验方案】
(3)为确认哪个猜想成立,兴趣小组进行如下实验,请填空:
【实验反思】
(4)小组成员认为该实验方案不能得出猜想三成立,理由是______ 。
(5)下列物质单独使用能够检验猜想三成立的是应改用的试剂是______(填序号)。
(1)实验一:向装有CuO的试管中加入一定量的稀硫酸,会观察到明显的
【实验内容二】探究某些溶液相互反应后的溶质成分
(2)实验二:为了证明氢氧化钠溶液和稀硫酸发生了反应,其反应的方程式为
【提出问题】氢氧化钠溶液和稀硫酸反应后溶液中的溶质成分有哪些?
【实验猜想】
猜想一:只有Na2SO4
猜想二:Na2SO4和NaOH
猜想三:Na2SO4和H2SO4
猜想四: Na2SO4、H2SO4和NaOH
兴趣小组成员一致认为猜想四不合理,理由是氢氧化钠和硫酸反应,不能共存 。
【实验方案】
(3)为确认哪个猜想成立,兴趣小组进行如下实验,请填空:
| 分别取样于试管中 | 步骤 | 现象 | 结论 |
| 向其中一份中滴加酚酞溶液,振荡 | 猜想二不成立 | ||
| 向另一份中滴加Ba(NO3)2溶液,振荡 | 出现白色沉淀 | 猜想三成立 |
【实验反思】
(4)小组成员认为该实验方案不能得出猜想三成立,理由是
(5)下列物质单独使用能够检验猜想三成立的是应改用的试剂是______(填序号)。
| A.pH试纸 | B.铜 | C.紫色石蕊试液 | D.硫酸铜 | E.镁条 |
您最近一年使用:0次
解题方法
10 . 为测定某胃药中碳酸氢钠的含量,向一锥形瓶中加入10g该胃药,再逐渐加入一定溶质质量分数的稀盐酸,当观察到气泡不再产生现象时,说明碳酸氢钠已完全反应。此时用去稀盐酸的质量是50g,测得锥形瓶内剩余物质质量是55.6g(假设胃药中的其他成分不参与反应,不考虑稀盐酸挥发,反应产生的气体全部逸出)。
(1)完全反应后,产生的二氧化碳的质量为__ g。
(2)计算该胃药中碳酸氢钠的质量分数(写出计算过程)。
(1)完全反应后,产生的二氧化碳的质量为
(2)计算该胃药中碳酸氢钠的质量分数(写出计算过程)。
您最近一年使用:0次



