解题方法
1 . 科学思维是从化学视角研究物质及其变化规律的思路与方法,下列说法正确的是
| A.变化与守恒:依据质量守恒定律,12gC和12gO2充分反应可得到24gCO2 |
| B.宏观与微观:氧气和液氧物理性质差异较大,因为两者的分子间隔不同 |
| C.模型与推理:化学反应伴随能量的变化,有能量变化的一定是化学反应 |
| D.探究与创新:探究氧化铜是否为过氧化氢分解的催化剂,只需设计实验证明氧化铜能否改变过氧化氢分解速率即可 |
您最近一年使用:0次
解题方法
2 . 分析推理是化学学习中常用的思维方法。下列分析推理正确的是
| A.CO2溶于水呈酸性,故酸雨是由CO2引起的 |
| B.碱溶液呈碱性,故呈碱性的溶液一定都是碱溶液 |
| C.化学反应时伴随着能量的变化,但有能量变化的不一定发生化学反应 |
| D.碳酸盐与盐酸反应放出气体,故能与盐酸反应放出气体的物质一定是碳酸盐 |
您最近一年使用:0次
解题方法
3 . 一种“贴身暖宝宝”贴的标签如图所示,下列说法错误的是

| A.铁粉和活性炭都属于单质 |
| B.暖宝宝中加入稀硫酸会产生气泡 |
| C.暖宝宝发热的原理主要是利用铁生锈放热 |
| D.内袋使用透气材料的原因是使袋内的物质与氧气接触 |
您最近一年使用:0次
解题方法
4 . 阅读下面科普短文,并回答问题。
从2014年起,我国新能源汽车产销量连续九年位居世界第一。与传统汽车使用化石燃料不同,新能源汽车的能量来源更加多元化。电动汽车:电池能为电动汽车提供动力,几类电池的部分性能指标如图1所示,其中能量密度表示单位体积的电池所具有的能量。氢内燃车:氢内燃车以氢气为燃料,不排放任何污染物;氢气可通过电解水(原理如图2)等多种方式获得。据测算,1kg氢气完全燃烧可释放14.3×104KJ的热量,1kg汽油完全燃烧可释放4.6×104KJ的热量。乙醇汽车:乙醇汽车以乙醇为燃料,乙醇是可再生能源,可以通过发酵甘蔗、玉米等农作物,或发酵粮食收割后剩余的秸秆大量提取。在新能源汽车发展领域,我国和西方发达国家处于同一起跑线上,并有望引领汽车的发展。_________ 。
(2)以氢气为燃料的汽车优点是:___________________ 。氢气可通过电解水,煤气化,天然气重整等多种方式获得,最理想的制氢气方法是在合适的催化剂作用下,利用太阳光使水分解制氢,该制氢过程_______ (填“吸收”或“放出”)能量。
(3)下列说法正确的是 (填序号)。
从2014年起,我国新能源汽车产销量连续九年位居世界第一。与传统汽车使用化石燃料不同,新能源汽车的能量来源更加多元化。电动汽车:电池能为电动汽车提供动力,几类电池的部分性能指标如图1所示,其中能量密度表示单位体积的电池所具有的能量。氢内燃车:氢内燃车以氢气为燃料,不排放任何污染物;氢气可通过电解水(原理如图2)等多种方式获得。据测算,1kg氢气完全燃烧可释放14.3×104KJ的热量,1kg汽油完全燃烧可释放4.6×104KJ的热量。乙醇汽车:乙醇汽车以乙醇为燃料,乙醇是可再生能源,可以通过发酵甘蔗、玉米等农作物,或发酵粮食收割后剩余的秸秆大量提取。在新能源汽车发展领域,我国和西方发达国家处于同一起跑线上,并有望引领汽车的发展。
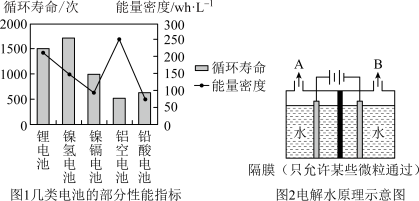
(2)以氢气为燃料的汽车优点是:
(3)下列说法正确的是 (填序号)。
| A.依据图1可知,镍氢电池优于铝空电池的性能指标是循环寿命。 |
| B.图2中,B出口产生的气体为氢气 |
| C.农业大国盛产薯类和玉米,有利于推广乙醇汽车 |
| D.报废的电动汽车电池,要及时用土进行掩埋处理 |
您最近一年使用:0次
名校
解题方法
5 . 氢能是一种来源丰富、绿色低碳、应用广泛的二次能源,被誉为21世纪的“终极能源”。科学家们正积极开展制氢研究。
(1)方法一:用风力、光伏发电,然后电解水制氢。这是将电能转化为_______ 能。
(2)方法二:PEM电解水制氢。基本原理如图所示。观察示意图判断其中能穿过质子交换膜的是_______ 。
①反应中2%La2O3—98%TiO2的作用是_______ ,反应的化学方程式为_______ 。
②Ti是钛元素的化学符号,钛和钛合金被誉为21世纪最重要的_______ (填“金属”或“非金属”)材料,TiO2的化学名称为_______ 。
(4)方法三与方法一、方法二对比,其优点是_______ 。
(1)方法一:用风力、光伏发电,然后电解水制氢。这是将电能转化为
(2)方法二:PEM电解水制氢。基本原理如图所示。观察示意图判断其中能穿过质子交换膜的是
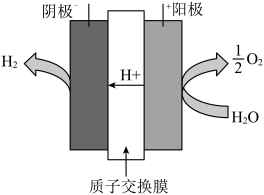
①反应中2%La2O3—98%TiO2的作用是
②Ti是钛元素的化学符号,钛和钛合金被誉为21世纪最重要的
(4)方法三与方法一、方法二对比,其优点是
您最近一年使用:0次
7日内更新
|
317次组卷
|
3卷引用:2024年广东省中山市万阅百校联盟三模化学试题
解题方法
6 . 化学小组在“设计和制作简易供氧器”的实践活动中,探究影响供氧剂过碳酸钠产氧速率的因素。
【查阅资料】
Ⅰ. 化学小组研究了图1所示的某品牌制氧机的装置原理后,利用身边物品自制了如图2所示的简易供氧器。
实验1:探究药品用量、温度对产氧速率的影响
【进行实验】在不同温度下,取一定质量的过碳酸钠和MnO2放入b瓶中,并加入相同体积的水,测得平均产氧速率数据如下表所示。
实验2:探究加水量对产氧速率的影响
【进行实验】20℃时,取一定质量的过碳酸钠和MnO2放入b瓶中,并加入不同体积的水,测得平均产氧速率及反应过程中温度变化数据如下表所示。
【解释与结论】
(1)实验中,过氧化氢分解生成氧气的化学方程式为_______ 。
(2)设计实验①②的目的是_______ 。
(3)由①③可以得到的结论是_______ 。
(4)⑤中x应为_______ 。
(5)依据实验2可知,该制氧过程中发生的化学反应属于_______ (填“吸热”或“放热”)反应。
【反思与评价】
(6)由上述实验可知,适当增加加水量可减缓产氧速率,其证据是_______ 。
(7)某同学欲进一步探究MnO2质量对产氧速率有影响,设计的实验方案是:20℃时,_______ 。
【查阅资料】
Ⅰ. 化学小组研究了图1所示的某品牌制氧机的装置原理后,利用身边物品自制了如图2所示的简易供氧器。
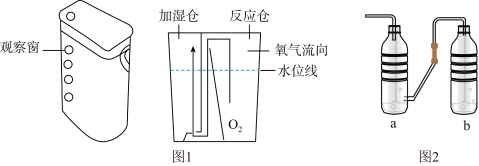
实验1:探究药品用量、温度对产氧速率的影响
【进行实验】在不同温度下,取一定质量的过碳酸钠和MnO2放入b瓶中,并加入相同体积的水,测得平均产氧速率数据如下表所示。
| 序号 | 过碳酸钠质量/g | MnO2质量/g | 温度/℃ | 平均产氧速率mL/s |
| ① | 10 | 0.3 | 26 | 2.73 |
| ② | 20 | 0.3 | 26 | 8.56 |
| ③ | 10 | 0.3 | 41 | 4.54 |
【进行实验】20℃时,取一定质量的过碳酸钠和MnO2放入b瓶中,并加入不同体积的水,测得平均产氧速率及反应过程中温度变化数据如下表所示。
| 序号 | 过碳酸钠质量/g | MnO2质量/g | 加水体积/mL | 反应液最高温度/℃ | 平均产氧速率mL/s |
| ④ | 240 | 2.5 | 350 | 98 | 33.3 |
| ⑤ | x | 2.5 | 500 | 74 | 15 |
| ⑥ | 240 | 2.5 | 800 | 53 | 10 |
(1)实验中,过氧化氢分解生成氧气的化学方程式为
(2)设计实验①②的目的是
(3)由①③可以得到的结论是
(4)⑤中x应为
(5)依据实验2可知,该制氧过程中发生的化学反应属于
【反思与评价】
(6)由上述实验可知,适当增加加水量可减缓产氧速率,其证据是
(7)某同学欲进一步探究MnO2质量对产氧速率有影响,设计的实验方案是:20℃时,
您最近一年使用:0次
7 . 利用如图装置测定空气中氧气含量(实验前注射器活塞拉至70mL处,忽略胶头滴管中水所占的体积)。
已知:白磷的着火点为40℃。
已知:白磷的着火点为40℃。
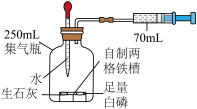
| 实验步骤和现象 | 实验解释 |
| Ⅰ、将胶头滴管中的水滴入生石灰中、 | 生石灰与水反应放出热量所达到的温度范围是 |
| Ⅱ、一段时间后,白磷开始燃烧。 | |
| Ⅲ、注射器中的活塞先向右移再向左移,最终停在 | 氧气约占空气体积的1/5。 |
您最近一年使用:0次
解题方法
8 . 阅读科普内容,回答相关问题:
化学发光是普遍存在的自然现象,绝大多数化学发光反应的发光强度都很弱。目前应用于分析化学的化学发光体系主要是一些强发光体系,这有助于提高分析灵敏度。鲁米诺(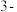 氨基
氨基 苯二甲酰肼)是目前最常用的化学发光试剂。在碱性水溶液中,鲁米诺被过氧化氢、铁氰化钾等氧化剂氧化为激发态的
苯二甲酰肼)是目前最常用的化学发光试剂。在碱性水溶液中,鲁米诺被过氧化氢、铁氰化钾等氧化剂氧化为激发态的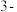 氨基邻苯二甲酸盐,并发出蓝色可见光。刑侦中的血迹鉴定就是基于血液中的红细胞可显著地增强鲁米诺一过氧化氢体系的化学发光;当在疑似血迹处喷上这种化学发光试剂时,在暗处用肉眼即可观察到蓝色的化学发光。
氨基邻苯二甲酸盐,并发出蓝色可见光。刑侦中的血迹鉴定就是基于血液中的红细胞可显著地增强鲁米诺一过氧化氢体系的化学发光;当在疑似血迹处喷上这种化学发光试剂时,在暗处用肉眼即可观察到蓝色的化学发光。
目前,化学发光分析法已广泛应用于生物医学分析、药物分析、环境监测以及食品安全等领域,成为一种重要的分析手段。
(1)化学发光中有能量转换,主要由化学能转换为______ (填“热能”或“光能”);
(2)不是所有化学发光体系都已应用于分析化学,理由是______ ;
(3)在碱性条件下,鲁米诺能被铁氰化钾氧化而发出蓝色可见光,说明化学反应的发生需要一定的______ 。
化学发光
在某些化学反应中,反应产生的能量可以通过光辐射的形式释放出来,这种现象称为化学发光。化学发光是普遍存在的自然现象,绝大多数化学发光反应的发光强度都很弱。目前应用于分析化学的化学发光体系主要是一些强发光体系,这有助于提高分析灵敏度。鲁米诺(
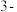 氨基
氨基 苯二甲酰肼)是目前最常用的化学发光试剂。在碱性水溶液中,鲁米诺被过氧化氢、铁氰化钾等氧化剂氧化为激发态的
苯二甲酰肼)是目前最常用的化学发光试剂。在碱性水溶液中,鲁米诺被过氧化氢、铁氰化钾等氧化剂氧化为激发态的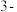 氨基邻苯二甲酸盐,并发出蓝色可见光。刑侦中的血迹鉴定就是基于血液中的红细胞可显著地增强鲁米诺一过氧化氢体系的化学发光;当在疑似血迹处喷上这种化学发光试剂时,在暗处用肉眼即可观察到蓝色的化学发光。
氨基邻苯二甲酸盐,并发出蓝色可见光。刑侦中的血迹鉴定就是基于血液中的红细胞可显著地增强鲁米诺一过氧化氢体系的化学发光;当在疑似血迹处喷上这种化学发光试剂时,在暗处用肉眼即可观察到蓝色的化学发光。目前,化学发光分析法已广泛应用于生物医学分析、药物分析、环境监测以及食品安全等领域,成为一种重要的分析手段。
(1)化学发光中有能量转换,主要由化学能转换为
(2)不是所有化学发光体系都已应用于分析化学,理由是
(3)在碱性条件下,鲁米诺能被铁氰化钾氧化而发出蓝色可见光,说明化学反应的发生需要一定的
您最近一年使用:0次
7日内更新
|
71次组卷
|
2卷引用:2024年湖南省岳阳市三湘C18联盟中考全真模拟压轴大联考化学试卷
解题方法
9 . 化学与人类的关系非常密切,它在各个领域都有广泛的应用,为人类提供了更加优质、方便、有益的生活条件和生产方式。如:
(1)医疗领域:医生常会给病人输送一种能供给呼吸的气体是___ 。
(2)食品领域:榕江“村超”将贵州的美食介绍给了全世界,其中最受欢迎的美食之一是卷粉,其配料有豆腐皮、腊肉、酸笋、花生等,请写出富含的营养素:____ (列举一种即可)。
(3)冶金领域:焦炭在金属冶炼中是一种重要的原料,请写出它在氧气充足的条件下燃烧的化学方程式:_____________ ,该反应是____ (填“吸热”或“放热”)反应。
(4)农业领域:贵州息烽红岩葡萄享有盛誉,为了促进葡萄生长,常施用的化肥有K2SO4、CO(NH2)2、Ca3(PO4)2,其中属于钾肥的是___ 。
(5)材料领域:2023年12月26日,贵阳市地铁3号线正式开通运营,为市民出行带来极大便利。地铁车厢地面普遍采用PVC材料,PVC是__________ (填“有机合成材料”或“金属材料”)。
(1)医疗领域:医生常会给病人输送一种能供给呼吸的气体是
(2)食品领域:榕江“村超”将贵州的美食介绍给了全世界,其中最受欢迎的美食之一是卷粉,其配料有豆腐皮、腊肉、酸笋、花生等,请写出富含的营养素:
(3)冶金领域:焦炭在金属冶炼中是一种重要的原料,请写出它在氧气充足的条件下燃烧的化学方程式:
(4)农业领域:贵州息烽红岩葡萄享有盛誉,为了促进葡萄生长,常施用的化肥有K2SO4、CO(NH2)2、Ca3(PO4)2,其中属于钾肥的是
(5)材料领域:2023年12月26日,贵阳市地铁3号线正式开通运营,为市民出行带来极大便利。地铁车厢地面普遍采用PVC材料,PVC是
您最近一年使用:0次
7日内更新
|
30次组卷
|
2卷引用:2024 年贵州省贵阳市息烽县初中学业水平考试适应性测试理综-初中化学
解题方法
10 . 我国高度重视并积极推动氢能技术与产业发展,近年来我国制氢量已位居世界第一。
(1)制氢方法一:水光解制氢。
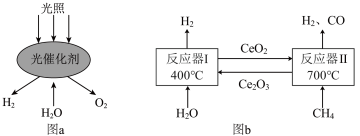
①水在光催化剂作用下制备氢气的原理如图a所示。光解水时,由______ 能转化为化学能;在反应过程中,光催化剂在反应前后的质量和______ 不变。
②三氧化二铈(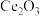 )中铈元素的化合价是
)中铈元素的化合价是______ 。
③图b中反应器Ⅱ内在催化剂作用下发生反应的化学方程式为______ ,且对反应器Ⅱ的生成气体需要进行______ 。
(2)①新型镁铝合金(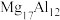 )是一种储氢材料,在氩气的氛围中,将一定比例的金属镁和铝熔炼得到镁铝合金。熔炼时须通入氩气,其目的是
)是一种储氢材料,在氩气的氛围中,将一定比例的金属镁和铝熔炼得到镁铝合金。熔炼时须通入氩气,其目的是______ 。
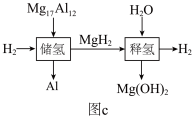
②镁铝合金储氢和释氢过程(如图c)释放的比储存的H2______ (填“多”或“少”)。______ 。(写两点)
(1)制氢方法一:水光解制氢。
①水在光催化剂作用下制备氢气的原理如图a所示。光解水时,由
②三氧化二铈(
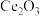 )中铈元素的化合价是
)中铈元素的化合价是③图b中反应器Ⅱ内在催化剂作用下发生反应的化学方程式为
(2)①新型镁铝合金(
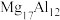 )是一种储氢材料,在氩气的氛围中,将一定比例的金属镁和铝熔炼得到镁铝合金。熔炼时须通入氩气,其目的是
)是一种储氢材料,在氩气的氛围中,将一定比例的金属镁和铝熔炼得到镁铝合金。熔炼时须通入氩气,其目的是②镁铝合金储氢和释氢过程(如图c)释放的比储存的H2
您最近一年使用:0次



