1 . 海洋封存是实现“碳中和”的途径之一,其原理是利用水等液体吸收CO2实现减碳目标。某科学小组对“二氧化碳气体的收集”这一课题开展了探究。
【提出问题】二氧化碳气体在水和食盐水中溶解能力相同吗?
【建立建设】二氧化碳气体在食盐水中溶解能力更强。
【实验设计与操作】
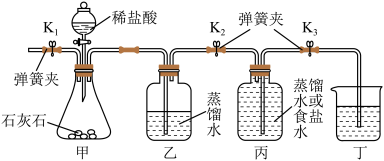
(1)实验时,需先将甲装置中的空气排尽。其操作是:打开弹簧夹K1,关闭弹簧夹K2,打开活塞,滴加稀盐酸至空气排尽。检验空气已排尽的方法是__________ 。
(2)关闭K1,打开K2、K3,分别用排水法、排食盐水法收集CO2,且每隔一段时间测出丁烧杯中液体的体积,测得数据如下:
根据以上数据分析,能用排水法收集CO2的理由是_________ 。
【实验结论】相同条件下,二氧化碳在_________ 中溶解能力更强。
(3)小组同学想了解水吸收CO2后溶液的酸碱性情况,在实验中做了以下操作,待丙装置中收集半瓶气体时,关闭活塞K2和K3,充分振荡丙装置。然后用pH计测得如下数据:
分析可知,在丙和丁装置中所溶解二氧化碳的体积___________ (选填“大于”、“小于”或“等于”)丙和丁装置中溶液的总体积。
【实验反思】海洋封存CO2后可能会带来哪些危害?_________ (写出一点即可)
【提出问题】二氧化碳气体在水和食盐水中溶解能力相同吗?
【建立建设】二氧化碳气体在食盐水中溶解能力更强。
【实验设计与操作】
(1)实验时,需先将甲装置中的空气排尽。其操作是:打开弹簧夹K1,关闭弹簧夹K2,打开活塞,滴加稀盐酸至空气排尽。检验空气已排尽的方法是
(2)关闭K1,打开K2、K3,分别用排水法、排食盐水法收集CO2,且每隔一段时间测出丁烧杯中液体的体积,测得数据如下:
| 时间/min | 0 | 0.5 | 6 | 12 | 24 | 48 |
| 排水法时丁中水的体积/mL | 0 | 2.5 | 14.5 | 23 | 34 | 41 |
| 排盐水法时丁中盐水的体积/mL | 0 | 1 | 7 | 9.5 | 11 | 12 |
【实验结论】相同条件下,二氧化碳在
(3)小组同学想了解水吸收CO2后溶液的酸碱性情况,在实验中做了以下操作,待丙装置中收集半瓶气体时,关闭活塞K2和K3,充分振荡丙装置。然后用pH计测得如下数据:
| 物质 | 丁装置中溶液 | 丙装置中溶液 |
| pH | 6.50 | 5.60 |
【实验反思】海洋封存CO2后可能会带来哪些危害?
您最近一年使用:0次
名校
2 . 某科学小组利用下图装置对 晶体中结晶水的含量进行测定(铁架台等已省略)。已知:
晶体中结晶水的含量进行测定(铁架台等已省略)。已知:
① 和
和 加热时易被空气中的氧气氧化;②
加热时易被空气中的氧气氧化;② 。
。
实验步骤如下:
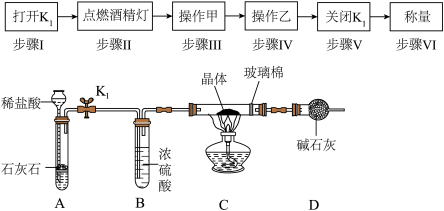
(1)步骤I打开 导入二氧化碳气体,排尽装置中的空气,其目的是
导入二氧化碳气体,排尽装置中的空气,其目的是___________ 。
(2)有同学建议,为加快产生 的速度,可将A装置中的稀盐酸浓度增大、石灰石磨成粉状。试问,制取气体时反应速度是否越快越好?其理由是
的速度,可将A装置中的稀盐酸浓度增大、石灰石磨成粉状。试问,制取气体时反应速度是否越快越好?其理由是_____________ 。
(3)步骤Ⅵ称量,若晶体 质量为m,反应前后C装置的质量减少了
质量为m,反应前后C装置的质量减少了 ,D装置的质量增加了
,D装置的质量增加了 ,则此晶体中结晶水的百分含量为
,则此晶体中结晶水的百分含量为____________ (用字母表示)。
 晶体中结晶水的含量进行测定(铁架台等已省略)。已知:
晶体中结晶水的含量进行测定(铁架台等已省略)。已知:①
 和
和 加热时易被空气中的氧气氧化;②
加热时易被空气中的氧气氧化;② 。
。实验步骤如下:
(1)步骤I打开
 导入二氧化碳气体,排尽装置中的空气,其目的是
导入二氧化碳气体,排尽装置中的空气,其目的是(2)有同学建议,为加快产生
 的速度,可将A装置中的稀盐酸浓度增大、石灰石磨成粉状。试问,制取气体时反应速度是否越快越好?其理由是
的速度,可将A装置中的稀盐酸浓度增大、石灰石磨成粉状。试问,制取气体时反应速度是否越快越好?其理由是(3)步骤Ⅵ称量,若晶体
 质量为m,反应前后C装置的质量减少了
质量为m,反应前后C装置的质量减少了 ,D装置的质量增加了
,D装置的质量增加了 ,则此晶体中结晶水的百分含量为
,则此晶体中结晶水的百分含量为
您最近一年使用:0次
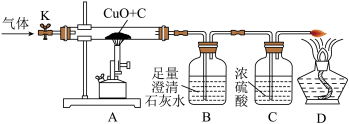
3 . 如图所示是木炭还原氧化铜的实验,小科对碳与氧化铜反应生成的气体成分进行探究。[提出问题]碳燃烧时可能生成CO2,也可能生成CO,那么碳与氧化铜反应生成的气体是否也有多种可能?
猜想①:CO;猜想②:CO2;
猜想③:CO和CO2。
[设计方案]打开K,缓缓通入干燥的氮气一段时间,关闭K,点燃酒精喷灯和酒精灯,充分反应后,熄灭酒精喷灯和酒精灯,打开K,再通一段时间氮气。
方案一:从定性观察角度判断
(1)若观察到B中澄清石灰水变浑浊,则可排除猜想_______ 。
(2)实验结束后,需要先熄灭(选填“A”或“D”)_______ 酒精灯。
(3)方案二:从定量计算角度判断取一定量炭粉和4g氧化铜的混合物进行实验,并测定表格中的四个数据:
若猜想②成立,则理论上(m4-m3)_______ (m1-m2)(填“>”“=”或“<”)。
(4)若猜想③成立且CuO全部转化成Cu,则参加反应碳的质量m的取值范围是________________ 。
猜想①:CO;猜想②:CO2;
猜想③:CO和CO2。
[设计方案]打开K,缓缓通入干燥的氮气一段时间,关闭K,点燃酒精喷灯和酒精灯,充分反应后,熄灭酒精喷灯和酒精灯,打开K,再通一段时间氮气。
方案一:从定性观察角度判断
(1)若观察到B中澄清石灰水变浑浊,则可排除猜想
(2)实验结束后,需要先熄灭(选填“A”或“D”)
(3)方案二:从定量计算角度判断取一定量炭粉和4g氧化铜的混合物进行实验,并测定表格中的四个数据:
| 反应前的质量 | 反应后的质量 | |
| A(玻璃管+固) | m1 | m2 |
| B+C+(广口瓶+混合液) | m3 | m4 |
(4)若猜想③成立且CuO全部转化成Cu,则参加反应碳的质量m的取值范围是
您最近一年使用:0次
2023·浙江·一模
4 . 实验室现有:氯酸钾、二氧化锰、块状大理石、稀硫酸、稀盐酸、浓硫酸等药品及部分实验装置,请回答以下问题。

(1)根据提供的药品,写出实验室制取CO2的化学方程式______ ;
(2)利用氯酸钾、二氧化锰制取并收集一瓶干燥的氧气,所选装置正确连接的顺序是______ (用字母表示)。

(1)根据提供的药品,写出实验室制取CO2的化学方程式
(2)利用氯酸钾、二氧化锰制取并收集一瓶干燥的氧气,所选装置正确连接的顺序是
您最近一年使用:0次
2023·浙江·一模
5 . 衢州山区石灰石资源丰富。用石灰石和砂岩粘土高温煅烧可得一种新型水泥熟料,主要反应为:CaCO3+SiO2 CaSiO3+CO2↑
CaSiO3+CO2↑

(1)CaSiO3中硅元素的化合价为___________ 。
(2)在实验室,用如图所示方法粗略测定石灰石中CaCO3的质量分数,可不需测定的数据是___________ (填序号)。
A.取用石灰石样品的质量 B.倒入的过量稀盐酸的质量
C.盐酸接触样品前电子称的读数 D.反应停止后电子秤的读数
(3)用含CaCO390%的石灰石1000t生产新型水泥熟料,理论上会排放CO2多少吨?___________ (写出计算过程)
 CaSiO3+CO2↑
CaSiO3+CO2↑
(1)CaSiO3中硅元素的化合价为
(2)在实验室,用如图所示方法粗略测定石灰石中CaCO3的质量分数,可不需测定的数据是
A.取用石灰石样品的质量 B.倒入的过量稀盐酸的质量
C.盐酸接触样品前电子称的读数 D.反应停止后电子秤的读数
(3)用含CaCO390%的石灰石1000t生产新型水泥熟料,理论上会排放CO2多少吨?
您最近一年使用:0次
2023·浙江·一模
6 . 下图是实验室中常见的一些装置,请根据所学知识回答下列问题:

(1)仪器①的名称是___________ 。
(2)实验室制取二氧化碳的发生装置可选择___________ (填字母)。
(3)小明采用图C方法检验二氧化碳的性质,观察到蜡烛熄灭。该现象除了能说明二氧化碳不能燃烧外,还能说明二氧化碳具有___________ 的性质。

(1)仪器①的名称是
(2)实验室制取二氧化碳的发生装置可选择
(3)小明采用图C方法检验二氧化碳的性质,观察到蜡烛熄灭。该现象除了能说明二氧化碳不能燃烧外,还能说明二氧化碳具有
您最近一年使用:0次
2023·浙江·一模
7 . 实验室有一瓶碳酸钙和氯化钙粉末组成的均匀混合物,小科在装有200.0g某浓度的稀盐酸中不断缓慢加入该混合物,充分反应后所得溶液(所得溶液均为不饱和溶液)与所加混合物关系如图所示:
(1)求混合物中碳酸钙和氯化钙质量之比___________ 。
(2)当加入36g混合物时,此时剩余固体质量为___________ 。

(3)当加入48g混合物时,所得溶液的溶质质量分数是多少___________ ?(写出计算过程,结果精确到0.1%)

(1)求混合物中碳酸钙和氯化钙质量之比
(2)当加入36g混合物时,此时剩余固体质量为

(3)当加入48g混合物时,所得溶液的溶质质量分数是多少

您最近一年使用:0次
2023·浙江·一模
8 . 实验室可以选用如图所示的装置,制取二氧化碳气体并进行有关实验。请回答下到问题:

(1)把A装置与E装置连接,发现E装置中溶液变浑浊,则证明二氧化碳气体中混有______ 气体;
(2)若要制取收集一瓶纯净、干燥的二氧化碳气体,请从上述各装置中选择适当的装置进行连接,连接顺序是______ 。(填字母)

(1)把A装置与E装置连接,发现E装置中溶液变浑浊,则证明二氧化碳气体中混有
(2)若要制取收集一瓶纯净、干燥的二氧化碳气体,请从上述各装置中选择适当的装置进行连接,连接顺序是
您最近一年使用:0次
2023·浙江·一模
9 . 某科学兴趣小组为测定大理石中碳酸钙的含量,进行如图1所示实验:将过量的稀盐酸加入到20克大理石中(其他成分不溶于水也不与盐酸反应),把产生的CO2气体用足量的烧碱溶液吸收,同时测量B瓶烧碱溶液增加的质量,结果如下表所示。

(1)上表中,x=___________ 。
(2)该大理石样品中碳酸钙的质量分数为多少?___________
(3)请在图2中画出剩余固体的质量随时间变化规律的关系曲线。___________
(4)利用该装置进行实验,测得的结果可能会偏大,原因是___________ 。

时间/分 | 0 | 2 | 4 | 6 | 8 | 10 |
B增加质量/克 | 0 | 4.4 | 6.6 | 7.04 | x | 7.04 |
(2)该大理石样品中碳酸钙的质量分数为多少?
(3)请在图2中画出剩余固体的质量随时间变化规律的关系曲线。
(4)利用该装置进行实验,测得的结果可能会偏大,原因是
您最近一年使用:0次
2023·浙江·一模
10 . 珍珠粉的主要成分是碳酸钙,其作为一种新型补钙剂,越来越受人们的青睐。兴趣小组利用图甲装置测定人工养殖珍珠中碳酸钙的含量。实验步骤如下:

①检查装置气密性。
②注射器活塞推到底部,向装置内装入1.25g磨成粉的珍珠样品,分液漏斗内加入足量盐酸,再次连接装置。
③打开分液漏斗活塞,将20mL足量稀盐酸加入装置后立即关闭活塞,充分反应后,观察到气泡不再产生,记录此时注射器的示数为240mL。
资料:标准状况下,二氧化碳气体的密度约为2.0g/L;珍珠粉中其它成分不与稀盐酸反应,反应的化学方程式为 ↑;甲装置固定装置略,不考虑活塞的摩擦和自重。
↑;甲装置固定装置略,不考虑活塞的摩擦和自重。
(1)检查装置气密性:关闭分液漏斗活塞,将注射器活塞底部从0mL处向上拉至100mL.如果气密性良好,松手后能观察到的现象是______ 。
(2)求该人工养殖珍珠中碳酸钙的质量分数。______
(3)结合图乙药房售卖的某品牌珍珠粉说明书,你认为上述人工养殖珍珠磨成粉是否可内服,你的理由是______ 。

①检查装置气密性。
②注射器活塞推到底部,向装置内装入1.25g磨成粉的珍珠样品,分液漏斗内加入足量盐酸,再次连接装置。
③打开分液漏斗活塞,将20mL足量稀盐酸加入装置后立即关闭活塞,充分反应后,观察到气泡不再产生,记录此时注射器的示数为240mL。
资料:标准状况下,二氧化碳气体的密度约为2.0g/L;珍珠粉中其它成分不与稀盐酸反应,反应的化学方程式为
 ↑;甲装置固定装置略,不考虑活塞的摩擦和自重。
↑;甲装置固定装置略,不考虑活塞的摩擦和自重。(1)检查装置气密性:关闭分液漏斗活塞,将注射器活塞底部从0mL处向上拉至100mL.如果气密性良好,松手后能观察到的现象是
(2)求该人工养殖珍珠中碳酸钙的质量分数。
(3)结合图乙药房售卖的某品牌珍珠粉说明书,你认为上述人工养殖珍珠磨成粉是否可内服,你的理由是
您最近一年使用:0次



