1 . 以硫酸工业产生的SO2尾气和氨水、石灰石、焦炭、碳酸氢铵为原料可以合成硫化钙、硫酸铵、亚硫酸铵等物质,生产流程如下:
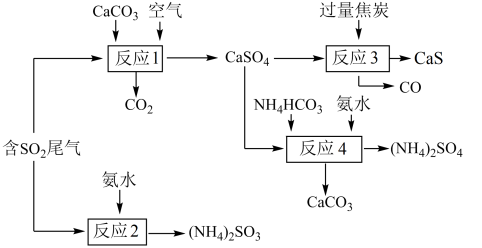
(1)反应1的化学方程式为________________ ;
(2)反应2中用足量氨水吸收SO2,该反应的离子方程式为___________________ ;
(3)为充分利用副产品CO,有人提出以熔融K2CO3为电解质,设计成CO燃料电池以减少对环境的污染。该燃料电池负极的电极反应式为______________ ;
(4)整个合成路线中可以循环利用的物质是_____________ ;
(5)(NH4)2SO3溶液可用于电厂产生的烟道气的脱氮,将氮氧化物转化为氮气,同时生成一种氮肥, 形成共生系统。计算10.00L 2.00mol/L的(NH4)2SO3溶液可以处理标准状况下NO气体的体积(写出计算过程)_______________ 。

(1)反应1的化学方程式为
(2)反应2中用足量氨水吸收SO2,该反应的离子方程式为
(3)为充分利用副产品CO,有人提出以熔融K2CO3为电解质,设计成CO燃料电池以减少对环境的污染。该燃料电池负极的电极反应式为
(4)整个合成路线中可以循环利用的物质是
(5)(NH4)2SO3溶液可用于电厂产生的烟道气的脱氮,将氮氧化物转化为氮气,同时生成一种氮肥, 形成共生系统。计算10.00L 2.00mol/L的(NH4)2SO3溶液可以处理标准状况下NO气体的体积(写出计算过程)
您最近半年使用:0次
2 . I.硫元素是动植物生长不可缺少的元素,硫酸是用途广泛的化工原料,可作脱水剂、吸水剂、氧化剂和催化剂等。
(1)Na2SO3溶液易变质,实验室检验Na2SO3溶液是否变质的试剂是_______ 。
(2)甲、乙两位同学用铜和硫酸做原料,设计了两种制取硫酸铜的方案。
方案甲:铜与浓硫酸加热直接反应,即Cu→CuSO4,方案乙:由Cu→CuO→CuSO4
①方案甲中,铜和浓硫酸反应的化学方程式是_______ 。
②这两种方案,你认为哪一种方案更合理?_______ 。理由是_______ 。
II.氨和硝酸是重要的工业产品,如图是工业合成氨及制备硝酸的流程示意图:
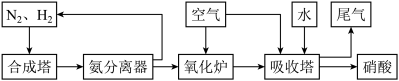
(3)合成塔中发生反应的化学方程式为_______ 。
(4)氨分离器中压强约为15MPa,温度约为-20℃,分离氨应用了氨的_______ 性质。
(5)氧化炉中,NH3转化为NO的化学方程式为_______ 。
(1)Na2SO3溶液易变质,实验室检验Na2SO3溶液是否变质的试剂是
(2)甲、乙两位同学用铜和硫酸做原料,设计了两种制取硫酸铜的方案。
方案甲:铜与浓硫酸加热直接反应,即Cu→CuSO4,方案乙:由Cu→CuO→CuSO4
①方案甲中,铜和浓硫酸反应的化学方程式是
②这两种方案,你认为哪一种方案更合理?
II.氨和硝酸是重要的工业产品,如图是工业合成氨及制备硝酸的流程示意图:

(3)合成塔中发生反应的化学方程式为
(4)氨分离器中压强约为15MPa,温度约为-20℃,分离氨应用了氨的
(5)氧化炉中,NH3转化为NO的化学方程式为
您最近半年使用:0次



