名校
解题方法
1 . 钠是活泼金属,受热后与氧气剧烈反应,发出黄色火焰,生成一种淡黄色固体——过氧化钠,由于空气中还有其它成分,因此可能还有一些同时发生的其它反应”。某校化学兴趣小组同学据此进行了有关探究。
【猜想】钠在空气中燃烧,生成过氧化钠、氧化钠,还有氮化钠。
【查阅资料】氮化钠与水反应能生成氢氧化钠和氨气。
【实验】①取11.5g钠单质放在一块薄铁皮上,上扣一玻璃罩(玻璃罩内为干燥且无酸性气体的空气),用酒精灯加热薄铁皮,钠燃烧;
②将燃烧产物投入水中,得到0.224L(折算成标准状态)气体和1000mL溶液;
③经检验,该气体为纯净的氧气;
④从1000mL溶液中取出25.00mL溶液,加入1.00mol·L-1HCl溶液至13.50mL时恰好完全反应。
【结论】
(1)通过计算确定钠的燃烧产物中是否含有氮化钠___________ 。
(2)计算钠在空气中燃烧产物中各成分的物质的量之比___________ 。
【猜想】钠在空气中燃烧,生成过氧化钠、氧化钠,还有氮化钠。
【查阅资料】氮化钠与水反应能生成氢氧化钠和氨气。
【实验】①取11.5g钠单质放在一块薄铁皮上,上扣一玻璃罩(玻璃罩内为干燥且无酸性气体的空气),用酒精灯加热薄铁皮,钠燃烧;
②将燃烧产物投入水中,得到0.224L(折算成标准状态)气体和1000mL溶液;
③经检验,该气体为纯净的氧气;
④从1000mL溶液中取出25.00mL溶液,加入1.00mol·L-1HCl溶液至13.50mL时恰好完全反应。
【结论】
(1)通过计算确定钠的燃烧产物中是否含有氮化钠
(2)计算钠在空气中燃烧产物中各成分的物质的量之比
您最近一年使用:0次
2022-09-22更新
|
467次组卷
|
2卷引用:浙江省温州市苍南县2022年第十六届“求知杯”高一化学竞赛试题
解题方法
2 . 铝镁合金有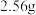 溶于
溶于 生成
生成 的氢气(标准状况下),请问,生成了
的氢气(标准状况下),请问,生成了_____ 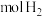 ,铝有
,铝有_______ g,镁有_______ g。
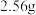 溶于
溶于 生成
生成 的氢气(标准状况下),请问,生成了
的氢气(标准状况下),请问,生成了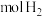 ,铝有
,铝有
您最近一年使用:0次
3 . 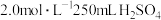 溶液中,溶质的质量是
溶液中,溶质的质量是_______ g,该溶质中含有_______ 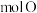 原子。
原子。
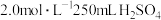 溶液中,溶质的质量是
溶液中,溶质的质量是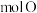 原子。
原子。
您最近一年使用:0次
4 . X是金属M的碱式碳酸盐,不含结晶水。称取质量相等的样品两份,分别进行处理:一份在H2中充分处理(反应1),收集得0.994g水,剩余残渣为金属M的单质,重2.356g;另一份则在CO中处理(反应2),完全反应后得到1.245LCO2(101.325kPa,0°C),剩余残渣和反应1完全相同。
(1)通过计算,推出X的化学式______ 。
(2)写出X分别和H2、CO反应的方程式______ (要求系数为最简整数比)
(1)通过计算,推出X的化学式
(2)写出X分别和H2、CO反应的方程式
您最近一年使用:0次
5 . 目前家用小型制氧机大多以变压吸附方式工作,其原理是以空气为原料,在加压时吸附剂将空气中大部分氮气吸附,氧气和未被吸附的少量氮气被收集起来,得到富氧空气。被吸附的氮气在减压条件下通过尾气管排至大气。某小型家用常压制氧机的标称参数为额定功率100W,输出富氧空气中氧气浓度91%(体积分数),输出富氧空气流量为1.8L·min-1,工作温度为25%℃。以空气进气量10mol为对象,计算达到分离效果所需要的最小能量以及该家用制氧机的能量效率_______ 、______ 。空气由体积分数为20%的氧气和80%的氮气组成,排出的尾气中只有氮气。所有气体均视作理想气体。
您最近一年使用:0次
6 . 回答下列问题:
(1)标准状况下,0.85 g NH3的体积为__________ L。
(2)Fe2(SO4)3溶液中SO 的浓度为0.3 mol∙L−1,c[Fe2(SO4)3]=
的浓度为0.3 mol∙L−1,c[Fe2(SO4)3]=__________ mol∙L−1。
(3)同温同压下,气体N2和O2的密度之比为__________ 。
(4)同温同压下,等体积的气体SO2和CO的物质的量之比为__________ 。
(5)标准状况下,0.66 g某气态氧化物RO2的体积为336 mL,则元素R的相对原子质量为__________ 。
(6)将7.8 g Na2O2溶于93.8 g水中充分反应后(此时溶液密度近似为1.0 g·cm−3),c(NaOH)=__________ mol∙L−1。
(1)标准状况下,0.85 g NH3的体积为
(2)Fe2(SO4)3溶液中SO
 的浓度为0.3 mol∙L−1,c[Fe2(SO4)3]=
的浓度为0.3 mol∙L−1,c[Fe2(SO4)3]=(3)同温同压下,气体N2和O2的密度之比为
(4)同温同压下,等体积的气体SO2和CO的物质的量之比为
(5)标准状况下,0.66 g某气态氧化物RO2的体积为336 mL,则元素R的相对原子质量为
(6)将7.8 g Na2O2溶于93.8 g水中充分反应后(此时溶液密度近似为1.0 g·cm−3),c(NaOH)=
您最近一年使用:0次
2020-12-15更新
|
133次组卷
|
2卷引用:广东省海珠区2022-2023学年高一上学期1月化学竞赛试题
解题方法
7 . 某多元化合物(含结晶水)是液流电池中解决阳极电解质和阴极电解质被污染的有用材料。该化合物中一些元素的质量百分数为:金属(M):21.67%,硫(S):13.64%,氧(O):61.26%。该化合物在水溶液中与氯化钡的盐酸溶液反应,产生白色沉淀。试推算出该化合物的化学式_______ 。
您最近一年使用:0次
8 . 根据下列实验数据,写出CuSO4(s) 转化为CuSO4·5H2O(s)的热化学方程式________ (给出具体计算过程,保留整数)。
I.称取3.2 gCuSO4 (160g·mol-1) 置于盛有H2O的烧杯(33.5g) 中搅拌溶解,得到50 mL CuSO4溶液,溶液温度升高5.5 °C。
II.称取5.0 g CuSO4·5H2O (250 g·mol-1)置于盛有H2O的烧杯(33.5g)中搅拌溶解,得到50 mL CuSO4溶液,溶液温度降低1.0 °C。已知: 烧杯、CuSO4溶液的比热容分别为0.84J·g-1·K-1、4.2 J-1·mL-1·K-1。
I.称取3.2 gCuSO4 (160g·mol-1) 置于盛有H2O的烧杯(33.5g) 中搅拌溶解,得到50 mL CuSO4溶液,溶液温度升高5.5 °C。
II.称取5.0 g CuSO4·5H2O (250 g·mol-1)置于盛有H2O的烧杯(33.5g)中搅拌溶解,得到50 mL CuSO4溶液,溶液温度降低1.0 °C。已知: 烧杯、CuSO4溶液的比热容分别为0.84J·g-1·K-1、4.2 J-1·mL-1·K-1。
您最近一年使用:0次
9 . 硫粉和S2-反应可以生成多硫离子S ,如:S+S2-→S
,如:S+S2-→S 、2S+S2-→S
、2S+S2-→S 。 在10 mL S2-溶液中加入0.080 g硫粉,控制条件使硫粉完全反应,检测到溶液中最大聚合度的多硫离子是S32-,且离子浓度之比符合等比数列1,10,……10n-1。,若不考虑其他副反应,计算反应后溶液中S2-的浓度c1=
。 在10 mL S2-溶液中加入0.080 g硫粉,控制条件使硫粉完全反应,检测到溶液中最大聚合度的多硫离子是S32-,且离子浓度之比符合等比数列1,10,……10n-1。,若不考虑其他副反应,计算反应后溶液中S2-的浓度c1=_______ ,其起始浓度c0=_______ 。
 ,如:S+S2-→S
,如:S+S2-→S 、2S+S2-→S
、2S+S2-→S 。 在10 mL S2-溶液中加入0.080 g硫粉,控制条件使硫粉完全反应,检测到溶液中最大聚合度的多硫离子是S32-,且离子浓度之比符合等比数列1,10,……10n-1。,若不考虑其他副反应,计算反应后溶液中S2-的浓度c1=
。 在10 mL S2-溶液中加入0.080 g硫粉,控制条件使硫粉完全反应,检测到溶液中最大聚合度的多硫离子是S32-,且离子浓度之比符合等比数列1,10,……10n-1。,若不考虑其他副反应,计算反应后溶液中S2-的浓度c1=
您最近一年使用:0次
2021-07-15更新
|
100次组卷
|
3卷引用:第32届中国化学奥林匹克竞赛(江苏赛区)初赛试题
第32届中国化学奥林匹克竞赛(江苏赛区)初赛试题浙江省丽水市缙云中学等三校2021-2022学年高三12月份联考化学试题(已下线)解密02 物质的量(分层训练)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)
10 . 现有一定量的Cu和CuO混合物,向其中加入0.6L 2.0mol/L稀硝酸,混合物完全溶解,同时生成4. 48L NO(标准状况)。向所得溶液中加入一定体积1. 0mol/LNaOH溶液,恰好使Cu2+沉淀完全,沉淀经洗涤、充分灼烧后得32. 0g固体。试计算:
(1)原混合物中CuO的质量_______ ;
(2)加入NaOH溶液的体积_______ 。
(1)原混合物中CuO的质量
(2)加入NaOH溶液的体积
您最近一年使用:0次



