名校
1 . 设 表示阿伏加德罗常数的值。下列说法正确的是
表示阿伏加德罗常数的值。下列说法正确的是
 表示阿伏加德罗常数的值。下列说法正确的是
表示阿伏加德罗常数的值。下列说法正确的是A.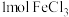 溶于水形成的胶体中含有 溶于水形成的胶体中含有 个 个 胶体粒子 胶体粒子 |
B.常温下,4g氢气所含的原子数目为 |
C.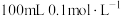 的 的 溶液中含有H原子数大于 溶液中含有H原子数大于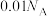 |
D.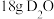 和 和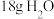 中含有的质子数均为 中含有的质子数均为 |
您最近一年使用:0次
2024-02-03更新
|
121次组卷
|
2卷引用:吉林省长春吉大附中实验学校2023-2024学年高一上学期1月期末化学试题
名校
解题方法
2 . 下列实验操作能达到目的的是
| 目 的 | 操 作 | |
| A | 制备Fe(OH)3胶体 | 向沸腾的蒸馏水中滴加饱和FeCl3溶液,继续煮沸至溶液呈红褐色,停止加热 |
| B | 配制浓度为0.010 mol/L的KMnO4溶液 | 称取KMnO4固体0.158 g,放入100 mL容量瓶中,加水溶解并稀释至刻度 |
| C | 检验溶液中是否有K+ | 取干净铂丝,酒精灯灼烧,观察火焰颜色是否为紫色 |
| D | 检验某溶液中是否存在Cl- | 取适量溶液,加入AgNO3溶液,观察白色沉淀 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
3 . 下列关于分散系的说法正确的是
| A.根据体系的稳定性可将分散系分为溶液、胶体和浊液 |
| B.将氯化铁饱和溶液加热煮沸可制得氢氧化铁胶体 |
| C.丁达尔效应是胶体和溶液的本质区别 |
| D.用渗析的方法可将胶体和溶液分离 |
您最近一年使用:0次
2023-11-08更新
|
0次组卷
|
3卷引用:吉林省实验中学2023-2024学年高一上学期期中考试化学试题
解题方法
4 . 分类是认识和研究物质及其变化的一种常用的科学方法。
(1)下列物质:①纯 ;②硝酸钾溶液;③铜;④二氧化碳;⑤
;②硝酸钾溶液;③铜;④二氧化碳;⑤ 固体;⑥
固体;⑥ 固体;⑦蔗糖;⑧熔融KCl;⑨氨水。其中能导电的是
固体;⑦蔗糖;⑧熔融KCl;⑨氨水。其中能导电的是___________ (填序号,下同),属于电解质的是___________ 。
(2) 胶体呈红褐色,具有良好的净水效果,写出饱和
胶体呈红褐色,具有良好的净水效果,写出饱和 溶液制备
溶液制备 胶体的化学方程式
胶体的化学方程式___________ 。
(3)硫酸酸化条件下,高锰酸钾可与草酸( )溶液发生反应,写出其化学方程式,并用单线桥法标出电子转移的方向和数目:
)溶液发生反应,写出其化学方程式,并用单线桥法标出电子转移的方向和数目:___________ 。
(4)在同温、同压下,实验测得CO、 和
和 三种气体的混合气体的密度是
三种气体的混合气体的密度是 的14.5倍,则混合气体中氧气的体积分数为
的14.5倍,则混合气体中氧气的体积分数为___________ 。
(5)如果ag某气体中含有的分子数为b,则cg该气体在标准状况下的体积是(式中 为阿伏加德罗常数的值)___________(填序号)。
为阿伏加德罗常数的值)___________(填序号)。
(1)下列物质:①纯
 ;②硝酸钾溶液;③铜;④二氧化碳;⑤
;②硝酸钾溶液;③铜;④二氧化碳;⑤ 固体;⑥
固体;⑥ 固体;⑦蔗糖;⑧熔融KCl;⑨氨水。其中能导电的是
固体;⑦蔗糖;⑧熔融KCl;⑨氨水。其中能导电的是(2)
 胶体呈红褐色,具有良好的净水效果,写出饱和
胶体呈红褐色,具有良好的净水效果,写出饱和 溶液制备
溶液制备 胶体的化学方程式
胶体的化学方程式(3)硫酸酸化条件下,高锰酸钾可与草酸(
 )溶液发生反应,写出其化学方程式,并用单线桥法标出电子转移的方向和数目:
)溶液发生反应,写出其化学方程式,并用单线桥法标出电子转移的方向和数目:(4)在同温、同压下,实验测得CO、
 和
和 三种气体的混合气体的密度是
三种气体的混合气体的密度是 的14.5倍,则混合气体中氧气的体积分数为
的14.5倍,则混合气体中氧气的体积分数为(5)如果ag某气体中含有的分子数为b,则cg该气体在标准状况下的体积是(式中
 为阿伏加德罗常数的值)___________(填序号)。
为阿伏加德罗常数的值)___________(填序号)。A.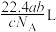 | B.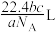 | C.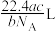 | D.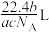 |
您最近一年使用:0次
解题方法
5 . 设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A.标准状况下, 所含的电子总数为 所含的电子总数为 |
B.含 的饱和溶液滴入沸腾的蒸馏水中,制得的氢氧化铁胶体粒子数为 的饱和溶液滴入沸腾的蒸馏水中,制得的氢氧化铁胶体粒子数为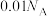 |
C.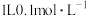 稀硝酸中,所含的氧原子总数为 稀硝酸中,所含的氧原子总数为 |
D. 和 和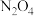 混合气体中含有原子总数为 混合气体中含有原子总数为 |
您最近一年使用:0次
名校
解题方法
6 . 实验证明,胶体的凝聚能力主要取决于与胶粒带相反电荷的离子所带的电荷数,电荷数越大,凝聚能力越大。
(1)已知Fe(OH)3胶体粒子带正电,则 向Fe(OH)3胶体中加入下列电解质时,其凝聚能力最强的为_______
①NaCl ②FeCl3 ③K2SO4 ④Na3PO4
(2)为了把黏土溶胶(黏土胶体粒子带负电荷)变成较洁净的水,加入下列电解质时,_______(填字母)效果最明显。
(3)将少量FeCl3饱和溶液分别滴加到下列物质中,得到三种分散系,完成相关问题:
甲:将FeCl3饱和溶液滴加到冷水中;
乙:将FeCl3饱和溶液滴加到NaOH溶液中;
丙:将FeCl3饱和溶液滴加到沸水中,继续加热煮沸得到红褐色透明液体。
①丙中反应的化学方程式为_______ 。
②向经过检验后的丙中逐滴加入稀盐酸,出现的现象为_______
③向丙中插入电极后通电,Fe(OH)3胶粒移向_______ (填“与电源负极相连”或“与电源正极相连”)的一极。
④可用如图所示的装置除去Fe(OH)3胶体中的杂质离子来提纯Fe(OH)3胶体,实验过程中需不断更换烧杯中的蒸馏水。该方法名称为_______ 。

(1)已知Fe(OH)3胶体粒子带正电,则 向Fe(OH)3胶体中加入下列电解质时,其凝聚能力最强的为
①NaCl ②FeCl3 ③K2SO4 ④Na3PO4
(2)为了把黏土溶胶(黏土胶体粒子带负电荷)变成较洁净的水,加入下列电解质时,_______(填字母)效果最明显。
| A.BaCl2 | B.Al2(SO4)3 | C.KCl | D.CuSO4 |
甲:将FeCl3饱和溶液滴加到冷水中;
乙:将FeCl3饱和溶液滴加到NaOH溶液中;
丙:将FeCl3饱和溶液滴加到沸水中,继续加热煮沸得到红褐色透明液体。
①丙中反应的化学方程式为
②向经过检验后的丙中逐滴加入稀盐酸,出现的现象为
③向丙中插入电极后通电,Fe(OH)3胶粒移向
④可用如图所示的装置除去Fe(OH)3胶体中的杂质离子来提纯Fe(OH)3胶体,实验过程中需不断更换烧杯中的蒸馏水。该方法名称为

您最近一年使用:0次
名校
解题方法
7 . 下列说法正确的是
| A.纳米铜颗粒(粒子直径为50~100nm)是一种胶体 |
B.向NaOH溶液中滴加饱和 溶液可制取 溶液可制取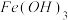 胶体 胶体 |
| C.直径在80nm左右的新冠病毒颗粒是由蛋白质构成的,在空气中不能形成气溶胶 |
D.将含100个 “分子”的饱和溶液逐滴滴入到沸水中充分反应,得到的 “分子”的饱和溶液逐滴滴入到沸水中充分反应,得到的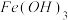 胶体微粒一定小于100个 胶体微粒一定小于100个 |
您最近一年使用:0次
名校
8 . 回答下列问题。
(1)现有下列10种物质:①纯碱;②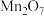 ;③硫酸;④CaO;⑤
;③硫酸;④CaO;⑤ ;⑥硫酸氢钠;⑦
;⑥硫酸氢钠;⑦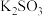 ;⑧
;⑧ ;⑨
;⑨ ;⑩CO。其中属于正盐的是
;⑩CO。其中属于正盐的是_______ ;属于酸性氧化物的是_______ 。
(2)实验室制备 胶体的化学方程式为
胶体的化学方程式为_______ ,取少量 胶体于试管中,逐滴加入硫酸至过量,可看到的现象是
胶体于试管中,逐滴加入硫酸至过量,可看到的现象是_______ 。将橘红色的硫化锑( )胶体,装入U形管,插入电极后通直流电,发现阳极附近橘红色加深,证明
)胶体,装入U形管,插入电极后通直流电,发现阳极附近橘红色加深,证明 胶粒带
胶粒带_______ (填“正”或“负”)电荷。
(1)现有下列10种物质:①纯碱;②
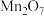 ;③硫酸;④CaO;⑤
;③硫酸;④CaO;⑤ ;⑥硫酸氢钠;⑦
;⑥硫酸氢钠;⑦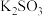 ;⑧
;⑧ ;⑨
;⑨ ;⑩CO。其中属于正盐的是
;⑩CO。其中属于正盐的是(2)实验室制备
 胶体的化学方程式为
胶体的化学方程式为 胶体于试管中,逐滴加入硫酸至过量,可看到的现象是
胶体于试管中,逐滴加入硫酸至过量,可看到的现象是 )胶体,装入U形管,插入电极后通直流电,发现阳极附近橘红色加深,证明
)胶体,装入U形管,插入电极后通直流电,发现阳极附近橘红色加深,证明 胶粒带
胶粒带
您最近一年使用:0次
9 . FeCl3溶液、Fe(OH)3胶体以及Fe(OH)3悬浊液是三种重要的分散系,下列说法正确的是
| A.Fe(OH)3胶体不同于另外两种分散系的本质特征是它具有丁达尔效应 |
| B.向FeCl3溶液中加入NaOH溶液可制得Fe(OH)3胶体 |
| C.可用丁达尔效应区分FeCl3溶液和Fe(OH)3胶体 |
| D.三种分散系的颜色相同,且都能与盐酸反应 |
您最近一年使用:0次
10 . 实验证明,胶体的凝聚能力主要取决于与胶粒带相反电荷的离子所带的电荷数,电荷数越大,凝聚能力越大。
(1)向Fe(OH)3胶体中加入下列电解质时,其凝聚能力最强的为___________ 。[已知:Fe(OH)3胶体粒子带正电荷]
①NaCl ②FeCl3 ③K2SO4 ④Na3PO4
(2)为了把黏土溶胶(黏土胶体粒子带负电荷)变成较洁净的水,加入下列电解质时,___________(填字母)效果最明显。
(3)将少量FeCl3饱和溶液分别滴加到下列物质中,得到三种分散系,完成相关问题:
甲:将FeCl3饱和溶液滴加到冷水中;
乙:将FeCl3饱和溶液滴加到NaOH溶液中;
丙:将FeCl3饱和溶液滴加到沸水中,继续加热煮沸得到红褐色透明液体。
①丙中反应的化学方程式为___________ 。
②用最简单的方法判断丙中是否成功制备胶体,写出相关的操作、现象和结论___________ ,能产生该现象的原因是胶体粒子对光波的___________ 所致。
③可用如图所示的装置除去Fe(OH)3胶体中的杂质离子来提纯Fe(OH)3胶体,实验过程中需不断更换烧杯中的蒸馏水。该方法名称为___________ 。
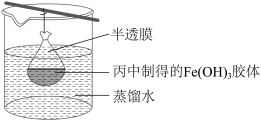
(1)向Fe(OH)3胶体中加入下列电解质时,其凝聚能力最强的为
①NaCl ②FeCl3 ③K2SO4 ④Na3PO4
(2)为了把黏土溶胶(黏土胶体粒子带负电荷)变成较洁净的水,加入下列电解质时,___________(填字母)效果最明显。
| A.BaCl2 | B.Al2(SO4)3 | C.KCl | D.CuSO4 |
甲:将FeCl3饱和溶液滴加到冷水中;
乙:将FeCl3饱和溶液滴加到NaOH溶液中;
丙:将FeCl3饱和溶液滴加到沸水中,继续加热煮沸得到红褐色透明液体。
①丙中反应的化学方程式为
②用最简单的方法判断丙中是否成功制备胶体,写出相关的操作、现象和结论
③可用如图所示的装置除去Fe(OH)3胶体中的杂质离子来提纯Fe(OH)3胶体,实验过程中需不断更换烧杯中的蒸馏水。该方法名称为

您最近一年使用:0次



