1 . 完成下列问题
(1)下列化学用语只能用来表示一种微粒的是______
(2)下列叙述中所描述的物质一定是金属元素的是______
(3)下列说法正确的是______
(4)X、Y、Z、W是原子序数依次增大的短周期元素。W与X位于同一主族;X、Y、Z三种元素形成的化合物具有强氧化性,其结构如下图所示;。
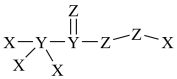
下列叙述错误的是______
(5)锶(Sr)位于元素周期表的第5周期ⅡA族。碳酸锶(SrCO3)是制取锶的原料,用天青石固体(主要成分SrSO4,难溶于水)和Na2CO3溶液混合浸泡可制取碳酸锶。完成下列填空:
①在上述反应体系中出现的几种短周期元素中,原子半径最大的是___________ (填元素符号,下同)。非金属性最强的是___________ 。写出与锶同族第3周期元素原子的结构示意图___________ 。
②反应体系中出现的非金属元素可形成二硫化碳(CS2),其分子构型是直线型分子,写出该分子的电子式___________ 。
③已知:锶的原子序数为38,某锶原子的质量数为88,写出能包含这些信息的一种化学符号___________ 。下列关于锶及其化合物的叙述中,错误的是___________ 。
a.锶的金属性比镁强 b.氢氢化锶呈两性
c.锶在化合物中呈+2价 d.锶在自然界中以游离态存在
(1)下列化学用语只能用来表示一种微粒的是______
| A.S | B.C2H6O | C.12C | D.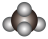 |
(2)下列叙述中所描述的物质一定是金属元素的是______
| A.易失去电子的物质 | B.第三周期中,原子的最外电子层只有2个电子的元素 |
| C.单质具有金属光泽的元素 | D.原子的最外电子层只有1个电子的元素 |
(3)下列说法正确的是______
| A.H2O、H2S、H2Se的分子间作用力依次增大 |
| B.Na2O2、MgCl2、NaOH、NH4Cl均为含共价键的离子化合物 |
| C.化学键通常指的是相邻的原子或离子之间的强烈的相互作用 |
| D.NaHSO4加热熔化时破坏了该物质中的离子键和共价键 |
(4)X、Y、Z、W是原子序数依次增大的短周期元素。W与X位于同一主族;X、Y、Z三种元素形成的化合物具有强氧化性,其结构如下图所示;。
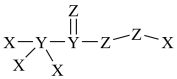
下列叙述错误的是______
| A.该化合物中各元素原子均达稳定结构 |
| B.Z的氢化物的沸点可能高于Y的氢化物 |
| C.Z、W形成的简单离子半径,Z大于W |
| D.由X、Y、Z、W四种元素形成的化合物一定能与X、Z、W形成的化合物反应 |
(5)锶(Sr)位于元素周期表的第5周期ⅡA族。碳酸锶(SrCO3)是制取锶的原料,用天青石固体(主要成分SrSO4,难溶于水)和Na2CO3溶液混合浸泡可制取碳酸锶。完成下列填空:
①在上述反应体系中出现的几种短周期元素中,原子半径最大的是
②反应体系中出现的非金属元素可形成二硫化碳(CS2),其分子构型是直线型分子,写出该分子的电子式
③已知:锶的原子序数为38,某锶原子的质量数为88,写出能包含这些信息的一种化学符号
a.锶的金属性比镁强 b.氢氢化锶呈两性
c.锶在化合物中呈+2价 d.锶在自然界中以游离态存在
您最近一年使用:0次
2 . 二氧化碳是造成大气污染的主要有害气体之一,二氧化硫尾气处理的方法之一是采用钠—钙联合处理法。
第一步:用NaOH溶液吸收SO2。2NaOH+SO2→Na2SO3+H2O
第二步:将所得的Na2SO3溶液与生石灰反应。Na2SO3+CaO+H2O→CaSO3↓+2NaOH
完成下列填空:
(1)在上述两步反应所涉及的短周期元素中,原子半径由小到大的顺序是__________ 。
(2)氧和硫属于同族元素,该族元素的原子最外层电子排布可表示为__________ 。写出一个能比较氧元素和硫元素非金属性强弱的化学反应方程式:_______________
(3)NaOH的电子式为_____________ 。
(4)若在第一步吸收SO2后得到的NaOH和Na2SO3混合溶液中,加入少许溴水,振荡后溶液变为无色,生成Na2SO4和NaBr。写出发生反应的化学方程式。_____________
(5)钠—钙联合处理法的优点有__________ 、____________ 。(任写两点)
第一步:用NaOH溶液吸收SO2。2NaOH+SO2→Na2SO3+H2O
第二步:将所得的Na2SO3溶液与生石灰反应。Na2SO3+CaO+H2O→CaSO3↓+2NaOH
完成下列填空:
(1)在上述两步反应所涉及的短周期元素中,原子半径由小到大的顺序是
(2)氧和硫属于同族元素,该族元素的原子最外层电子排布可表示为
(3)NaOH的电子式为
(4)若在第一步吸收SO2后得到的NaOH和Na2SO3混合溶液中,加入少许溴水,振荡后溶液变为无色,生成Na2SO4和NaBr。写出发生反应的化学方程式。
(5)钠—钙联合处理法的优点有
您最近一年使用:0次
2020-03-11更新
|
159次组卷
|
2卷引用:上海大学附属中学2018-2019学年高三下学期第一次月考化学试题



