解题方法
1 . 设 是阿伏加德罗常数的值,下列说法错误的是
是阿伏加德罗常数的值,下列说法错误的是
 是阿伏加德罗常数的值,下列说法错误的是
是阿伏加德罗常数的值,下列说法错误的是A.标准状况下,33.6 L HF中含有氟原子的数目为1.5 |
B.1 L   溶液中 溶液中 的数目小于0.1 的数目小于0.1 |
C.0.1 mol乙烯和乙醇的混合物完全燃烧消耗 的数目为0.3 的数目为0.3 |
D.电解精炼铜,当电路中通过 个电子时,阳极质量减少32 g 个电子时,阳极质量减少32 g |
您最近一年使用:0次
2 . 设 阿伏加德罗常数的值,下列说法不正确的是
阿伏加德罗常数的值,下列说法不正确的是
 阿伏加德罗常数的值,下列说法不正确的是
阿伏加德罗常数的值,下列说法不正确的是A.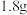 的 的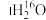 含有的中子数均为 含有的中子数均为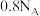 |
B.1 该物质 该物质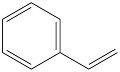 含有4 含有4 π键 π键 |
C.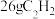 与 与 混合气体中含 混合气体中含 键的数目为 键的数目为 |
D.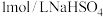 中含有的阳离子数为2 中含有的阳离子数为2 |
您最近一年使用:0次
3 . 设阿伏加 德罗常数的值为N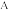 ,关于反应
,关于反应 下列说法错误的是
下列说法错误的是
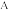 ,关于反应
,关于反应 下列说法错误的是
下列说法错误的是| A.8.8gCO2中共用电子对的数目为0.8NA |
| B.消耗CO24.48L(标准状况下)时转移电子的数目为0.8NA |
| C.12g金刚石(C)中所含共价键的数目为4NA |
| D.0.1molMgO中所有离子的最外层电子数之和为1.6NA |
您最近一年使用:0次
4 . NA表示阿伏加德罗常数的值。下列说法中正确的是
①常温下,0.1molCl2与足量NaOH溶液反应,转移的电子数目为0.2NA
②常温常压下,18gH2O中含有的电子总数为10NA
③将100 mL 0.1 mol·L-1FeCl3溶液滴入沸水中可制得Fe(OH)3胶粒0.01NA
④在反应KIO3+6HI==KI+3I2+3H2O中,每生成3 mol I2转移的电子数为5NA
⑤常温常压下,14g的C2H4和C4H8混合气体中含有的原子数为3NA
⑥在标准状况下,0.5molNO与0.5molO2混合后气体分子数为0.75 NA
⑦1.0L 1.0 mol·L-1 Na2SiO3水溶液中含有的氧原子数为3NA
①常温下,0.1molCl2与足量NaOH溶液反应,转移的电子数目为0.2NA
②常温常压下,18gH2O中含有的电子总数为10NA
③将100 mL 0.1 mol·L-1FeCl3溶液滴入沸水中可制得Fe(OH)3胶粒0.01NA
④在反应KIO3+6HI==KI+3I2+3H2O中,每生成3 mol I2转移的电子数为5NA
⑤常温常压下,14g的C2H4和C4H8混合气体中含有的原子数为3NA
⑥在标准状况下,0.5molNO与0.5molO2混合后气体分子数为0.75 NA
⑦1.0L 1.0 mol·L-1 Na2SiO3水溶液中含有的氧原子数为3NA
| A.①⑤⑦ | B.③④⑥ |
| C.②④⑤ | D.②③⑦ |
您最近一年使用:0次
2016-11-09更新
|
289次组卷
|
3卷引用:2017届山东省济南一中高三上学期期中化学试卷



