解题方法
1 . 某同学为了探究硫与氧气的反应情况,装配好如图所示的装置,待内外空气压强不变时标注出水银液面的刻度(用红漆)。取下橡胶塞,在玻璃燃烧匙中加入硫粉,用酒精灯点燃迅速移入锥形瓶中并塞紧橡胶塞。硫粉安静地燃烧,水银柱推向左管。当火焰熄灭后,静置,水银柱又慢慢地回到原先标定的刻度。简要回答下列问题:
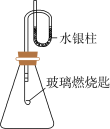
(1)水银柱推向左管是否一定说明生成气体的量一定大于反应气体的量,说明原因:_______ 。
(2)硫粉未燃尽时火焰就熄灭了,说明_______ 。
(3)根据水银柱最后又回到原先标定的刻度,可得到什么结论?_______ 。
(4)根据反应方程式S+O2 SO2和上述结论又可推导(证明)出什么?
SO2和上述结论又可推导(证明)出什么?_______ 。

(1)水银柱推向左管是否一定说明生成气体的量一定大于反应气体的量,说明原因:
(2)硫粉未燃尽时火焰就熄灭了,说明
(3)根据水银柱最后又回到原先标定的刻度,可得到什么结论?
(4)根据反应方程式S+O2
 SO2和上述结论又可推导(证明)出什么?
SO2和上述结论又可推导(证明)出什么?
您最近一年使用:0次
名校
2 . 二氧化碳捕获技术用于去除气流中的二氧化碳或者分离出二氧化碳作为气体产物,其中CO2催化合成甲酸是原子利用率高的反应,且生成的甲酸是重要化工原料。下列说法不正确的是
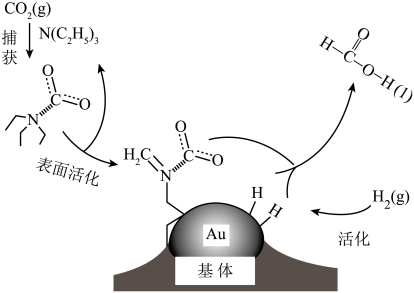
| A.每反应22.4 L CO2,转移电子数为2 NA |
| B.在捕获过程,二氧化碳分子中的共价键未完全断裂 |
| C.N(C2H5)3能够协助二氧化碳到达催化剂表面 |
| D.该方法制备甲酸符合“碳中和”思想,并且原子利用率可达100% |
您最近一年使用:0次
解题方法
3 . 一种光催化重整聚乳酸生成丙酮酸的过程如图所示。设 为阿伏加德罗常数的值,下列说法错误的是
为阿伏加德罗常数的值,下列说法错误的是
 为阿伏加德罗常数的值,下列说法错误的是
为阿伏加德罗常数的值,下列说法错误的是
A.1mol乳酸分子中含有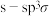 键数目为 键数目为 |
B.1mol乳酸比1mol丙酮酸多 质子 质子 |
C.生成1mol丙酮酸,需要消耗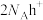 |
D.1mol丙酮酸与足量 溶液反应,生成 溶液反应,生成 分子数为 分子数为 |
您最近一年使用:0次
名校
解题方法
4 . 运载火箭常用偏二甲肼[ ]与
]与 作推进剂,二者反应生成
作推进剂,二者反应生成 、
、 和
和 。设
。设 为阿伏加德罗常数的值,下列有关说法正确的是
为阿伏加德罗常数的值,下列有关说法正确的是
 ]与
]与 作推进剂,二者反应生成
作推进剂,二者反应生成 、
、 和
和 。设
。设 为阿伏加德罗常数的值,下列有关说法正确的是
为阿伏加德罗常数的值,下列有关说法正确的是A.偏二甲肼中N原子的杂化类型均为 |
B.标准状况下,11.2L  中的σ键数目为 中的σ键数目为 |
C.18g  含有的中子数为10 含有的中子数为10 |
D.92g  和 和 混合气体含有的原子数为6 混合气体含有的原子数为6 |
您最近一年使用:0次
解题方法
5 . 用NA表示阿伏加德罗常数,下列说法错误的是
A.将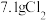 通入足量氢氧化钠溶液中,转移电子数为 通入足量氢氧化钠溶液中,转移电子数为 |
B.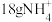 所含的电子数目为 所含的电子数目为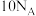 |
C.含0.2mol FeCl3的氯化铁饱和溶液滴入沸水充分反应形成的 胶体粒子数小于0.2NA 胶体粒子数小于0.2NA |
D. 在空气中完全燃烧生成MgO和Mg3N2的混合物,转移的电子数为 在空气中完全燃烧生成MgO和Mg3N2的混合物,转移的电子数为 |
您最近一年使用:0次
名校
6 .  表示阿伏伽德罗常数的值,下列说法
表示阿伏伽德罗常数的值,下列说法错误 的是
 表示阿伏伽德罗常数的值,下列说法
表示阿伏伽德罗常数的值,下列说法A.标准状况下,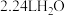 含有的质子数为 含有的质子数为 |
B.常温常压下,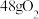 和 和 的混合气体中含有 的混合气体中含有 原子数为 原子数为 |
C.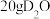 比 比 多 多 个中子 个中子 |
D. 质量分数为46%的乙醇 质量分数为46%的乙醇 水溶液中,含有的O原子数目为 水溶液中,含有的O原子数目为 |
您最近一年使用:0次
7 . 设NA为阿伏加德罗常数的值,下列说法不正确 的是
| A.3.2g 氧气分子含有O原子数为0.2NA |
| B.常温常压下,22.4L CH4气体含有分子数小于NA |
| C.23g Na在空气中燃烧,生成Na2O和Na2O2的混合物,转移的电子数为NA |
| D.0.1 mol·L−1的NaCl溶液中,Na+数目为0.1NA |
您最近一年使用:0次
解题方法
8 . 用NA以表示阿伏加德罗常数的值,下列说法中正确的是
| A.常温常压下,28gN2和CO的混合物中所含有的原子数目为2NA |
| B.在25℃1.01×105Pa的条件下,2.24LH2中含有的分子数等于0.1NA |
| C.0.2mol·L-1的CaCl2,溶液中含有的Cl-的数目为0.4NA |
| D.常温常压下,27gAl与足量的盐酸反应,得到H2的分子数为3NA |
您最近一年使用:0次
9 . 下列说法不正确 的是
A. 的摩尔质量为 的摩尔质量为 |
B.标准状况下,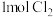 的体积是 的体积是 |
C.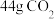 中含有的氧原子数约为 中含有的氧原子数约为 |
D.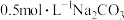 溶液中 溶液中 是 是 |
您最近一年使用:0次
10 . 下列说法不正确 的是
| A.CH4的摩尔质量是16g/mol |
| B.常温常压下,22.4LCO2的物质的量为1mol |
| C.1molN2约含有6.02×1023个氮分子 |
| D.1L1mol/LNaOH溶液中含有1molNa+ |
您最近一年使用:0次



