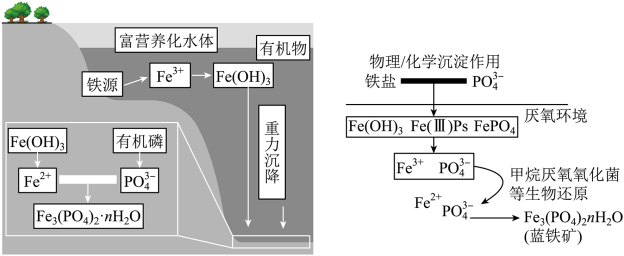
1 . 一方面,磷矿藏在地球上分布不均匀且储量有限;另一方面,污水中含有较多的磷元素。因此在污水处理生物污泥中的蓝铁矿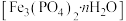 因其潜在的特殊用途以及经济价值而备受关注。蓝铁矿在自然水体中形成的过程如图。
因其潜在的特殊用途以及经济价值而备受关注。蓝铁矿在自然水体中形成的过程如图。
(1)水处理时,加入的高铁酸钾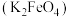 作为净水消毒剂,发生反应的化学方程式为
作为净水消毒剂,发生反应的化学方程式为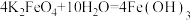 (胶体)
(胶体)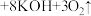 。
。
① 中
中 的化合价为
的化合价为_______ 价,上述反应涉及的物质中属于盐的是_______ 。
②高铁酸钾可用于净水消毒的原因是_______ 。
(2)在甲烷厌氧氧化菌的作用下,氢氧化铁和甲烷发生如下反应,配平该离子方程式:_______ 。

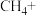

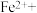
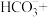

(3)无氧条件下加热,蓝铁矿(无杂质)发生分解: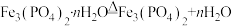 ,蓝铁矿的质量由5.02g减小为3.58g,则n=
,蓝铁矿的质量由5.02g减小为3.58g,则n=_______ ,蓝铁矿的相对分子质量为_______ 。
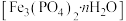 因其潜在的特殊用途以及经济价值而备受关注。蓝铁矿在自然水体中形成的过程如图。
因其潜在的特殊用途以及经济价值而备受关注。蓝铁矿在自然水体中形成的过程如图。
(1)水处理时,加入的高铁酸钾
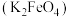 作为净水消毒剂,发生反应的化学方程式为
作为净水消毒剂,发生反应的化学方程式为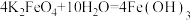 (胶体)
(胶体)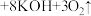 。
。①
 中
中 的化合价为
的化合价为②高铁酸钾可用于净水消毒的原因是
(2)在甲烷厌氧氧化菌的作用下,氢氧化铁和甲烷发生如下反应,配平该离子方程式:

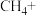

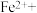
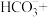

(3)无氧条件下加热,蓝铁矿(无杂质)发生分解:
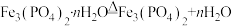 ,蓝铁矿的质量由5.02g减小为3.58g,则n=
,蓝铁矿的质量由5.02g减小为3.58g,则n=
您最近一年使用:0次
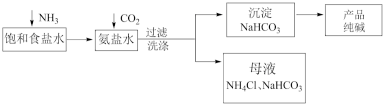
2 . 侯德榜于1940年完成的制碱新工艺开创了世界制碱工业的新纪元,其工艺流程如下。(其中NH4HCO3不稳定,温度高于35℃会分解。)
(1)实验室中可用NH4Cl与Ca(OH)2反应制备NH3,写出化学方程式_____ ;工业合成氨: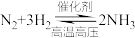 ,若有2 mol N2完全反应,转移电子数目为
,若有2 mol N2完全反应,转移电子数目为_____ (NA为阿伏加德罗常数的数值,用含NA的代数式表示);试从元素化合价的角度分析NH3具有还原性的理由______ 。
(2)写出产生NaHCO3沉淀的化学方程式_______ ,该反应需控制温度在30℃~34℃左右,采用的加热方式为________ ,温度过高不利于生产的原因是_________ 。
(3)氨盐水中通足量二氧化碳后过滤,实现了混合物的分离,是利用物质的_____ (填字母序号)
a.熔沸点差异 b.溶解性差异 c.氧化性还原性差异
(4)母液可用于制备副产品NH4Cl,该副产品的用途是________ 。(任写一种)
(5)经过焙烧后获得粗产品纯碱中混有少量氯化钠,提纯粗产品的方法是_______ 。

(1)实验室中可用NH4Cl与Ca(OH)2反应制备NH3,写出化学方程式
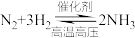 ,若有2 mol N2完全反应,转移电子数目为
,若有2 mol N2完全反应,转移电子数目为(2)写出产生NaHCO3沉淀的化学方程式
(3)氨盐水中通足量二氧化碳后过滤,实现了混合物的分离,是利用物质的
a.熔沸点差异 b.溶解性差异 c.氧化性还原性差异
(4)母液可用于制备副产品NH4Cl,该副产品的用途是
(5)经过焙烧后获得粗产品纯碱中混有少量氯化钠,提纯粗产品的方法是
您最近一年使用:0次
2022-02-08更新
|
274次组卷
|
3卷引用:云南省玉溪市2021-2022学年高二上学期期末教学质量检测化学试题
名校
3 . 铝热反应是铝的一个重要性质,该性质用途十分广泛,不仅被用于焊接钢轨,而且还常被用于冶炼高熔点的金属如钒、铬、锰等。
(1)某校化学兴趣小组同学,取磁性氧化铁按教材中的实验装置(如图甲)进行铝热反应,现象很壮观。指明使用镁条和氯酸钾的目的是______________________ 。
(2)某同学用图乙装置进行铝热反应。取反应后的“铁块”溶于盐酸,向其中滴加KSCN溶液,溶液未见血红色。为测定该实验所得 “铁块”中铁元素含量,设计实验流程如图所示。

几种氢氧化物开始沉淀和完全沉淀的pH如下表所示。
① 试剂A应选择________ ,试剂B应选择_______ 。(填序号)
A.稀盐酸 B.氧化铁 C.H2O2溶液 D.氨水
② 写出反应Ⅱ的离子方程式_____________________ 。
③ 设计简单实验证明M的成分是Fe2O3而非Fe3O4。
④ 上述实验应灼烧至M质量不变,则能证明M质量不变的标志是____________ 。
⑤ 若最终红色粉未M的质量为12.0 g,则该“铁块”的纯度是_______ 。
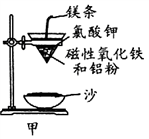

(1)某校化学兴趣小组同学,取磁性氧化铁按教材中的实验装置(如图甲)进行铝热反应,现象很壮观。指明使用镁条和氯酸钾的目的是
(2)某同学用图乙装置进行铝热反应。取反应后的“铁块”溶于盐酸,向其中滴加KSCN溶液,溶液未见血红色。为测定该实验所得 “铁块”中铁元素含量,设计实验流程如图所示。

几种氢氧化物开始沉淀和完全沉淀的pH如下表所示。
| Fe2+ | Fe3+ | Al3+ | Mg2+ | |
| 开始沉淀时的pH | 7.5 | 2.8 | 4.2 | 9.6 |
| 沉淀完全时的pH | 9.0 | 4.0 | 5 | 11 |
A.稀盐酸 B.氧化铁 C.H2O2溶液 D.氨水
② 写出反应Ⅱ的离子方程式
③ 设计简单实验证明M的成分是Fe2O3而非Fe3O4。
| 操作 | 预期现象 |
| 取少量M固体于试管中,向其中加入 | 固体完全溶解,溶液呈黄色。 |
| 继续向上述溶液中滴入 |
④ 上述实验应灼烧至M质量不变,则能证明M质量不变的标志是
⑤ 若最终红色粉未M的质量为12.0 g,则该“铁块”的纯度是
您最近一年使用:0次
2017-03-03更新
|
163次组卷
|
2卷引用:云南省昭通市巧家县第四中学2019-2020学年高一上学期期末考试化学试题



