名校
1 . 设NA为阿伏加德罗常数的值。下列说法正确的是
A.11g 和 和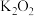 的混合物中含有的离子数目为0.3NA 的混合物中含有的离子数目为0.3NA |
B.标准状况下,4.48L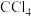 所含的分子数为0.2NA 所含的分子数为0.2NA |
| C.56gFe与足量水蒸气充分反应,转移电子数为3NA |
D. 溶液中含有的氧原子数为0.4NA 溶液中含有的氧原子数为0.4NA |
您最近一年使用:0次
2022-10-18更新
|
820次组卷
|
4卷引用:专题02 阿伏加德罗常数及其化学计算 (练)-2023年高考化学二轮复习讲练测(新高考专用)
(已下线)专题02 阿伏加德罗常数及其化学计算 (练)-2023年高考化学二轮复习讲练测(新高考专用)(已下线)专题03 突破阿伏加德罗常数正误判断(选择题)-2023年高考化学毕业班二轮热点题型归纳与变式演练(全国通用)陕西省咸阳市武功县2023届高三上学期第一次质量检测化学试题吉林省通化市梅河口市第五中学2022-2023学年高三上学期10月期中考试化学试题
22-23高一上·全国·课时练习
解题方法
2 . 有关物质的量浓度的计算
(1)计算的基本公式:c=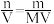 。
。
(2)计算的基本类型和方法:
①已知溶质的质量
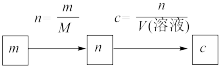
②已知溶液中某种粒子的数目
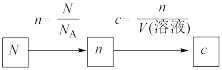
③标准状况下,气体溶质的物质的量浓度的计算
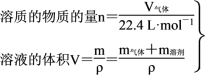 c=
c=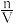
(3)注意:
①物质加入水中,注意溶质的判断。如SO3 H2SO4,Na2O或Na2O2
H2SO4,Na2O或Na2O2 NaOH,Na
NaOH,Na NaOH,NH3
NaOH,NH3 NH3·H2O等。
NH3·H2O等。
②溶液浓度与离子浓度的定量关系要注意电离程度与组成。
如0.1 mol·L-1的K2SO4溶液中c(K+)=0.2 mol·L-1。
(4)物质的量浓度与溶质的质量分数的换算
①换算公式:cB=_______ mol·L-1.M:溶质B的摩尔质量 ρ:溶液密度(g·mL-1)。
②推导方法:设溶液体积为1 L,则cB=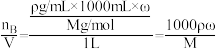 mol·L-1。
mol·L-1。
(5)溶液稀释和混合的计算
①溶液稀释的有关计算:稀释前后溶质的物质的量和质量都保持不变。_______ 。
②溶液混合的计算:混合前后溶质的物质的量或质量不变。_______ 。
注意:无特别指明时,V(混)≠V1+V2;V(混)= ,但溶液的质量守恒:m(混)=m1+m2。
,但溶液的质量守恒:m(混)=m1+m2。
(6)常见物理量之间的换算关系
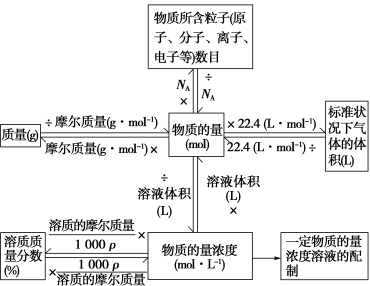
万能公式:n= =cBV
=cBV
(1)计算的基本公式:c=
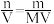 。
。(2)计算的基本类型和方法:
①已知溶质的质量

②已知溶液中某种粒子的数目
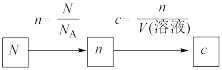
③标准状况下,气体溶质的物质的量浓度的计算
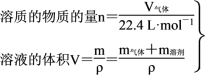 c=
c=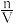
(3)注意:
①物质加入水中,注意溶质的判断。如SO3
 H2SO4,Na2O或Na2O2
H2SO4,Na2O或Na2O2 NaOH,Na
NaOH,Na NaOH,NH3
NaOH,NH3 NH3·H2O等。
NH3·H2O等。②溶液浓度与离子浓度的定量关系要注意电离程度与组成。
如0.1 mol·L-1的K2SO4溶液中c(K+)=0.2 mol·L-1。
(4)物质的量浓度与溶质的质量分数的换算
①换算公式:cB=
②推导方法:设溶液体积为1 L,则cB=
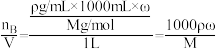 mol·L-1。
mol·L-1。(5)溶液稀释和混合的计算
①溶液稀释的有关计算:稀释前后溶质的物质的量和质量都保持不变。
②溶液混合的计算:混合前后溶质的物质的量或质量不变。
注意:无特别指明时,V(混)≠V1+V2;V(混)=
 ,但溶液的质量守恒:m(混)=m1+m2。
,但溶液的质量守恒:m(混)=m1+m2。(6)常见物理量之间的换算关系

万能公式:n=
 =cBV
=cBV
您最近一年使用:0次
名校
3 . NA是阿伏加德罗常数的值。下列说法正确的是
| A.26gC2H2与C6H6混合气体中含σ键的数目为3NA |
| B.过量的铜与含0.2molHNO3的浓硝酸反应,转移电子的数目大于0.1NA |
| C.16.25gFeCl3水解形成的Fe(OH)3胶体粒子数为0.1NA |
| D.标准状况下11.2LCl2溶于水,溶液中Cl-、ClO-和HClO的微粒数之和为NA |
您最近一年使用:0次
名校
4 . 设NA表示阿伏加德罗常数的值,下列说法正确的是
A. 中含有电子数为10NA 中含有电子数为10NA |
B. 苯中σ键总数为6NA 苯中σ键总数为6NA |
C. 和足量 和足量 反应,生成 反应,生成 和 和 的混合物,转移电子数为NA 的混合物,转移电子数为NA |
D.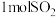 溶于足量水中,溶液中 溶于足量水中,溶液中 的分子数为NA 的分子数为NA |
您最近一年使用:0次
5 . NA为阿伏加德罗常数的值。下列说法不正确的是
| A.3.6g由CaS和CaO2组成的混合物中含有阴、阳离子总数为0.1NA |
| B.S2和S8的混合物共6.4g,其中所含硫原子数一定为0.2NA. |
| C.将0.1molCl2溶于水中,溶液中Cl-、ClO-、HClO的数目之和为0.2NA |
| D.标准状况下,11.2L1H37Cl气体中含有的中子数为10NA |
您最近一年使用:0次
22-23高一上·全国·课时练习
解题方法
6 . 下列各组物质中,含原子数最多的是
| A.0.4molNH3 | B.4℃时5.4mL水 |
| C.10g氖气 | D.6.02×1023个硫酸分子 |
您最近一年使用:0次
名校
7 . 下列物质所含分子数最多的是
A.0.2 mol  |
B.标准状况下2.24 L  |
C.44 g ( ( 的摩尔质量为 的摩尔质量为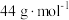 ) ) |
D. 个NO( 个NO( 为阿伏加德罗常数的值) 为阿伏加德罗常数的值) |
您最近一年使用:0次
2022-09-05更新
|
868次组卷
|
3卷引用:专题四 化学计量及应用
2021高三·全国·专题练习
8 . 标准状况下,22.4 L氧气、氮气和CO的混合气体中含有2NA个原子___________
您最近一年使用:0次
2021高三·全国·专题练习
9 . 标准状况下,22.4 L SO3中含有SO3分子数为NA___________
您最近一年使用:0次
2021高三·全国·专题练习
解题方法
10 . 所含共价键数目均为NA的白磷和甲烷的物质的量相等。(_______)
您最近一年使用:0次



