名校
1 . 小组探究Na2CO3和NaHCO3与碱的反应,实验过程及结果如下。
资料:等浓度指的是1L中含 、
、 离子数目相同
离子数目相同
下列说法不正确 的是
资料:等浓度指的是1L中含
 、
、 离子数目相同
离子数目相同实验装置 | 试剂X | 实验结果 | ||
 | I | Ⅱ | Ⅲ | ①Ⅱ、Ⅲ均产生白色沉淀 ②烧杯中溶液pH变化如下  |
| 蒸馏水 | 等浓度Na2CO3 稀溶液 | 等浓度 NaHCO3 稀溶液 | ||
| A.I是空白实验,排除因体积变化对Ⅱ、Ⅲ溶液pH的影响 |
B.Ⅱ和I的pH曲线基本重合,说明 与OH-不反应,Ⅱ中发生反应: 与OH-不反应,Ⅱ中发生反应: +Ca2+=CaCO3↓ +Ca2+=CaCO3↓ |
C.Ⅲ比Ⅱ的pH曲线降低,说明 与OH-反应,Ⅲ中初期发生反应: 与OH-反应,Ⅲ中初期发生反应: +OH-+Ca2+=CaCO3↓+H2O +OH-+Ca2+=CaCO3↓+H2O |
| D.Ⅲ中石灰水恰好完全反应时,溶液呈中性 |
您最近一年使用:0次
2024-01-07更新
|
66次组卷
|
2卷引用:北京市第三十五中学2023-2024学年高一上学期期中考试化学试题
名校
解题方法
2 . 除去粗盐中的杂质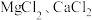 和
和 ,过程如下:
,过程如下:
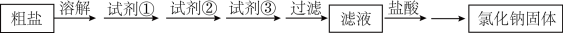
下列有关说法中,不正确的是
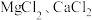 和
和 ,过程如下:
,过程如下: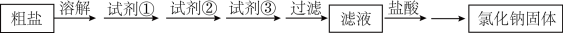
下列有关说法中,不正确的是
A.除去 的主要反应: 的主要反应: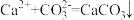 |
| B.除杂试剂在使用时应该过量,保证杂质除干净 |
C.除去 的主要反应: 的主要反应: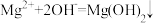 |
D.试剂①、②、③可以分别是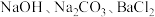 |
您最近一年使用:0次
解题方法
3 . 钠与水反应、铁与水蒸气反应的实验装置图如下。
下列说法不正确 的是
Ⅰ.钠与水反应 | Ⅱ.铁与水蒸气反应 |
|
|
| A.Ⅰ中钠熔化成小球说明反应放热和钠的熔点低 |
B.Ⅰ中钠与水反应的离子方程式: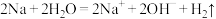 |
| C.Ⅱ中有肥皂泡产生说明有H2生成 |
D.Ⅱ中铁与水蒸气反应的化学方程式: |
您最近一年使用:0次
名校
4 . 为落实“五水共治”,某工厂拟综合处理含 废水和工业废气(主要含N2、CO2、SO2、NO、CO,不考虑其他成分),设计了如下流程:
废水和工业废气(主要含N2、CO2、SO2、NO、CO,不考虑其他成分),设计了如下流程:不正确 的是
 废水和工业废气(主要含N2、CO2、SO2、NO、CO,不考虑其他成分),设计了如下流程:
废水和工业废气(主要含N2、CO2、SO2、NO、CO,不考虑其他成分),设计了如下流程:
| A.固体1中主要含有Ca(OH)2、CaCO3、CaSO3 |
| B.X可以是空气,且需过量 |
| C.捕获剂所捕获的气体主要是CO |
D.处理含NH 废水时,发生反应的离子方程式为: 废水时,发生反应的离子方程式为: + + =N2↑+2H2O =N2↑+2H2O |
您最近一年使用:0次
2023-11-21更新
|
215次组卷
|
4卷引用:北京市中国人民大学附属中学2021-2022学年高一下学期期末考试化学试题
名校
解题方法
5 . 1923年化学家Bronsted和Lowry提出:凡是能给出质子(质子即 )的分子或离子都是质子的给体,称为酸;凡是能与质子结合的分子或离子都是质子的受体,称为碱,即:
)的分子或离子都是质子的给体,称为酸;凡是能与质子结合的分子或离子都是质子的受体,称为碱,即: 、
、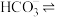
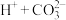 ,即:
,即: ,其中左边的酸是右边碱的共轭酸,而右边的碱则是左边酸的共轭碱,彼此联系在一起叫做共轭酸碱对。共轭酸的酸性越强,其共轭碱就越弱。相同条件下,已知碱性由强到弱:
,其中左边的酸是右边碱的共轭酸,而右边的碱则是左边酸的共轭碱,彼此联系在一起叫做共轭酸碱对。共轭酸的酸性越强,其共轭碱就越弱。相同条件下,已知碱性由强到弱:
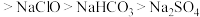 ,以下说法
,以下说法不正确 的是
 )的分子或离子都是质子的给体,称为酸;凡是能与质子结合的分子或离子都是质子的受体,称为碱,即:
)的分子或离子都是质子的给体,称为酸;凡是能与质子结合的分子或离子都是质子的受体,称为碱,即: 、
、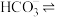
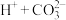 ,即:
,即: ,其中左边的酸是右边碱的共轭酸,而右边的碱则是左边酸的共轭碱,彼此联系在一起叫做共轭酸碱对。共轭酸的酸性越强,其共轭碱就越弱。相同条件下,已知碱性由强到弱:
,其中左边的酸是右边碱的共轭酸,而右边的碱则是左边酸的共轭碱,彼此联系在一起叫做共轭酸碱对。共轭酸的酸性越强,其共轭碱就越弱。相同条件下,已知碱性由强到弱:
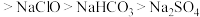 ,以下说法
,以下说法A.物质酸性由强到弱: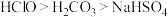 |
B.物质酸性由强到弱: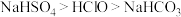 |
C.向NaClO溶液中通入少量 : :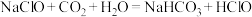 |
D.向 中加入 中加入 溶液可产生HClO 溶液可产生HClO |
您最近一年使用:0次
名校
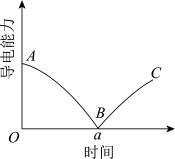
6 . 向 溶液中滴入几滴酚酞溶液,然后逐滴加入稀硫酸,测得混合溶液的导电能力随时间变化如右图所示。下列说法
溶液中滴入几滴酚酞溶液,然后逐滴加入稀硫酸,测得混合溶液的导电能力随时间变化如右图所示。下列说法不正确 的是
 溶液中滴入几滴酚酞溶液,然后逐滴加入稀硫酸,测得混合溶液的导电能力随时间变化如右图所示。下列说法
溶液中滴入几滴酚酞溶液,然后逐滴加入稀硫酸,测得混合溶液的导电能力随时间变化如右图所示。下列说法
A.A点导电能力强是 在水中以离子形式存在的实验证据 在水中以离子形式存在的实验证据 |
B.AB段发生反应的离子方程式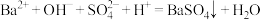 |
C.C点溶液中存在的微粒主要有 、 、 、 、 |
D.溶液由红色变成无色、产生白色沉淀分别是 、 、 参加反应的实验证据 参加反应的实验证据 |
您最近一年使用:0次
名校
解题方法
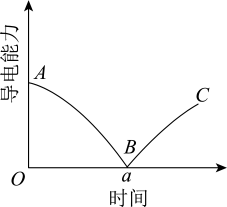
7 . 某同学向一定体积的Ba(OH)2溶液中滴加稀硫酸,测得混合溶液的导电能力随时间变化如下图所示。下列说法中,正确的是
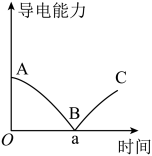

A.实验过程中反应的离子方程式为Ba2++2OH-+SO +2H+=BaSO4↓+2H2O +2H+=BaSO4↓+2H2O |
| B.AB段溶液的导电能力减弱,说明生成的BaSO4不是电解质 |
| C.a时刻Ba(OH)2溶液与稀硫酸恰好完全中和 |
| D.BC段溶液的导电能力增大,主要是由于过量的Ba(OH)2电离出的离子导电 |
您最近一年使用:0次
2023-01-09更新
|
450次组卷
|
17卷引用:北京市西城区2020-2021学年高一上学期期末考试化学试题
北京市西城区2020-2021学年高一上学期期末考试化学试题北京市丰台区2021-2022学年高一上学期期中考试化学试题北京市北京师范大学附属中学2022-2023学年高一上学期期中考试化学试题北京市第七中学2022-2023学年高一上学期期中考试化学试题黑龙江省黑河市五校(嫩江市第一中学,嫩江市职业高中,黑河七中,伊拉哈中学,海江中学)2021-2022学年高一上学期期末联考化学试题辽宁省葫芦岛市普通高中2021-2022学年高一上学期期末学业质量监测化学试题天津市实验中学2022-2023学年高一上学期学情评估(一)化学试题安徽省宿州市十三所重点中学2022-2023学年高一上学期期中质量检测化学试题浙江省宁波市五校联盟2022-2023学年高一上学期期中联考化学试题广东省惠州市惠阳区中山中学2021-2022学年高一上学期第三次月考质量检测化学试题湖南省岳阳市2022-2023学年高一上学期期末教学质量监测化学试题山东省曹县第一中学2022-2023学年高一上学期期末考试化学试题河北省保定市泽龙实验中学2022-2023学年高一下学期开学检测化学试题甘肃省张掖市高台县第一中学2022-2023学年高一下学期开学检测化学试题天津市东丽区2021-2022学年高一上学期期末质量检测化学试题广东省揭阳市揭东第一中学等三校2022-2023学年高一下学期期中联考化学试题湖南省岳阳市2022-2023学年高一上学期1月期末考试化学试题
名校
解题方法
8 . 下列关于钠与水反应的说法中,不正确 的是
| A.从元素化合价及氧化还原反应规律分析,反应中产生的无色气体只能是氢气 |
| B.钠块熔化成小球,说明钠的熔点低且该反应放热 |
| C.将酚酞溶液滴入反应后的溶液中,溶液变红,说明产物有碱性物质生成 |
| D.钠与水反应的离子方程式:Na+H2O=Na++OH-+H2↑ |
您最近一年使用:0次
2023-01-05更新
|
326次组卷
|
4卷引用:北京市东城区2022-2023学年高一上学期期末统一检测化学试卷
北京市东城区2022-2023学年高一上学期期末统一检测化学试卷北京市第九中学2023-2024学年高一上学期期中统练化学试题北京市第一五六中学2023-2024学年高一上学期期中考试化学试题(已下线)第05讲 钠及钠的氧化物-【暑假自学课】2023年新高一化学暑假精品课(人教版2019必修第一册)
名校
9 . 向Ba(OH)2溶液中滴入几滴酚酞溶液,然后逐滴加入稀硫酸,测得混合溶液的导电能力随时间变化如图所示。下列说法不正确 的是

| A.A点导电率高是Ba(OH)2在水中以离子形式存在的实验证据 |
B.溶液由红色变成无色、产生白色沉淀分别是OH-、 参加反应的实验证据 参加反应的实验证据 |
C.AB段发生反应的离子方程式为Ba2++OH- + +H+=BaSO4↓+H2O +H+=BaSO4↓+H2O |
D.C点溶液中存在的微粒主要有H2O、H+、 |
您最近一年使用:0次
2022-01-25更新
|
737次组卷
|
7卷引用:北京市丰台区2021-2022学年高一上学期期末考试化学试题
北京市丰台区2021-2022学年高一上学期期末考试化学试题北京师范大学附属实验中学2022-2023学年高一上学期期中考试化学试题北京市第一六六中学2023-2024学年高一上学期期中考试化学试题北京市第十一中学2023-2024学年高一上学期期中考试化学试题(已下线)1.2.2 离子方程式的书写-2022-2023学年高一化学上学期课后培优分级练 (人教版2019必修第一册)山东省临沂市沂水县第一中学2022-2023学年高一上学期阶段性检测 化学试题福建省厦门市翔安第一中学2023-2024学年高一上学期第二次月考试化学卷
名校
解题方法
10 . 溶液的导电能力(I)与溶液中离子浓度的大小有关,向0.01 mol·L-1Ba(OH)2溶液中滴加 0.2 mol·L-1H2SO4溶液时,溶液的导电能力与所加H2SO4溶液的体积的关系如图所示,下列说法不正确的是


| A.a点溶液导电能力较强,说明Ba(OH)2是电解质 |
B.b点发生反应的离子方程式为Ba2++ =BaSO4↓ =BaSO4↓ |
C.c点溶液中含有的主要微粒是H+和 |
| D.b点观察到的现象是溶液中有白色沉淀生成 |
您最近一年使用:0次
2021-10-13更新
|
369次组卷
|
3卷引用:北京市中关村中学2020-2021学年高一上学期期中考试化学试题





