解题方法
1 . 十种元素A~J在元素周期表中的相对位置如表所示:
回答下列问题:
(1)A、C元素组成的常见化合物分别为M和N,其中M含有18个电子。
①M的电子式为______ 。
②实验室制取N的化学方程式为______ 。
(2)元素C、H、J的最高价含氧酸的酸性从强到弱的顺序为______ (用相应酸的化学式表示)。
(3)不同价态的I元素可以相互转化,若反应前后存在4种价态的I元素,写出该反应的化学方程式:______ 。
(4)请用一个化学方程式证明元素D和E的非金属性强弱关系:______ 。
(5)某研究学习小组用如图装置探究F、G的金属性强弱。

当试管(Ⅰ)出现______ 的现象、且试管(Ⅱ)出现______ 的现象时,能说明金属性F大于G,写出试管(Ⅱ)依次发生反应的离子方程式:______ 、_____ 。
| 族 周期 | ⅠA | 0 | ||||||
| 1 | A | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | B | C | D | E | ||||
| 3 | F | G | H | Ⅰ | J | |||
(1)A、C元素组成的常见化合物分别为M和N,其中M含有18个电子。
①M的电子式为
②实验室制取N的化学方程式为
(2)元素C、H、J的最高价含氧酸的酸性从强到弱的顺序为
(3)不同价态的I元素可以相互转化,若反应前后存在4种价态的I元素,写出该反应的化学方程式:
(4)请用一个化学方程式证明元素D和E的非金属性强弱关系:
(5)某研究学习小组用如图装置探究F、G的金属性强弱。

当试管(Ⅰ)出现
您最近一年使用:0次
2 . 某实验小组拟制取银氨溶液,并探究银镜反应。
Ⅰ.氨气的制备
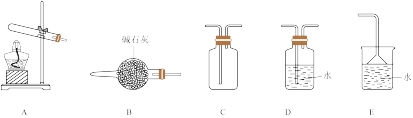
(1)利用上图装置,实验室制取氨气的化学方程式为_______ 。
(2)用上述方法制取干燥纯净的氨气,其所选装置的连接顺序为:A→_______→_______→_______(按气流方向,用英文字母表示)。_______
Ⅱ.银氨溶液制备
(3)将制得的氨气溶于水,稀释至质量分数约为2%,选用甲基橙做指示剂,用标准盐酸滴定其物质的量浓度,达到滴定终点的现象为_______ 。
(4)取上述新制氨水,进行如下实验。已知:白色AgOH沉淀不稳定,极易分解生成棕褐色 ;
; 溶于浓氨水生成
溶于浓氨水生成 。
。
①步骤a中产生沉淀的离子方程式_______ 。
②取步骤b中制得的银氨溶液,进行如下实验,

通过对溶液A的检验,可证明银氨溶液中溶质主要为 ,而不是
,而不是 。请将实验方案和现象补充完整:
。请将实验方案和现象补充完整:
取少量溶液A于试管中,测定其pH约为10(查资料得知同浓度的 ,pH在13左右);
,pH在13左右);
另取少量溶液A于试管中,加入过量盐酸酸化后滤去沉淀,再向滤液中加入_______ (试剂名称),充分反应后若出现_______ ,则证明溶质为 。
。
Ⅲ.银镜反应:
已知:随 降低,
降低, 氧化性减弱,银氨溶液中存在平衡
氧化性减弱,银氨溶液中存在平衡 。
。
(5)分析实验,推测实验d中未见银镜的原因可能是_______ 。
Ⅰ.氨气的制备
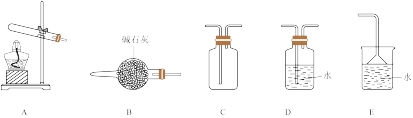
(1)利用上图装置,实验室制取氨气的化学方程式为
(2)用上述方法制取干燥纯净的氨气,其所选装置的连接顺序为:A→_______→_______→_______(按气流方向,用英文字母表示)。
Ⅱ.银氨溶液制备
(3)将制得的氨气溶于水,稀释至质量分数约为2%,选用甲基橙做指示剂,用标准盐酸滴定其物质的量浓度,达到滴定终点的现象为
(4)取上述新制氨水,进行如下实验。已知:白色AgOH沉淀不稳定,极易分解生成棕褐色
 ;
; 溶于浓氨水生成
溶于浓氨水生成 。
。| 实验装置 | 步骤 | 实验操作 | 实验现象 |
 | a | 向试管中滴加2~3滴2%氨水,并不断振荡 | 产生棕褐色沉淀 |
| b | 继续向试管中逐滴加入2%氨水,并不断振荡,至沉淀恰好完全溶解,停止滴加氨水。 | 沉淀消失 |
②取步骤b中制得的银氨溶液,进行如下实验,

通过对溶液A的检验,可证明银氨溶液中溶质主要为
 ,而不是
,而不是 。请将实验方案和现象补充完整:
。请将实验方案和现象补充完整:取少量溶液A于试管中,测定其pH约为10(查资料得知同浓度的
 ,pH在13左右);
,pH在13左右);另取少量溶液A于试管中,加入过量盐酸酸化后滤去沉淀,再向滤液中加入
 。
。Ⅲ.银镜反应:
已知:随
 降低,
降低, 氧化性减弱,银氨溶液中存在平衡
氧化性减弱,银氨溶液中存在平衡 。
。| 实验装置 | 步骤 | 实验操作 | 实验现象 |
 | c | 取步骤b中得到的银氨溶液于试管中,加入3滴新开瓶的40%的乙醛溶液;水浴加热3分钟 | 试管内壁出现光亮的银镜 |
| d | 取步骤b中得到银氨溶液的试管中滴加浓氨水,无明显现象,加入新开瓶的40%的乙醛溶液,振荡,水浴加热3分钟 | 闻到刺激性气味,溶液略显灰色,试管壁未见银镜 |
您最近一年使用:0次
2022-12-28更新
|
490次组卷
|
3卷引用:广东省汕头市普通高中2022-2023学年高三上学期教学质量检测化学试题
3 . 氨是重要的化工原料,回答下列问题:
I.氨气的制备

(1)制取并收集一瓶干燥氨气,上述装置的连接顺序为A→_____→_____→C→____,____ ,制气时的化学方程式为___________ ,收集时气体从___________ 口进入
II.氨气的性质
(2)装置如图所示,打开止水夹,用热毛巾将烧瓶捂热,水上喷形成红色喷泉,说明氨气___________ 。

III.氨气的用途
利用下图装置由氨制硝酸,实验时戊中溶液呈淡黄色时关闭分液漏斗活塞。

(3)Na2O2的作用___________ ,证明有硝酸生成的实验是___________ ,发生反应的离子方程式___________ 。
(4)实验中的氮氧化物(NOx)尾气折算成标准状况下的体积为aL,完全吸收时,烧杯中c(NaOH)至少是___________ mol/L(忽略溶液体积变化)。
I.氨气的制备

(1)制取并收集一瓶干燥氨气,上述装置的连接顺序为A→_____→_____→C→____,
II.氨气的性质
(2)装置如图所示,打开止水夹,用热毛巾将烧瓶捂热,水上喷形成红色喷泉,说明氨气

III.氨气的用途
利用下图装置由氨制硝酸,实验时戊中溶液呈淡黄色时关闭分液漏斗活塞。

(3)Na2O2的作用
(4)实验中的氮氧化物(NOx)尾气折算成标准状况下的体积为aL,完全吸收时,烧杯中c(NaOH)至少是
您最近一年使用:0次
2021-12-11更新
|
1080次组卷
|
3卷引用:四川省达州市2021-2022学年高三上学期第一次诊断考试理科综合化学试题
四川省达州市2021-2022学年高三上学期第一次诊断考试理科综合化学试题(已下线)微专题24 氯气、氨气、二氧化硫的实验室制备与应用-备战2023年高考化学一轮复习考点微专题四川省达州市普通高中2022届高三第一次诊断性测试理综化学试题



