名校
解题方法
1 . 土壤中的硝酸盐会被细菌分解。有一种脱氧硫杆菌能够利用土壤中的硫化物来分解硝酸盐,其主要化学原理如下:
 (条件略)
(条件略)
1.写出 的电子式
的电子式___________ 。
2.能证明 是离子化合物的事实是___________。
是离子化合物的事实是___________。
3.下列说法正确的是___________。
4.下列说法中正确的是___________。
 (条件略)
(条件略)1.写出
 的电子式
的电子式2.能证明
 是离子化合物的事实是___________。
是离子化合物的事实是___________。| A.常温下是固体 | B.易溶于水 | C.水溶液能导电 | D.熔融态能导电 |
A. 和 和 溶于水时都会破坏离子键 溶于水时都会破坏离子键 |
B. 能电离出 能电离出 和 和 ,所以 ,所以 是离子化合物 是离子化合物 |
C. 中每个原子的最外层都具有8电子的稳定结构 中每个原子的最外层都具有8电子的稳定结构 |
D. 是共价分子,液氮汽化时破坏共价键和分子间作用力 是共价分子,液氮汽化时破坏共价键和分子间作用力 |
| A.离子化合物中一定只有离子键 | B.共价化合物中一定只有共价键 |
| C.氯化氢溶于水时会破坏离子键 | D.蔗糖溶于水时破坏分子间作用力 |
您最近一年使用:0次
2 . 利用下图装置制取 并验证
并验证 的性质。下列说法错误的是
的性质。下列说法错误的是
 并验证
并验证 的性质。下列说法错误的是
的性质。下列说法错误的是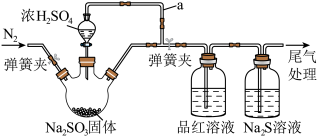
| A.导管a的作用是保证浓硫酸顺利滴下 |
B.品红溶液褪色,说明 可能具有漂白性 可能具有漂白性 |
C. 溶液中出现浑浊,证明 溶液中出现浑浊,证明 具有氧化性 具有氧化性 |
D.三颈烧瓶内反应开始前通 与反应结束后通 与反应结束后通 目的相同 目的相同 |
您最近一年使用:0次
解题方法
3 . 氨的催化氧化过程是当下研究的重要课题。
(1) 与
与 在一定压强和800℃条件下发生催化氧化反应时,可发生不同反应:
在一定压强和800℃条件下发生催化氧化反应时,可发生不同反应:
反应i:

反应ii: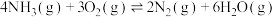
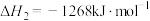
①该条件下 与
与 反应生成NO的热化学方程式为
反应生成NO的热化学方程式为___________ 。
②在恒温恒容密闭容器中,下列说法可以证明反应i已达到平衡状态的是___________ (填序号)。
A.
B.n个 键断裂的同时,有n个
键断裂的同时,有n个 键形成
键形成
C.混合气体的密度不变
D.容器内压强不变
③反应i与反应ii有关物质产率与温度的关系如图。下列说法正确 的是___________ 。
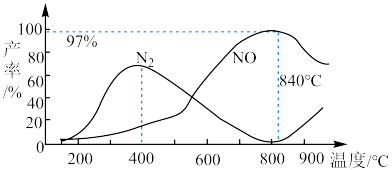
A.氨催化氧化生成 时,温度应控制在400℃左右
时,温度应控制在400℃左右
B.对反应升温可提高反应物转化率
C.提高物料比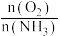 的值,主要目的的是提高反应速率
的值,主要目的的是提高反应速率
D.840℃后,NO产率下降的主要原因是以反应(ii)为主
(2)在两个恒压密闭容器中分别充入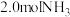 、
、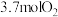 ,仅发生反应ii,测得
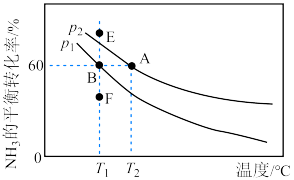
,仅发生反应ii,测得 的平衡转化率随温度的变化如图所示。
的平衡转化率随温度的变化如图所示。
①
___________  (填“>”或“<”),理由是
(填“>”或“<”),理由是___________ 。
②若容器的初始体积为2.0L,则在A点状态下平衡时容器中
___________  。
。
③B点的平衡常数
___________ 。(用分压表示,气体分压=气体总压 气体的物质的量分数。写出代数式,无需计算具体结果)
气体的物质的量分数。写出代数式,无需计算具体结果)
④若温度为 ,压强为
,压强为 ,容器的初始体积为2.0L时,分别充入
,容器的初始体积为2.0L时,分别充入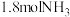 、
、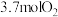 、0.2molAr发生反应ii,此时
、0.2molAr发生反应ii,此时 的平衡转化率为图中的点
的平衡转化率为图中的点___________ (选填“E”、“B”或“F”)。
(1)
 与
与 在一定压强和800℃条件下发生催化氧化反应时,可发生不同反应:
在一定压强和800℃条件下发生催化氧化反应时,可发生不同反应:反应i:


反应ii:
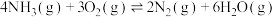
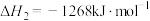
①该条件下
 与
与 反应生成NO的热化学方程式为
反应生成NO的热化学方程式为②在恒温恒容密闭容器中,下列说法可以证明反应i已达到平衡状态的是
A.

B.n个
 键断裂的同时,有n个
键断裂的同时,有n个 键形成
键形成C.混合气体的密度不变
D.容器内压强不变
③反应i与反应ii有关物质产率与温度的关系如图。下列说法

A.氨催化氧化生成
 时,温度应控制在400℃左右
时,温度应控制在400℃左右B.对反应升温可提高反应物转化率
C.提高物料比
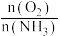 的值,主要目的的是提高反应速率
的值,主要目的的是提高反应速率D.840℃后,NO产率下降的主要原因是以反应(ii)为主
(2)在两个恒压密闭容器中分别充入
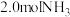 、
、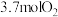 ,仅发生反应ii,测得
,仅发生反应ii,测得 的平衡转化率随温度的变化如图所示。
的平衡转化率随温度的变化如图所示。
①

 (填“>”或“<”),理由是
(填“>”或“<”),理由是②若容器的初始体积为2.0L,则在A点状态下平衡时容器中

 。
。③B点的平衡常数

 气体的物质的量分数。写出代数式,无需计算具体结果)
气体的物质的量分数。写出代数式,无需计算具体结果)④若温度为
 ,压强为
,压强为 ,容器的初始体积为2.0L时,分别充入
,容器的初始体积为2.0L时,分别充入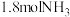 、
、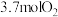 、0.2molAr发生反应ii,此时
、0.2molAr发生反应ii,此时 的平衡转化率为图中的点
的平衡转化率为图中的点
您最近一年使用:0次
名校
解题方法
4 . 人类对物质微观结构的探索从未停歇,随着科学技术的发展,新的发现将继续揭开开原子更深层次结构的奥秘.
(1)原子结构模型的演变顺序正确的是
①道尔顿模型 ②有核模型 ③葡萄干面包模型 ④电子云模型 ⑤玻尔模型
(2)第一位通过实验证明原子可以再分的科学家是
(3)卢瑟福团队用 粒子
粒子 来轰击金箔,该化学符号中4代表的含义是①
来轰击金箔,该化学符号中4代表的含义是①_____________ ;在1~18号元素中,最外层电子数与氦原子相等的元素是②_____________ (填元素符号)。
(4)氦元素在自然界中仅有 和
和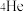 两种原子,它们具有相同的
两种原子,它们具有相同的
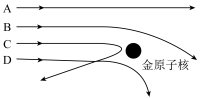
(5)当用 粒子轰击金箔时,如图所示的运动轨迹中不可能存在的是
粒子轰击金箔时,如图所示的运动轨迹中不可能存在的是
(6)关于 粒子散射实验现象的记载如下:①________的
粒子散射实验现象的记载如下:①________的 粒子都直接穿过金箔,②______的
粒子都直接穿过金箔,②______的 粒子发生偏转,③ 的
粒子发生偏转,③ 的 粒子甚至被直接反弹回去.①②③三处空格分别为
粒子甚至被直接反弹回去.①②③三处空格分别为
(7)通过该试验,卢瑟福得出了原子结构的_____________ 模型。
(8)2022年诺贝尔化学奖授予三位在“点击化学和生物正交化学”方面作出突出贡献的科学家.点击化学的核心理念是,通过小单元的简便拼接,快速可靠地完成各种各样分子的化学合成.在点击化学中,反应快速发生,而且不会产生副产物.下列有关点击化学说法错误的是
(1)原子结构模型的演变顺序正确的是
①道尔顿模型 ②有核模型 ③葡萄干面包模型 ④电子云模型 ⑤玻尔模型
| A.①③②⑤④ | B.①②③④⑤ | C.①⑤③②④ | D.①③⑤④② |
(2)第一位通过实验证明原子可以再分的科学家是
| A.德谟克利特 | B.道尔顿 | C.汤姆孙 | D.卢瑟福 |
(3)卢瑟福团队用
 粒子
粒子 来轰击金箔,该化学符号中4代表的含义是①
来轰击金箔,该化学符号中4代表的含义是①(4)氦元素在自然界中仅有
 和
和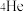 两种原子,它们具有相同的
两种原子,它们具有相同的 | A.质子数 | B.中子数 | C.物理性质 | D.化学性质 |
(5)当用
 粒子轰击金箔时,如图所示的运动轨迹中不可能存在的是
粒子轰击金箔时,如图所示的运动轨迹中不可能存在的是 
| A.A | B.B | C.C | D.D |
(6)关于
 粒子散射实验现象的记载如下:①________的
粒子散射实验现象的记载如下:①________的 粒子都直接穿过金箔,②______的
粒子都直接穿过金箔,②______的 粒子发生偏转,③ 的
粒子发生偏转,③ 的 粒子甚至被直接反弹回去.①②③三处空格分别为
粒子甚至被直接反弹回去.①②③三处空格分别为 | A.绝大多数,极少数,个别 | B.个别,极少数,绝大多数 |
| C.几乎半数,几乎半数,个别 | D.个别,几乎半数,几乎半数 |
(7)通过该试验,卢瑟福得出了原子结构的
(8)2022年诺贝尔化学奖授予三位在“点击化学和生物正交化学”方面作出突出贡献的科学家.点击化学的核心理念是,通过小单元的简便拼接,快速可靠地完成各种各样分子的化学合成.在点击化学中,反应快速发生,而且不会产生副产物.下列有关点击化学说法错误的是
| A.点击化学的反应中会出现新的分子 | B.点击化学的反应中会出现新的原子 |
| C.点击化学能提高反应的准确性 | D.点击化学在生物医疗领域有广泛的应用前景 |
您最近一年使用:0次
名校
解题方法
5 . 醇酸树脂是一种成膜性很好的树脂,下面是一种醇酸树脂的合成线路线:
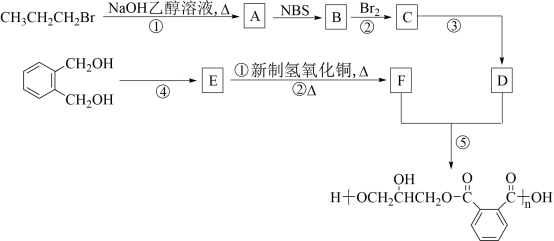
已知: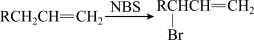
(1)D的化学名称是_______ ,B中含有的官能团的名称是_______ ,③的反应的类型是_______ 。
(2)③的反应试剂与条件为_______ ,④的反应试剂与条件为_______ ,①的反应方程式为_______ 。
(3)下列说法正确的是_______。
(4)工业上大量获得A的方法是_______。
(5)下列关于F的说法正确的是_______。
(6)含有相同官能团的有机物通常具有相似的化学性质,因此可以预测醇酸树脂具有与_______ 化合物相似的化学性质(填写物质类别)。
(7)化合物X是 的同分异构体,能与
的同分异构体,能与 溶液发生显色反应,1moX最多消耗1molNa,其中有五种不同的等效氢,个数比为1:2:2:2:3,则其结构简式为
溶液发生显色反应,1moX最多消耗1molNa,其中有五种不同的等效氢,个数比为1:2:2:2:3,则其结构简式为_______ 。(写出一种即可)
(8)工业上可用丙烯氧化法生产丙烯酸(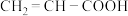 ),得到的丙烯酸中往往混有丙烯醛(
),得到的丙烯酸中往往混有丙烯醛(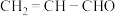 ),证明生成的丙烯酸中混有丙烯醛的方法是:
),证明生成的丙烯酸中混有丙烯醛的方法是:_______ 。

已知:
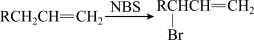
(1)D的化学名称是
(2)③的反应试剂与条件为
(3)下列说法正确的是_______。
| A.醇酸树脂是纯净物 | B.1mol E与足量的银氨溶液反应能生成2mol Ag |
| C.E能使酸性高锰酸钾溶液褪色 | D.反应⑤是加聚反应 |
| A.石油裂解 | B.丙醇脱水 | C.石油分馏 | D.煤的干馏 |
| A.所有原子一定都在同一平面上 | B.1molF最多可与5mol氢气发生加成反应 |
| C.至少有12个原子在同一平面上 | D.1molF与足量 溶液反应得44g 溶液反应得44g |
(7)化合物X是
 的同分异构体,能与
的同分异构体,能与 溶液发生显色反应,1moX最多消耗1molNa,其中有五种不同的等效氢,个数比为1:2:2:2:3,则其结构简式为
溶液发生显色反应,1moX最多消耗1molNa,其中有五种不同的等效氢,个数比为1:2:2:2:3,则其结构简式为(8)工业上可用丙烯氧化法生产丙烯酸(
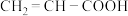 ),得到的丙烯酸中往往混有丙烯醛(
),得到的丙烯酸中往往混有丙烯醛(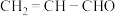 ),证明生成的丙烯酸中混有丙烯醛的方法是:
),证明生成的丙烯酸中混有丙烯醛的方法是:
您最近一年使用:0次
2023-03-17更新
|
381次组卷
|
2卷引用:上海市建平中学2022-2023学年高二下学期3月测试化学(B 卷)试题
6 . 向AgNO3溶液中通入过量SO2,过程和现象如图。

经检验,白色沉淀为Ag2SO3;灰色固体中含有Ag。
下列说法不正确的是

经检验,白色沉淀为Ag2SO3;灰色固体中含有Ag。
下列说法不正确的是
| A.①中生成白色沉淀的离子方程式为2Ag++SO2+H2O=Ag2SO3↓+2H+ |
| B.①中未生成Ag2SO4,证明溶度积:Ksp(Ag2SO3)<Ksp(Ag2SO4) |
| C.②中的现象体现了Ag+的氧化性 |
| D.该实验条件下,SO2与AgNO3反应生成Ag2SO3的速率大于生成Ag的速率 |
您最近一年使用:0次
2022-05-15更新
|
2164次组卷
|
12卷引用:北京市海淀区2022届高三二模化学试题
北京市海淀区2022届高三二模化学试题北京市海淀区2021-2022学年高三下学期期末练习化学试题河南省南阳市第一中学校2023届高三上学期第二次阶段考试化学试题北京市第二十中学2022-2023学年高二上学期期末考试化学试题广东省昌乐市第一中学2022-2023学年高三上学期期末质量检测化学试题江苏省南京外国语学校2022-2023学年高三上学期期末考试化学试题江苏省南京外国语学校2022-2023学年高三上学期期末考试化学试题江苏省百校联考2022-2023学年高二下学期5月第一次考试化学试题北京市顺义牛栏山第一中学2023-2024学年高二上学期期中考试化学试题辽宁省沈阳市第二中学2023-2024学年高三上学期期末模拟考试化学试题北京市第十三中学2023-2024学年高三上学期开学考化学试卷 北京市中关村中学2023-2024学年高三下学期3月月考化学试题
名校
7 . 蕴藏在海底的大量“可燃冰”(甲烷的水合物)是一种清洁燃料,其开发利用是解决能源危机的重要课题。在一定条件下 与
与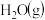 可发生反应:
可发生反应:

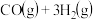 ,该反应的能量变化如下图所示。
,该反应的能量变化如下图所示。
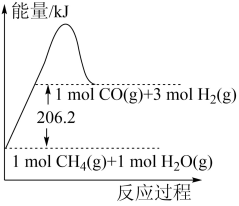
请回答下列问题:
(1)请用电子式表示CH4的形成过程_______ 。
(2)在一定条件下,由一定量的 和
和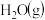 反应生成了
反应生成了 和6molH2(g)时所吸收的热量为
和6molH2(g)时所吸收的热量为_______ kJ。
(3)下列措施中可以加快该反应的化学反应速率的是_______  填字母
填字母 。
。
A.恒温恒容条件下,向其中充入
B.恒温恒压条件下,向其中充入
C.恒温恒容条件下,向其中充入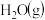
D.其他条件不变,降低温度
E.其他条件不变,减小容器的体积
F.其他条件不变,及时分离出生成的H2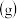
(4)T℃下,在容积为2L的恒容密闭容器中通入 和
和 发生该反应。
发生该反应。
①下列说法中能证明该反应已达到化学平衡状态的是_______  填字母
填字母 。
。
A.单位时间内消耗
 的同时生成了
的同时生成了
B.一个 键断裂的同时有三个
键断裂的同时有三个 键断裂
键断裂
C.密闭容器中混合气体的密度不再变化
D.混合气体的平均相对分子质量不再变化
E.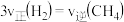
F.密闭容器内总压强不再变化
②若该反应达到化学平衡状态时,容器内气体的压强变为起始压强的1.6倍,则达平衡时 的转化率为
的转化率为_______ ,CO的体积分数为_______ %(计算结果保留一位小数 )。
 与
与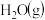 可发生反应:
可发生反应:

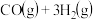 ,该反应的能量变化如下图所示。
,该反应的能量变化如下图所示。
请回答下列问题:
(1)请用电子式表示CH4的形成过程
(2)在一定条件下,由一定量的
 和
和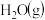 反应生成了
反应生成了 和6molH2(g)时所吸收的热量为
和6molH2(g)时所吸收的热量为(3)下列措施中可以加快该反应的化学反应速率的是
 填字母
填字母 。
。A.恒温恒容条件下,向其中充入

B.恒温恒压条件下,向其中充入

C.恒温恒容条件下,向其中充入
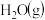
D.其他条件不变,降低温度
E.其他条件不变,减小容器的体积
F.其他条件不变,及时分离出生成的H2
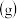
(4)T℃下,在容积为2L的恒容密闭容器中通入
 和
和 发生该反应。
发生该反应。①下列说法中能证明该反应已达到化学平衡状态的是
 填字母
填字母 。
。A.单位时间内消耗

 的同时生成了
的同时生成了
B.一个
 键断裂的同时有三个
键断裂的同时有三个 键断裂
键断裂C.密闭容器中混合气体的密度不再变化
D.混合气体的平均相对分子质量不再变化
E.
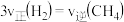
F.密闭容器内总压强不再变化
②若该反应达到化学平衡状态时,容器内气体的压强变为起始压强的1.6倍,则达平衡时
 的转化率为
的转化率为
您最近一年使用:0次
2022-04-18更新
|
256次组卷
|
2卷引用:湖北省新高考联考协作体2021-2022学年高一下学期期中考试化学试题
名校
8 . 化学实验是验证假设、推断结论的重要方法。某小组同学学习了氧化还原知识后,对碳与浓硫酸的反应及其产物进行验证,对 的性质进行了探究。
的性质进行了探究。
(1)盛放浓硫酸的仪器名称:_____ 。
(2)写出碳与浓硫酸在加热条件下反应的化学方程式:_____ 。
(3)证明产物中有水生成的实验现象_____ 。
(4)装置④的作用是_____ ,体现 的
的_____ 性(填氧化或漂白或还原)。
(5)装置⑤的作用是_____ 。
(6)证明产物中有 的实验现象是
的实验现象是_____ 。
(7)如何说明装置①的反应产物中有 ?
?_____ 。
(8)如何检验装置①反应后的圆底烧瓶中是否含有 离子?
离子?_____ 。
 的性质进行了探究。
的性质进行了探究。
(1)盛放浓硫酸的仪器名称:
(2)写出碳与浓硫酸在加热条件下反应的化学方程式:
(3)证明产物中有水生成的实验现象
(4)装置④的作用是
 的
的(5)装置⑤的作用是
(6)证明产物中有
 的实验现象是
的实验现象是(7)如何说明装置①的反应产物中有
 ?
?(8)如何检验装置①反应后的圆底烧瓶中是否含有
 离子?
离子?
您最近一年使用:0次
9 .  和
和 等金属氯化物易升华.
等金属氯化物易升华.
(1)设计实验证明 是共价化合物
是共价化合物________________ ;
(2) 是一种强电解质,写出
是一种强电解质,写出 溶液中滴加少量氨水的离子方程式
溶液中滴加少量氨水的离子方程式________________ 。
 和
和 等金属氯化物易升华.
等金属氯化物易升华.(1)设计实验证明
 是共价化合物
是共价化合物(2)
 是一种强电解质,写出
是一种强电解质,写出 溶液中滴加少量氨水的离子方程式
溶液中滴加少量氨水的离子方程式
您最近一年使用:0次
名校
10 . 以下说法正确的是
A.下列反应可证明苯环受甲基的影响,甲苯易被酸性高锰酸钾氧化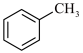  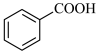 |
| B.鉴别苯和甲苯可将少量溴水滴入分别盛有苯和甲苯的两支试管中,观察现象 |
| C.间二甲苯只有一种结构可说明苯分子中不存在碳碳单键与碳碳双键交替的结构 |
| D.1mol乙醇可以与足量金属钠反应,生成0.5molH2,能证明乙醇分子有一个H原子与其余的H原子不同 |
您最近一年使用:0次



