1 . 利用下图装置制取 并验证
并验证 的性质。下列说法错误的是
的性质。下列说法错误的是
 并验证
并验证 的性质。下列说法错误的是
的性质。下列说法错误的是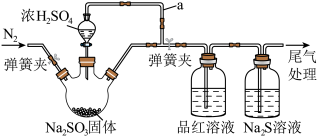
| A.导管a的作用是保证浓硫酸顺利滴下 |
B.品红溶液褪色,说明 可能具有漂白性 可能具有漂白性 |
C. 溶液中出现浑浊,证明 溶液中出现浑浊,证明 具有氧化性 具有氧化性 |
D.三颈烧瓶内反应开始前通 与反应结束后通 与反应结束后通 目的相同 目的相同 |
您最近一年使用:0次
解题方法
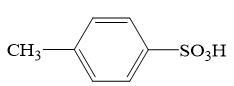
2 . Ⅰ.对甲苯磺酸是一种白色晶体,熔点107℃,易溶于醇、醚和水,是用途广泛的化工原料。
(2)写出反应的化学方程式。___________
Ⅱ.根据对甲苯磺酸的结构,有同学推测对甲苯磺酸的性质和硫酸相似,进行了如下探究:
(3)对甲苯磺酸可能是强酸,电离方程式: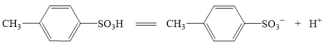 ,设计简单实验证明猜想。
,设计简单实验证明猜想。___________
(4)采用如图所示装置进行实验,观察到蔗糖迅速变黑。上述实验现象说明对甲苯磺酸具有___________ 。
(5)向吸收液中滴加一定量___________ 溶液,仍未观察到明显现象,说明对甲苯磺酸不具有强氧化性。
A.Ba(OH)2 B.NaCl C.CaCl2
Ⅲ.对甲苯磺酸可做酯化反应的催化剂,催化合成丙酸乙酯。
将0.2 mol丙酸(M=74 g∙mol−1)、1 g对甲苯磺酸和0.24 mol乙醇(M=46 g∙mol−1)加入三口瓶中,加热进行反应。反应结束后将反应液过滤,分别经水、碳酸钠溶液、饱和食盐水洗涤,干燥后进行蒸馏,蒸出17.4 g馏分。
(6)计算该反应的产率____ 。(产率= ,写出计算过程,结果保留1位小数)
,写出计算过程,结果保留1位小数)
(7)请评价用对甲苯磺酸代替浓硫酸做酯化反应催化剂的优点___________ 。
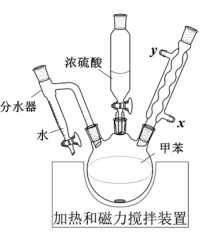
| A.当分水器中的水量不再增加时,停止加热 |
| B.分水器可将反应体系中的甲苯移除 |
| C.烧瓶中不需要添加沸石 |
| D.冷凝水从x口进入 |
Ⅱ.根据对甲苯磺酸的结构,有同学推测对甲苯磺酸的性质和硫酸相似,进行了如下探究:
(3)对甲苯磺酸可能是强酸,电离方程式:
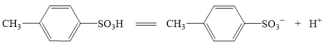 ,设计简单实验证明猜想。
,设计简单实验证明猜想。(4)采用如图所示装置进行实验,观察到蔗糖迅速变黑。上述实验现象说明对甲苯磺酸具有
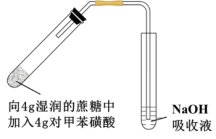
(5)向吸收液中滴加一定量
A.Ba(OH)2 B.NaCl C.CaCl2
Ⅲ.对甲苯磺酸可做酯化反应的催化剂,催化合成丙酸乙酯。
将0.2 mol丙酸(M=74 g∙mol−1)、1 g对甲苯磺酸和0.24 mol乙醇(M=46 g∙mol−1)加入三口瓶中,加热进行反应。反应结束后将反应液过滤,分别经水、碳酸钠溶液、饱和食盐水洗涤,干燥后进行蒸馏,蒸出17.4 g馏分。
(6)计算该反应的产率
 ,写出计算过程,结果保留1位小数)
,写出计算过程,结果保留1位小数)(7)请评价用对甲苯磺酸代替浓硫酸做酯化反应催化剂的优点
您最近一年使用:0次
名校
3 . 下列针对有机实验的说法正确的是
| 实验目的 | 实验操作、现象或结论 | 实验解释 | |
| A | 检验电石和水反应可产生乙炔 | 将产生的气体通过饱和食盐水后,再通入酸性 溶液中;若酸性 溶液中;若酸性 溶液褪色,说明有乙炔生成 溶液褪色,说明有乙炔生成 | 因为用饱和食盐水可以除去乙炔中混有的还原性杂质,所以证明有乙炔生成 |
| B | 探究光照条件下甲烷与氯气反应产物的种类 | 当氯气少量时,生成物中含有 、 、 、 、 、 、 等 等 | 因为 、 、 、 、 、 、 中碳氢键极性逐渐增强,所以与氯气发生取代反应的能力逐渐增强 中碳氢键极性逐渐增强,所以与氯气发生取代反应的能力逐渐增强 |
| C | 比较钠与水、钠与乙醇两个反应速率的大小 | 向两只分别盛有水和无水乙醇的烧杯中,各加入相同大小的钠,发现钠与水反应更剧烈 | 因为钠与水反应放出热量更多,温度升高更快,所以反应更剧烈 |
| D | 检验苯和液溴在 催化剂作用下生成的气体 催化剂作用下生成的气体 | 将苯、液溴、铁粉混合物反应产生的气体通入到 溶液中有淡黄色沉淀产生 溶液中有淡黄色沉淀产生 | 因为产生了淡黄色沉淀,所以证明有HBr气体生成 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
4 . 某小组同学探究SO2与新制Cu(OH)2悬浊液反应的实验装置图如下所示:
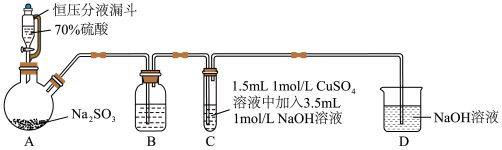
下列说法不正确的是

下列说法不正确的是
| A.配制70%硫酸溶液需要用到的仪器有烧杯、量筒、玻璃棒、胶头滴管 |
| B.装置B的作用是监控SO2流速,其中试剂可以用饱和NaHSO4溶液 |
| C.反应开始时C中出现砖红色沉淀,氧化剂和还原剂的物质的量之比为2:1 |
| D.反应后向C的溶液中加入稀盐酸酸化后,再滴加BaCl2溶液、有白色沉淀生成,证明反应中SO2作还原剂 |
您最近一年使用:0次
2024-04-07更新
|
421次组卷
|
2卷引用:2024届甘肃省兰州市高三下学期诊断考试化学试卷
名校
解题方法
5 . 硫酸渣是硫酸生产过程中产生的固体废料,主要化学成分有 、
、 、
、 等。
等。
I.研究人员可利用硫酸渣制备高纯度硫酸亚铁晶体,流程如下图所示:
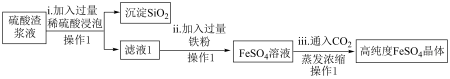
已知: 是难溶于水的酸性氧化物。
是难溶于水的酸性氧化物。
(1)操作1是______ 。
(2)步骤ii中涉及反应的离子方程式有_______ 、_________ 。
(3)步骤iii中的 的作用是
的作用是______ 。
(4)取少量高纯度 晶体配成溶液,
晶体配成溶液,_______ (操作和现象),证明该晶体中不含 。
。
Ⅱ.研究人员还可利用硫酸渣与含氯废气( 和HCl混合气)来制备絮凝剂聚合氯化铁,流程如下图所示:
和HCl混合气)来制备絮凝剂聚合氯化铁,流程如下图所示:
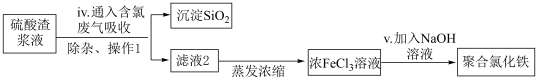
已知:聚合氯化铁的一种形式为 。
。
(5)写出以下物质中加点元素 的化合价: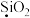
_____ ,
_____ 。
(6)下列关于步骤iv中含氯废气作用的说法中,不正确的是___________ 。
a.盐酸中 作用是使FeO、
作用是使FeO、 溶解
溶解
b.氯气参与反应的离子方程式为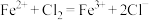
c.盐酸与氯气中的氯元素均转移到 中
中
(7)补全步骤v中涉及到反应的化学方程式______ 。
 。
。
 、
、 、
、 等。
等。I.研究人员可利用硫酸渣制备高纯度硫酸亚铁晶体,流程如下图所示:

已知:
 是难溶于水的酸性氧化物。
是难溶于水的酸性氧化物。(1)操作1是
(2)步骤ii中涉及反应的离子方程式有
(3)步骤iii中的
 的作用是
的作用是(4)取少量高纯度
 晶体配成溶液,
晶体配成溶液, 。
。Ⅱ.研究人员还可利用硫酸渣与含氯废气(
 和HCl混合气)来制备絮凝剂聚合氯化铁,流程如下图所示:
和HCl混合气)来制备絮凝剂聚合氯化铁,流程如下图所示:
已知:聚合氯化铁的一种形式为
 。
。(5)写出以下物质中
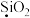

(6)下列关于步骤iv中含氯废气作用的说法中,不正确的是
a.盐酸中
 作用是使FeO、
作用是使FeO、 溶解
溶解b.氯气参与反应的离子方程式为
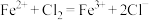
c.盐酸与氯气中的氯元素均转移到
 中
中(7)补全步骤v中涉及到反应的化学方程式
 。
。
您最近一年使用:0次
名校
6 . 对下列图示的说法错误的是
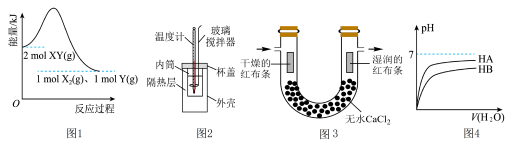

| A.图1中反应物的总键能大于生成物的总键能 |
| B.用图2进行中和热的测定实验时,氢氧化钠一次性快速加入,测定的中和热数值误差更小 |
C.图3中通入干燥的 可验证干燥的氯气是否有漂白性 可验证干燥的氯气是否有漂白性 |
D.由图4可证明图示条件下 |
您最近一年使用:0次
7 . 为了探究温度对水解平衡的影响,用手持技术测定一定浓度 溶液的pH随温度变化的关系如图所示,下列说法不正确的是
溶液的pH随温度变化的关系如图所示,下列说法不正确的是
 溶液的pH随温度变化的关系如图所示,下列说法不正确的是
溶液的pH随温度变化的关系如图所示,下列说法不正确的是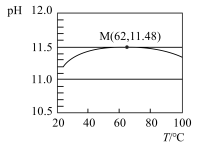
| A.该实验能证明升温促进水解 | B.点M之后 水解放热 水解放热 |
C.点M处溶液中 略大于 略大于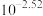 mol/L mol/L | D.点M后pH下降是因为升温对 的影响更大 的影响更大 |
您最近一年使用:0次
名校
8 . 利用元素的化合价推测物质的性质是化学研究的重要手段。如图是硫元素的常见化合价与部分物质类别的对应关系: 的电子式为
的电子式为________ ;将 与X混合,可生成黄色固体,该反应氧化产物与还原产物的质量之比为
与X混合,可生成黄色固体,该反应氧化产物与还原产物的质量之比为________ 。
(2)S粉与热的Z浓溶液反应可转化为________ ,反应的化学方程式为________ 。
(3)配平下列反应:_____
____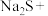 ____
____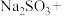 ____
____ ____
____ ____
____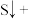 ____
____
(4)下列有关硫及其化合物的性质,说法正确的是
(5)某同学为探究Cu与浓硫酸的反应,用如图所示的装置进行有关实验。________ 。
②C的作用是________ ,装置D中试管口放置的棉花应浸有一种液体,这种液体是________ 。
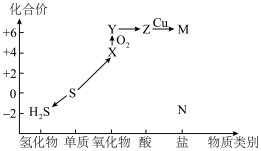
 的电子式为
的电子式为 与X混合,可生成黄色固体,该反应氧化产物与还原产物的质量之比为
与X混合,可生成黄色固体,该反应氧化产物与还原产物的质量之比为(2)S粉与热的Z浓溶液反应可转化为
(3)配平下列反应:
____
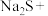 ____
____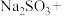 ____
____ ____
____ ____
____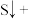 ____
____
(4)下列有关硫及其化合物的性质,说法正确的是
| A.X能使溴水褪色,证明X有漂白性 | B.将X通入 溶液中有白色沉淀生成 溶液中有白色沉淀生成 |
C.硫在过量的 中燃烧可以生成Y 中燃烧可以生成Y | D.若N为钠盐,则N与Z的稀溶液反应可生成 |
(5)某同学为探究Cu与浓硫酸的反应,用如图所示的装置进行有关实验。

②C的作用是
您最近一年使用:0次
名校
解题方法
9 . 高氯酸三碳酰肼合镍(GTN)的组成可表示为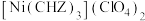 ,其中CHZ为碳酰肼(结构简式为:
,其中CHZ为碳酰肼(结构简式为: )。已知
)。已知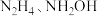 (羟胺)具有类似于
(羟胺)具有类似于 的碱性。
的碱性。

(1)请用方程式解释羟胺水溶液呈碱性
 溶液反应实现转化2得到
溶液反应实现转化2得到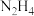 和两种常见钠盐,反应的化学方程式为
和两种常见钠盐,反应的化学方程式为(2)下列有关说法正确的是___________。
A. 均只含极性键 均只含极性键 |
B.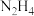 与过量硫酸溶液反应形成酸式盐的化学式为 与过量硫酸溶液反应形成酸式盐的化学式为 |
C.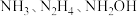 的碱性依次减弱 的碱性依次减弱 |
D. 是一种无机酸酯,转化3发生的是取代反应 是一种无机酸酯,转化3发生的是取代反应 |
(3)酸性强弱:
 (
(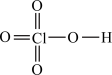 )
)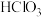 (
( )(填“>”“=”或“<”),请从结构角度解释原因
)(填“>”“=”或“<”),请从结构角度解释原因(4)
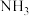 与
与 反应生成固体产物中除了尿素还有另外一种盐,设计实验证明该固体产物中的N元素
反应生成固体产物中除了尿素还有另外一种盐,设计实验证明该固体产物中的N元素
您最近一年使用:0次
解题方法
10 . 根据分散质粒子的大小,可将分散系分为溶液、胶体、浊液等.胶体的微粒大小使其具有一些特殊性质,在生产生活中广泛存在。
(1)气溶胶是新型冠状病毒传播的重要途径。气溶胶属于胶体的一种,下列关于胶体的说法不正确的是_____ 。
(2)已知土壤胶体粒子带负电,在使用下列化肥时,农作物对氮肥的吸收效果最差的是_____ 。
(3)下列应用或事实与胶体的性质无关的是_____ 。
生活中许多物质能构成胶体分散系,比如将淀粉分散在水中能形成胶体分散系,如图是小李同学设计的提纯淀粉胶体的实验:在半透膜里盛有淀粉胶体和KI溶液混合液体,将半透膜悬挂在盛有蒸馏水的烧杯中,回答下列问题:
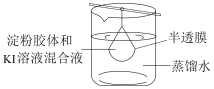
(4)淀粉胶体______ (选填“透过”或“未透过”),试设计简单实验证明你的结论:_____ 。
(5)半透膜的实验原理在我们日常生活中及医疗、工业等领域有广泛应用,试举一例:_____ 。
(1)气溶胶是新型冠状病毒传播的重要途径。气溶胶属于胶体的一种,下列关于胶体的说法不正确的是
| A.胶体是一种分散系,属于混合物 |
| B.胶体分散质粒子直径介于10-9-10-7m之间 |
| C.胶体的本质特征是能发生丁达尔效应 |
| D.利用丁达尔现象是区分胶体和溶液的一种常用方法 |
| A.碳酸氢铵 | B.硝酸钾 | C.氯化铵 | D.硫酸铵 |
| A.用明矾净化饮用水 |
| B.在氯化铁溶液中滴加氯氧化钠溶液出现红褐色沉淀 |
| C.用石膏或盐卤点制豆腐 |
| D.清晨的阳光穿过茂密的林木枝叶所产生的美丽光线 |
生活中许多物质能构成胶体分散系,比如将淀粉分散在水中能形成胶体分散系,如图是小李同学设计的提纯淀粉胶体的实验:在半透膜里盛有淀粉胶体和KI溶液混合液体,将半透膜悬挂在盛有蒸馏水的烧杯中,回答下列问题:

(4)淀粉胶体
(5)半透膜的实验原理在我们日常生活中及医疗、工业等领域有广泛应用,试举一例:
您最近一年使用:0次



