1 . 某同学用如图所示装置制备溴苯并验证其反应类型,下列说法错误的是
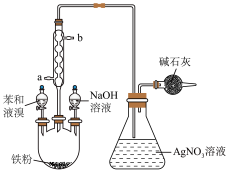
| A.将苯和液溴加入三颈烧瓶后,可观察到瓶内有红棕色气体产生 |
| B.冷凝管中冷凝水的流向为a口进,b口出 |
| C.AgNO3溶液中产生黄色沉淀即可证明该反应为取代反应 |
| D.实验结束后,应先向三颈烧瓶中加入NaOH溶液再拆卸装置 |
您最近一年使用:0次
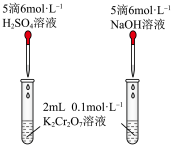
2 . 关于如图所示实验的说法,正确的是
|
|
| i.推测CH3COOH的Ka和H2CO3的Ka1的大小 | ii.研究c(H+)对Cr2O 、CrO 、CrO 相互转化的影响 相互转化的影响 |
|
|
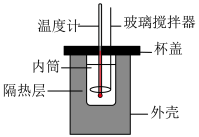
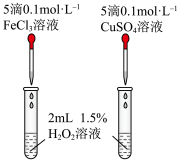
| iii.测定稀盐酸与NaOH溶液中和的反应热 | iv.比较Fe3+与Cu2+对H2O2分解反应的催化效果 |
A.图i反应的离子方程式为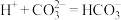 |
B.图ii证明增大 有利于增大 有利于增大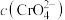 ,减小 ,减小 |
| C.图iii中去隔热层不保温,测得的反应热偏小 |
D.图iv中将 溶液换为 溶液换为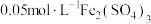 溶液更为合理 溶液更为合理 |
您最近一年使用:0次
名校
解题方法
3 . 完成下列问题
(1)下列变化过程中有可能不涉及氧化还原反应的是_______
(2)氮元素在地球上含量丰富,氮及其化合物在工农业生产、生活中有着重要作用。下列叙述与氮元素的循环无关的是____
(3)关于新制饱和氯水,下列叙述正确的是_______
(4)下列实验中,能实现不同价态含硫物质的转化的是_______
(5)据文献报道,我国学者提出O2氧化HBr生成Br2的反应历程如图所示。下列有关该历程的说法错误的是_____

(6)高锰酸钾是生活中常用的一种消毒剂,也常被用于物质成分分析。二氧化锰是制取高锰酸钾的重要原料。制取高锰酸钾的方法是先用二氧化锰制取锰酸钾(K2MnO4),再转化为高锰酸钾。反应过程如下:
i.______MnO2+________KOH+____KClO3 ____K2MnO4+____KCl+____H2O
____K2MnO4+____KCl+____H2O
ii.3K2MnO4+4HCl=2KMnO4+4KCl+2H2O+MnO2
①下列反应中二氧化锰做氧化剂的是___________
a.实验室用氯酸钾和二氧化锰的混合物加热制取氧气
b.实验室用二氧化锰和浓盐酸混合加热制取氯气
c.用二氧化锰和铝混合发生铝热反应制取锰
d.用二氧化锰、氢氧化钾、氯酸钾共熔制取锰酸钾(K2MnO4)
②设计实验证明二氧化锰中含有哪种类型的化学键。(写出实验步骤、现象和结论)_________
③配平反应i的化学方程式_________ 。
④标出反应ii中电子转移的方向和数目_________ 。
⑤若工业上使用纯度为87%的软锰矿(主要成分为二氧化锰)制取高锰酸钾,理论上10吨软锰矿可制取高锰酸钾___________ 吨。
(1)下列变化过程中有可能不涉及氧化还原反应的是_______
| A.钝化 | B.漂白 | C.固氮 | D.燃烧 |
(2)氮元素在地球上含量丰富,氮及其化合物在工农业生产、生活中有着重要作用。下列叙述与氮元素的循环无关的是____
| A.工业合成氨的过程是固氮的过程 |
| B.自然界中,氨是动物体特别是蛋白质腐败后的产物 |
| C.为防止粮食、罐头、水果等食品腐烂,常用氮气作保护气 |
| D.在雷鸣的雨天,N2与O2会发生反应并最终转化为硝酸盐被植物吸收 |
(3)关于新制饱和氯水,下列叙述正确的是_______
| A.加入适量NaOH,溶液黄绿色褪去,说明氯水中含有Cl2分子 |
| B.加入少量NaCl粉末,溶液漂白性增强 |
| C.加入少量的碳酸钠粉末,pH增大,溶液漂白性一定减弱 |
| D.光照过程中,有气泡冒出,溶液的导电性减弱 |
(4)下列实验中,能实现不同价态含硫物质的转化的是_______
| A.向含足量NaOH的Na2S溶液中加入Na2SO3 |
| B.常温下,向试管中加入1mL浓硫酸和一小块铜片 |
| C.将0.5g硫粉和1.0g铁粉均匀混合,在石棉网上用红热玻璃棒触及粉末一端至粉末红热 |
| D.向Na2SO3固体中加入70%的浓硫酸制备SO2 |
(5)据文献报道,我国学者提出O2氧化HBr生成Br2的反应历程如图所示。下列有关该历程的说法错误的是_____

| A.O2氧化HBr生成Br2的总反应为:O2+4HBr=2Br2+2H2O |
| B.中间体HOOBr和HOBr中Br的化合价相同 |
| C.发生步骤②时,断裂的化学键既有极性键又有非极性键 |
| D.步骤③中,每生成1molBr2转移2mol电子 |
(6)高锰酸钾是生活中常用的一种消毒剂,也常被用于物质成分分析。二氧化锰是制取高锰酸钾的重要原料。制取高锰酸钾的方法是先用二氧化锰制取锰酸钾(K2MnO4),再转化为高锰酸钾。反应过程如下:
i.______MnO2+________KOH+____KClO3
 ____K2MnO4+____KCl+____H2O
____K2MnO4+____KCl+____H2Oii.3K2MnO4+4HCl=2KMnO4+4KCl+2H2O+MnO2
①下列反应中二氧化锰做氧化剂的是
a.实验室用氯酸钾和二氧化锰的混合物加热制取氧气
b.实验室用二氧化锰和浓盐酸混合加热制取氯气
c.用二氧化锰和铝混合发生铝热反应制取锰
d.用二氧化锰、氢氧化钾、氯酸钾共熔制取锰酸钾(K2MnO4)
②设计实验证明二氧化锰中含有哪种类型的化学键。(写出实验步骤、现象和结论)
③配平反应i的化学方程式
④标出反应ii中电子转移的方向和数目
⑤若工业上使用纯度为87%的软锰矿(主要成分为二氧化锰)制取高锰酸钾,理论上10吨软锰矿可制取高锰酸钾
您最近一年使用:0次
名校
解题方法
4 . 某化学小组欲探究反应“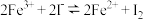 ”为可逆反应,做了如下实验:
”为可逆反应,做了如下实验:

已知:
现象为:实验ii中产生了黄色沉淀;实验iii中溶液变蓝;实验iv中溶液不变蓝,下列说法中不正确 的是
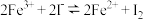 ”为可逆反应,做了如下实验:
”为可逆反应,做了如下实验:
已知:

现象为:实验ii中产生了黄色沉淀;实验iii中溶液变蓝;实验iv中溶液不变蓝,下列说法中
A.实验ii中产生黄色沉淀的离子方程式为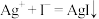 |
B.实验iii加淀粉溶液变蓝,证明棕黄色溶液中有 生成 生成 |
C.设计实验iv的目的是为了排除空气中氧气氧化 的可能 的可能 |
D.通过上述实验可以证明“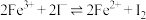 ”为可逆反应 ”为可逆反应 |
您最近一年使用:0次
2024-01-20更新
|
148次组卷
|
3卷引用:北京市顺义区2023-2024学年高二上学期期末质量监测化学试题
名校
5 . 以下说法错误的是
| A.苯的邻二氯代物只有一种证明苯没有单双键交替的结构 |
| B.甲苯使高锰酸钾溶液褪色说明苯环对甲基有影响 |
C.CH3CHBrCH2CH3与 的醇溶液共热反应有机产物有2种(不考虑顺反异构) 的醇溶液共热反应有机产物有2种(不考虑顺反异构) |
| D.甲苯在一定条件下发生硝化反应产物只有TNT一种 |
您最近一年使用:0次
7日内更新
|
293次组卷
|
2卷引用:黑龙江省哈尔滨市第九中学校2023-2024学年高二下学期期中考试化学试卷
6 . 以锗石矿A(化学式为 )为原料,可以实现如下转化。
)为原料,可以实现如下转化。
请回答:
(1)D的化学式为___________ ,液体E的沸点___________  (填“高于”或“低于”)。
(填“高于”或“低于”)。
(2)下列说法不正确 的是___________。
(3)已知液体E以物质的量之比1∶1与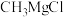 反应,该反应可用来构建
反应,该反应可用来构建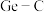 键,写出步骤Ⅲ的化学方程式
键,写出步骤Ⅲ的化学方程式___________ 。
(4)写出溶液G中所有的阴离子___________ ,设计实验证明溶液G中含有Cu元素___________ 。
 )为原料,可以实现如下转化。
)为原料,可以实现如下转化。
请回答:
(1)D的化学式为
 (填“高于”或“低于”)。
(填“高于”或“低于”)。(2)下列说法
| A.气体B是形成酸雨的成分之一 | B.固体C中可能含有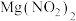 |
C. 也能与浓盐酸反应 也能与浓盐酸反应 | D.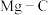 键强于 键强于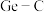 键 键 |
(3)已知液体E以物质的量之比1∶1与
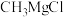 反应,该反应可用来构建
反应,该反应可用来构建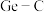 键,写出步骤Ⅲ的化学方程式
键,写出步骤Ⅲ的化学方程式(4)写出溶液G中所有的阴离子
您最近一年使用:0次
7 . 秸秆是成熟农作物茎叶的总称。农作物光合作用的产物有一半以上存在于秸秆中,秸秆富含氮、磷、钾、钙、镁和有机质。秸秆(含多糖类物质)的综合利用具有重要意义。
(1)下列关于糖类的说法正确的是_______ 。
A.糖类都有甜味,具有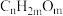 的通式
的通式
B.麦芽糖水解生成互为同分异构体的葡萄糖和果糖
C.用银镜反应不能判断淀粉水解是否完全
D.淀粉和纤维素都属于多糖,是同分异构体
E.糖类是多羟基的醛类化合物
(2)下列关于糖类、油脂、蛋白质的说法中正确的是_______ 。
A.蛋白质、植物油、纤维素、淀粉都属于高分子化合物
B.葡萄糖和果糖都能进一步水解
C.油脂在酸性条件下水解与在碱性条件下水解产物完全相同
D.纤维素在人体消化过程中起着重要作用,但纤维素不能作为人类的营养物质
E.蛋白质在酶的作用下最终水解为氨基酸,氨基酸既具有酸性又具有碱性
(3)下列检验或除杂方法正确的是_______。
(4)我国于2008年起禁止农民焚烧秸秆,焚烧秸秆的危害有_______。
(1)下列关于糖类的说法正确的是
A.糖类都有甜味,具有
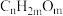 的通式
的通式 B.麦芽糖水解生成互为同分异构体的葡萄糖和果糖
C.用银镜反应不能判断淀粉水解是否完全
D.淀粉和纤维素都属于多糖,是同分异构体
E.糖类是多羟基的醛类化合物
(2)下列关于糖类、油脂、蛋白质的说法中正确的是
A.蛋白质、植物油、纤维素、淀粉都属于高分子化合物
B.葡萄糖和果糖都能进一步水解
C.油脂在酸性条件下水解与在碱性条件下水解产物完全相同
D.纤维素在人体消化过程中起着重要作用,但纤维素不能作为人类的营养物质
E.蛋白质在酶的作用下最终水解为氨基酸,氨基酸既具有酸性又具有碱性
(3)下列检验或除杂方法正确的是_______。
A.向 中加入少量 中加入少量 溶液有淡黄色沉淀生成说明 溶液有淡黄色沉淀生成说明 含有溴原子 含有溴原子 |
B.向淀粉溶液量加入稀硫酸,加热几分钟,冷却后先加入NaOH中和稀硫酸再加入新制 悬浊液,加热,若没有砖红色沉淀生成,说明淀粉没有水解成葡萄糖 悬浊液,加热,若没有砖红色沉淀生成,说明淀粉没有水解成葡萄糖 |
C.欲证明 中含有碳碳双键滴入酸性 中含有碳碳双键滴入酸性 溶液,若紫色褪去,说明其中含有碳碳双键 溶液,若紫色褪去,说明其中含有碳碳双键 |
| D.欲除去苯中混有的苯酚,向混合液中加入浓溴水,充分反应后过滤 |
(4)我国于2008年起禁止农民焚烧秸秆,焚烧秸秆的危害有_______。
| A.温室效应 | B.酸雨 | C.可吸入颗粒物超标 | D.臭氧空洞 |
您最近一年使用:0次
名校
8 . 有机化合物不仅与人类的衣、食、住、行密切相关,而且还是揭示生命现象及其规律的钥匙运用所学知识,回答下列问题。
(1)甲烷是最简单的有机物,在我国的南海、东海海底已发现天然气(含甲烷等)的水合物,外形似冰,被称为“可燃冰”。下列关于甲烷的说法错误的是______。
(2)下列事实能证明甲烷分子是以碳原子为中心的正四面体结构而不是正方形的平面结构的是______。
(3)取一支大试管,用排饱和食盐水的方法收集4体积氯气,再通入l体积甲烷。把装有混合气体的试管倒置于盛有饱和食盐水的水槽甲,对该实验中现象的分析错误的是_______。
(4)烷烃的主要来源是石油和天然气,是重要的化工原料和能源物资。下列关于烷烃的叙述不正确的是______。
(5)A(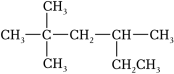 )的系统命名名称是
)的系统命名名称是 ________ 。A的一氯代物的同分异构体有 _____ 种(不考虑立体异构)。
乙烯是石油化工的重要基本原料。通过一系列化学反应,可以由乙烯得到有机高分子材料、药物等成千上万种有用的物质。如图是一套实验室制取乙烯并验证乙烯具有还原性的实验装置。_______ ,反应类型______ 。
(7)圆底烧瓶中除了主反应外还会发生副反应,请写出副反应的产物________ 。
(8)能够说明乙烯具有还原性的现象是_________ 。
(9)实验时烧瓶中液体混合物逐渐变黑,装置甲的作用是_________ 。
(10)能鉴别的同时除去甲烷中混有的乙烯的试剂是_____。
(11)下列物质不可能是乙烯的加成产物的是______。
(12)乙烯是一种重要的化工原料,下列关于乙烯的说法不正确的是______。
(13)下列对于乙烯(CH2=CH2)和聚乙烯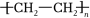 的说法错误的是_____。
的说法错误的是_____。
(1)甲烷是最简单的有机物,在我国的南海、东海海底已发现天然气(含甲烷等)的水合物,外形似冰,被称为“可燃冰”。下列关于甲烷的说法错误的是______。
| A.甲烷是无色、无味,密度比空气小,极难溶于水的气体 |
| B.甲烷不能发生氧化反应 |
| C.点燃甲烷气体时,一定要检验纯度 |
| D.沼气和天然气的主要成分都是甲烷 |
(2)下列事实能证明甲烷分子是以碳原子为中心的正四面体结构而不是正方形的平面结构的是______。
| A.CH3Cl只存在一种结构 | B.CH2Cl2只存在一种结构 |
| C.CHCl3只存在一种结构 | D.四个C﹣H键完全相同 |
(3)取一支大试管,用排饱和食盐水的方法收集4体积氯气,再通入l体积甲烷。把装有混合气体的试管倒置于盛有饱和食盐水的水槽甲,对该实验中现象的分析错误的是_______。

| A.试管内壁会出现油状液滴,液滴成分是一氯甲烷 |
| B.水槽中会析出白色晶体,晶体成分是氯化钠 |
| C.反应结束后试管内液面会上升,是由于反应后试管内气体压强减小 |
| D.试管中会形成白雾,是由于反应生成的氯化氢气体遇水形成的酸雾 |
(4)烷烃的主要来源是石油和天然气,是重要的化工原料和能源物资。下列关于烷烃的叙述不正确的是______。
| A.烷烃中的碳原子均以共价单键与碳原子或氢原子相连 |
| B.凡是化学式符合通式CnH2n+2的烃一定是烷烃 |
| C.甲烷、乙烷及丙烷均无同分异构体 |
| D.碳原子数相同的烷烃的同分异构体中,支链越多沸点越高 |
(5)A(
 )的系统命名名称是
)的系统命名名称是 乙烯是石油化工的重要基本原料。通过一系列化学反应,可以由乙烯得到有机高分子材料、药物等成千上万种有用的物质。如图是一套实验室制取乙烯并验证乙烯具有还原性的实验装置。
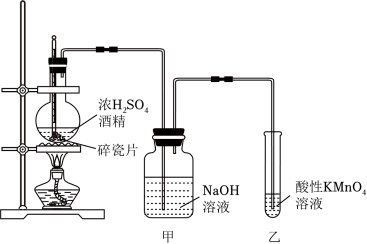
(7)圆底烧瓶中除了主反应外还会发生副反应,请写出副反应的产物
(8)能够说明乙烯具有还原性的现象是
(9)实验时烧瓶中液体混合物逐渐变黑,装置甲的作用是
(10)能鉴别的同时除去甲烷中混有的乙烯的试剂是_____。
| A.稀硫酸 | B.溴的四氯化碳溶液 |
| C.水 | D.酸性高锰酸钾溶液 |
(11)下列物质不可能是乙烯的加成产物的是______。
| A.CH3CH3 | B.CH3CH2OH |
| C.CH3CH2Br | D.CH3CHBr2 |
(12)乙烯是一种重要的化工原料,下列关于乙烯的说法不正确的是______。
| A.乙烯能使溴的四氯化碳溶液褪色 | B.乙烯是一种植物生长调节剂,可用作水果的催熟剂 |
| C.乙烯属于饱和烃,能发生加成反应 | D.乙烯能使高锰酸钾的酸性溶液褪色 |
(13)下列对于乙烯(CH2=CH2)和聚乙烯
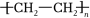 的说法错误的是_____。
的说法错误的是_____。| A.乙烯是纯净物,聚乙烯是混合物 | B.乙烯的性质与聚乙烯相同 |
| C.乙烯是聚乙烯的原料 | D.乙烯可使溴水褪色,聚乙烯则不能 |
您最近一年使用:0次
9 . 醇和酚在人类生产和生活中扮演着重要的角色。回答下列问题:苯肾上腺素是一种抗休克的血管活性药,其结构简式如图所示:___________ (填字母)。
a.可与烧碱溶液反应 b.可与氢气发生加成反应
c.可与酸性高锰酸钾溶液反应 d.可与碳酸氢钠溶液反应放出二氧化碳
(2)下列物质既能发生消去反应,又能氧化成醛的是___________。
(3)以下为有机物的制备实验装置。下列相关说法错误的是___________。
(4)某一元醛(非甲醛)发生银镜反应,最多生成金属银4.32g,等质量的该醛完全燃烧生成水1.08g,则此醛可能是___________。
(5)膳食纤维具有突出的保健功能,是人体的“第七营养素”。木质素是一种非糖类膳食纤维,其单体之一是芥子醇,结构简式如图所示。下列有关芥子醇的说法正确的是_____。
(6)龙脑烯醛是合成檀香系列香料的中间体,其结构简式为 ,下列关于检验该物质官能团的试剂和顺序正确的是___________。
,下列关于检验该物质官能团的试剂和顺序正确的是___________。
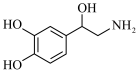
a.可与烧碱溶液反应 b.可与氢气发生加成反应
c.可与酸性高锰酸钾溶液反应 d.可与碳酸氢钠溶液反应放出二氧化碳
(2)下列物质既能发生消去反应,又能氧化成醛的是___________。
A. | B. |
C.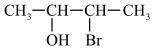 | D.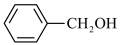 |
(3)以下为有机物的制备实验装置。下列相关说法错误的是___________。
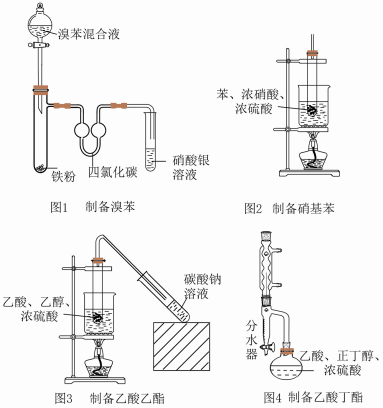
| A.图1右侧试管中观察到淡黄色沉淀,可证明制备溴苯的反应为取代反应 |
B.图2所制得的硝基苯因溶解有 略带黄色,可加入 略带黄色,可加入 溶液过滤除去 溶液过滤除去 |
C.图3导气管口应在右侧试管中 溶液液面上方,以防止倒吸 溶液液面上方,以防止倒吸 |
| D.图4球形冷凝管可冷凝回流提高产率,分水器分出生成的水可提高反应转化率 |
(4)某一元醛(非甲醛)发生银镜反应,最多生成金属银4.32g,等质量的该醛完全燃烧生成水1.08g,则此醛可能是___________。
| A.乙醛 | B.丙烯醛( ) ) |
C.丁醛(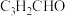 ) ) | D.丁烯醛( ) ) |
(5)膳食纤维具有突出的保健功能,是人体的“第七营养素”。木质素是一种非糖类膳食纤维,其单体之一是芥子醇,结构简式如图所示。下列有关芥子醇的说法正确的是_____。
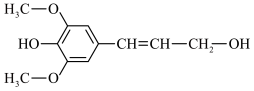
A.芥子醇的分子式是 ,属于芳香烃 ,属于芳香烃 |
B.芥子醇不能与 溶液发生显色反应 溶液发生显色反应 |
C.1mol芥子醇与足量浓溴水反应,最多消耗 |
| D.芥子醇能发生的反应类型有氧化反应、取代反应、加成反应 |
(6)龙脑烯醛是合成檀香系列香料的中间体,其结构简式为
 ,下列关于检验该物质官能团的试剂和顺序正确的是___________。
,下列关于检验该物质官能团的试剂和顺序正确的是___________。| A.先加入溴水;后加入银氨溶液,水浴加热 |
| B.先加入新制氢氧化铜悬浊液,加热;酸化后再加入溴水 |
| C.先加入溴水;后加入酸性高锰酸钾溶液 |
| D.先加入银氨溶液;再另取该物质加入溴水 |
您最近一年使用:0次
名校
10 . 盐碱地是土壤表层集聚过多盐碱成分,对农作物有害的土地。回答下列问题:
(1)盐碱地(含较多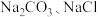 )不利于植物生长,盐碱地呈碱性的原因为
)不利于植物生长,盐碱地呈碱性的原因为___________ (用离子方程式说明);已知 时,
时, 的
的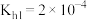 ,则当
,则当 溶液中
溶液中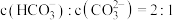 时,溶液的
时,溶液的
___________ 。
(2) 是农作物生长过程中不可缺少的微量元素。常用的铜肥是胆矾,在盐碱地施用胆矾时宜将其溶液
是农作物生长过程中不可缺少的微量元素。常用的铜肥是胆矾,在盐碱地施用胆矾时宜将其溶液___________ (填“喷在叶片上”或“随水灌入土壤中”),主要理由是___________ 。
(3)已知:常温下,碳酸的电离平衡常数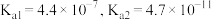 。常温下,向
。常温下,向 溶液中缓慢滴加
溶液中缓慢滴加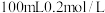 盐酸,溶液中各离子的物质的量随加入盐酸的物质的量的变化如图所示(
盐酸,溶液中各离子的物质的量随加入盐酸的物质的量的变化如图所示( 和
和 未画出)。根据图回答下列问题:
未画出)。根据图回答下列问题:
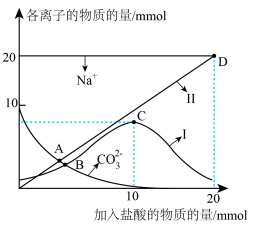
①曲线Ⅰ代表的离子是_______ 。
②A、B两点水的电离程度大小为A_______ B。
③根据上图,下列有关说法不正确的是_______ 。
a.滴加至 点时,
点时,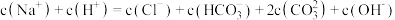
b.滴加至 点时,
点时,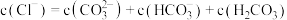
c.滴加至 点时,溶液
点时,溶液
④已知 电离平衡常数约为
电离平衡常数约为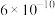 ,用一个离子方程式说明
,用一个离子方程式说明 和
和 结合
结合 能力的相对强弱
能力的相对强弱_______ 。
⑤证明 是弱电解质,你的设计方案是
是弱电解质,你的设计方案是_______ 。
(1)盐碱地(含较多
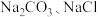 )不利于植物生长,盐碱地呈碱性的原因为
)不利于植物生长,盐碱地呈碱性的原因为 时,
时, 的
的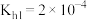 ,则当
,则当 溶液中
溶液中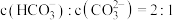 时,溶液的
时,溶液的
(2)
 是农作物生长过程中不可缺少的微量元素。常用的铜肥是胆矾,在盐碱地施用胆矾时宜将其溶液
是农作物生长过程中不可缺少的微量元素。常用的铜肥是胆矾,在盐碱地施用胆矾时宜将其溶液(3)已知:常温下,碳酸的电离平衡常数
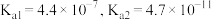 。常温下,向
。常温下,向 溶液中缓慢滴加
溶液中缓慢滴加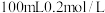 盐酸,溶液中各离子的物质的量随加入盐酸的物质的量的变化如图所示(
盐酸,溶液中各离子的物质的量随加入盐酸的物质的量的变化如图所示( 和
和 未画出)。根据图回答下列问题:
未画出)。根据图回答下列问题:
①曲线Ⅰ代表的离子是
②A、B两点水的电离程度大小为A
③根据上图,下列有关说法不正确的是
a.滴加至
 点时,
点时,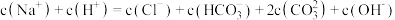
b.滴加至
 点时,
点时,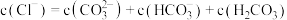
c.滴加至
 点时,溶液
点时,溶液
④已知
 电离平衡常数约为
电离平衡常数约为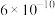 ,用一个离子方程式说明
,用一个离子方程式说明 和
和 结合
结合 能力的相对强弱
能力的相对强弱⑤证明
 是弱电解质,你的设计方案是
是弱电解质,你的设计方案是
您最近一年使用:0次
2023-12-13更新
|
65次组卷
|
2卷引用:广东省佛山市H7教育共同体2023-2024学年高二上学期联考化学试题