完成下列问题
(1)下列变化过程中有可能不涉及氧化还原反应的是_______
(2)氮元素在地球上含量丰富,氮及其化合物在工农业生产、生活中有着重要作用。下列叙述与氮元素的循环无关的是____
(3)关于新制饱和氯水,下列叙述正确的是_______
(4)下列实验中,能实现不同价态含硫物质的转化的是_______
(5)据文献报道,我国学者提出O2氧化HBr生成Br2的反应历程如图所示。下列有关该历程的说法错误的是_____

(6)高锰酸钾是生活中常用的一种消毒剂,也常被用于物质成分分析。二氧化锰是制取高锰酸钾的重要原料。制取高锰酸钾的方法是先用二氧化锰制取锰酸钾(K2MnO4),再转化为高锰酸钾。反应过程如下:
i.______MnO2+________KOH+____KClO3 ____K2MnO4+____KCl+____H2O
____K2MnO4+____KCl+____H2O
ii.3K2MnO4+4HCl=2KMnO4+4KCl+2H2O+MnO2
①下列反应中二氧化锰做氧化剂的是___________
a.实验室用氯酸钾和二氧化锰的混合物加热制取氧气
b.实验室用二氧化锰和浓盐酸混合加热制取氯气
c.用二氧化锰和铝混合发生铝热反应制取锰
d.用二氧化锰、氢氧化钾、氯酸钾共熔制取锰酸钾(K2MnO4)
②设计实验证明二氧化锰中含有哪种类型的化学键。(写出实验步骤、现象和结论)_________
③配平反应i的化学方程式_________ 。
④标出反应ii中电子转移的方向和数目_________ 。
⑤若工业上使用纯度为87%的软锰矿(主要成分为二氧化锰)制取高锰酸钾,理论上10吨软锰矿可制取高锰酸钾___________ 吨。
(1)下列变化过程中有可能不涉及氧化还原反应的是_______
| A.钝化 | B.漂白 | C.固氮 | D.燃烧 |
(2)氮元素在地球上含量丰富,氮及其化合物在工农业生产、生活中有着重要作用。下列叙述与氮元素的循环无关的是____
| A.工业合成氨的过程是固氮的过程 |
| B.自然界中,氨是动物体特别是蛋白质腐败后的产物 |
| C.为防止粮食、罐头、水果等食品腐烂,常用氮气作保护气 |
| D.在雷鸣的雨天,N2与O2会发生反应并最终转化为硝酸盐被植物吸收 |
(3)关于新制饱和氯水,下列叙述正确的是_______
| A.加入适量NaOH,溶液黄绿色褪去,说明氯水中含有Cl2分子 |
| B.加入少量NaCl粉末,溶液漂白性增强 |
| C.加入少量的碳酸钠粉末,pH增大,溶液漂白性一定减弱 |
| D.光照过程中,有气泡冒出,溶液的导电性减弱 |
(4)下列实验中,能实现不同价态含硫物质的转化的是_______
| A.向含足量NaOH的Na2S溶液中加入Na2SO3 |
| B.常温下,向试管中加入1mL浓硫酸和一小块铜片 |
| C.将0.5g硫粉和1.0g铁粉均匀混合,在石棉网上用红热玻璃棒触及粉末一端至粉末红热 |
| D.向Na2SO3固体中加入70%的浓硫酸制备SO2 |
(5)据文献报道,我国学者提出O2氧化HBr生成Br2的反应历程如图所示。下列有关该历程的说法错误的是_____

| A.O2氧化HBr生成Br2的总反应为:O2+4HBr=2Br2+2H2O |
| B.中间体HOOBr和HOBr中Br的化合价相同 |
| C.发生步骤②时,断裂的化学键既有极性键又有非极性键 |
| D.步骤③中,每生成1molBr2转移2mol电子 |
(6)高锰酸钾是生活中常用的一种消毒剂,也常被用于物质成分分析。二氧化锰是制取高锰酸钾的重要原料。制取高锰酸钾的方法是先用二氧化锰制取锰酸钾(K2MnO4),再转化为高锰酸钾。反应过程如下:
i.______MnO2+________KOH+____KClO3
 ____K2MnO4+____KCl+____H2O
____K2MnO4+____KCl+____H2Oii.3K2MnO4+4HCl=2KMnO4+4KCl+2H2O+MnO2
①下列反应中二氧化锰做氧化剂的是
a.实验室用氯酸钾和二氧化锰的混合物加热制取氧气
b.实验室用二氧化锰和浓盐酸混合加热制取氯气
c.用二氧化锰和铝混合发生铝热反应制取锰
d.用二氧化锰、氢氧化钾、氯酸钾共熔制取锰酸钾(K2MnO4)
②设计实验证明二氧化锰中含有哪种类型的化学键。(写出实验步骤、现象和结论)
③配平反应i的化学方程式
④标出反应ii中电子转移的方向和数目
⑤若工业上使用纯度为87%的软锰矿(主要成分为二氧化锰)制取高锰酸钾,理论上10吨软锰矿可制取高锰酸钾
更新时间:2024-02-02 21:20:37
|
相似题推荐
【推荐1】氧化还原反应是中学化学的重要内容。回答下列问题:
(1)野外,一般用铝热反应来焊接铁轨,其化学方程式为 。该反应中氧化剂为
。该反应中氧化剂为_______ ,还原产物为_______ 。
(2)用单线桥法表示电子转移的方向和数目:________
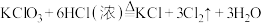
被氧化和被还原的氯原子的个数之比为_______ 。
(3)高铁酸钠是一种新型的绿色消毒剂,主要用于饮用水处理,其中一种制备方法如下,配平该离子方程式:__________
_______ _______
_______ _______
_______ _______
_______ _______
_______ _______
_______
(1)野外,一般用铝热反应来焊接铁轨,其化学方程式为
 。该反应中氧化剂为
。该反应中氧化剂为(2)用单线桥法表示电子转移的方向和数目:
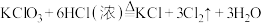
被氧化和被还原的氯原子的个数之比为
(3)高铁酸钠是一种新型的绿色消毒剂,主要用于饮用水处理,其中一种制备方法如下,配平该离子方程式:
_______
 _______
_______ _______
_______ _______
_______ _______
_______ _______
_______
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】回答下列问题:
(1)用金属钠制取氧化钠通常利用以下反应:2NaNO3+10Na 6Na2O+N2↑。试说明不用金属钠与氧气的反应而采用此反应的理由:
6Na2O+N2↑。试说明不用金属钠与氧气的反应而采用此反应的理由:______ 。此反应的氧化剂:______ ;氧化产物:______ 。
(2)利用图所示装置及药品制取氨气。
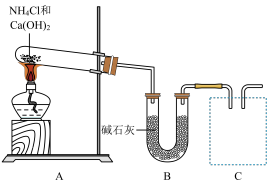
①A中制氨气的化学方程式是______ 。
②B中碱石灰的作用是______ 。
③C处是用集气瓶收集氨气的装置,请绘出装置图(在虚线内画出)______ 。
④证明氨气已集满的方法是______ 。
(1)用金属钠制取氧化钠通常利用以下反应:2NaNO3+10Na
 6Na2O+N2↑。试说明不用金属钠与氧气的反应而采用此反应的理由:
6Na2O+N2↑。试说明不用金属钠与氧气的反应而采用此反应的理由:(2)利用图所示装置及药品制取氨气。

①A中制氨气的化学方程式是
②B中碱石灰的作用是
③C处是用集气瓶收集氨气的装置,请绘出装置图(在虚线内画出)
④证明氨气已集满的方法是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】用化学符号表示:
(1)常温下密度最小的气体为_______ ;
(2)地壳中含量最多的元素为_______ ,空气中含量最多的元素为_________ ;
(3)写出地壳中含量最多的金属元素,并表明其在化合物中的化合价__________ 。
(1)常温下密度最小的气体为
(2)地壳中含量最多的元素为
(3)写出地壳中含量最多的金属元素,并表明其在化合物中的化合价
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】氮气、氧气、氦气、水蒸气和二氧化碳都是空气的成分.请用化学式填写:
(1)能用于抢救病人,供给呼吸的气体是____ ;
(2)空气中含量升高会引起温室效应的气体是____ ;
(3)占空气体积78%,常用作焊接金属保护气的是____ ;
(4)性质很稳定,可用于填充探空气球或飞艇的气体是____ ;
(5)炎热的夏季从冰箱拿出的饮料瓶外壁上会凝结一层小液滴,说明空气中含有____ .
(1)能用于抢救病人,供给呼吸的气体是
(2)空气中含量升高会引起温室效应的气体是
(3)占空气体积78%,常用作焊接金属保护气的是
(4)性质很稳定,可用于填充探空气球或飞艇的气体是
(5)炎热的夏季从冰箱拿出的饮料瓶外壁上会凝结一层小液滴,说明空气中含有
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】工业上硝酸的制备和自然界中硝酸的生成既有相同之处,又有区别。图中路线a、b、c是工业制备硝酸的主要途径,路线Ⅰ、Ⅱ、Ⅲ是雷电固氮过程中生成硝酸的途径。
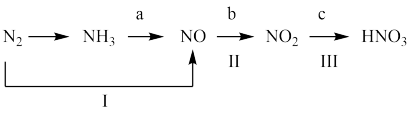
(1)写出N2的—种用途:__________ 。
(2)实验室制取NH3的化学方程式为______ 。
(3)写出工业制硝酸中c过程中反应的化学方程式:______ 。
(4)硝酸是一种具有强氧化性、腐蚀性的强酸,其还原产物因硝酸溶液浓度的不同而有变化。浓硝酸的还原产物主要为NO2,稀硝酸的还原产物主要为NO。实验室中,常用Cu与浓HNO3反应制取NO2,用Cu与稀HNO3反应制取NO。
①请写出实验室中用Cu与浓HNO3反应制取NO2的化学方程式:_____ 。该反应中发生氧化反应的物质是_____ 。
②64.0gCu与适量的浓HNO3反应,铜全部溶解后,共收集到1mol NO2和NO的混合气体,反应中消耗HNO3的物质的量是____ (填标号)。
A.1.5mol B.2.0mol C.2.5mol D.3.0mol
③实际上HNO3不仅可被还原为NO2或NO,浓度更稀时HNO3还可以被还原为N2O、N2、NH4NO3等。请将3种物质: 、
、 和
和 分别填入下面对应的横线上,组成一个未配平的化学方程式并配平其对应的离子方程式。
分别填入下面对应的横线上,组成一个未配平的化学方程式并配平其对应的离子方程式。
i.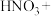
____ 
___ 
___ 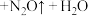
ii.
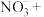

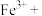
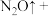

_______________ 。

(1)写出N2的—种用途:
(2)实验室制取NH3的化学方程式为
(3)写出工业制硝酸中c过程中反应的化学方程式:
(4)硝酸是一种具有强氧化性、腐蚀性的强酸,其还原产物因硝酸溶液浓度的不同而有变化。浓硝酸的还原产物主要为NO2,稀硝酸的还原产物主要为NO。实验室中,常用Cu与浓HNO3反应制取NO2,用Cu与稀HNO3反应制取NO。
①请写出实验室中用Cu与浓HNO3反应制取NO2的化学方程式:
②64.0gCu与适量的浓HNO3反应,铜全部溶解后,共收集到1mol NO2和NO的混合气体,反应中消耗HNO3的物质的量是
A.1.5mol B.2.0mol C.2.5mol D.3.0mol
③实际上HNO3不仅可被还原为NO2或NO,浓度更稀时HNO3还可以被还原为N2O、N2、NH4NO3等。请将3种物质:
 、
、 和
和 分别填入下面对应的横线上,组成一个未配平的化学方程式并配平其对应的离子方程式。
分别填入下面对应的横线上,组成一个未配平的化学方程式并配平其对应的离子方程式。i.
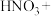


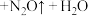
ii.

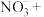

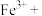
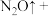

您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】回答下列问题:
(1)用电子式表示下列化合物的形成过程:
HClO :_______ ,MgCl2:_______ 。
(2)有以下物质:①AlCl3 ②HClO ③H2O ④NH4Cl ⑤NaCl ⑥Na2O2 ⑦H2 ⑧H2O2 ⑨NaOH
只含有极性键的是_______ ;只含有非极性键的是_______ ;既含有极性键的是又含有非极性键的是_______ ;只含离子键的是_______ ;⑥含有什么键_______ ;属于离子化合物的是_______ ;属于共价化合物的是_______ 。
(1)用电子式表示下列化合物的形成过程:
HClO :
(2)有以下物质:①AlCl3 ②HClO ③H2O ④NH4Cl ⑤NaCl ⑥Na2O2 ⑦H2 ⑧H2O2 ⑨NaOH
只含有极性键的是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】Ⅰ.下列物质中:
①N2、②MgCl2、③NH4Cl、 ④ZnSO4、⑤CO2、⑥HClO4、⑦KOH、⑧H3PO4(填编号)
(1)属于非电解质的是__ ;属于弱电解质的是___ 。
(2)属于共价化合物的是___ ;不含有共价键的离子化合物是__ 。
(3)既含有离子键又含有共价键的是__ 。
Ⅱ.写出化学方程式或离子方程式:
(1)氢氧化钠和盐酸反应的离子方程式____ 。
(2)Na和水反应的化学方程式_____ 。
(3)氢气和氯气(光照)反应的化学方程式____ 。
①N2、②MgCl2、③NH4Cl、 ④ZnSO4、⑤CO2、⑥HClO4、⑦KOH、⑧H3PO4(填编号)
(1)属于非电解质的是
(2)属于共价化合物的是
(3)既含有离子键又含有共价键的是
Ⅱ.写出化学方程式或离子方程式:
(1)氢氧化钠和盐酸反应的离子方程式
(2)Na和水反应的化学方程式
(3)氢气和氯气(光照)反应的化学方程式
您最近一年使用:0次
填空题
|
较易
(0.85)
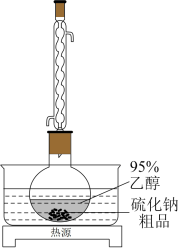
【推荐1】硫化钠可广泛用于染料、医药行业。工业生产的硫化钠粗品中常含有一定量的煤灰及重金属硫化物等杂质。硫化钠易溶于热乙醇,重金属硫化物难溶于乙醇。实验室中常用95%乙醇重结晶纯化硫化钠粗品。回答下列问题:_______ 。回流结束后,需进行的操作有①停止加热②关闭冷凝水③移去水浴,正确的顺序为_______ (填标号)。
A.①②③B.③①②C.②①③D.①③②
A.①②③B.③①②C.②①③D.①③②
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】按要求填空:
(1)①石墨 ②盐酸 ③胆矾 ④KOH固体 ⑤Fe ⑥氨水 ⑦乙醇 ⑧冰醋酸 ⑨干冰 ⑩熔融BaSO4
能导电的是________________________ ,电解质是_______________________ ,非电解质是________________________ ;
(2)KIO3 + 5KI + 3H2SO4 == 3K2SO4 + 3I2 + 3H2O的反应中氧化产物和还原产物的物质的量之比是__________________ ;
(3)铁是应用最广的金属,铁的卤化物、氧化物以及高价铁的含氧酸盐为重要的化合物。高铁酸钾(K2FeO4)是一种强氧化剂,可作为水处理剂和高容量电池材料。FeCl3和KClO在强碱条件下反应制取K2FeO4,其反应的离子方程式为____________________________________
(1)①石墨 ②盐酸 ③胆矾 ④KOH固体 ⑤Fe ⑥氨水 ⑦乙醇 ⑧冰醋酸 ⑨干冰 ⑩熔融BaSO4
能导电的是
(2)KIO3 + 5KI + 3H2SO4 == 3K2SO4 + 3I2 + 3H2O的反应中氧化产物和还原产物的物质的量之比是
(3)铁是应用最广的金属,铁的卤化物、氧化物以及高价铁的含氧酸盐为重要的化合物。高铁酸钾(K2FeO4)是一种强氧化剂,可作为水处理剂和高容量电池材料。FeCl3和KClO在强碱条件下反应制取K2FeO4,其反应的离子方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】牙膏中的摩擦剂碳酸钙可以用石灰石来制备,甲同学和乙同学分别设计了一种在实验室制备碳酸钙的实验方案。
甲同学设计的实验方案:石灰石 生石灰
生石灰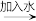 熟石灰
熟石灰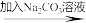 碳酸钙。
碳酸钙。
乙同学设计的实验方案:石灰石 氯化钙
氯化钙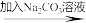 碳酸钙。
碳酸钙。
回答下列问题:
(1)生石灰与氯化钙均可用作食品的干燥剂。
①生石灰能用作食品干燥剂的原理为___________ (用化学方程式表示)。
②氯化钙在水中的电离方程式为___________ 。
(2)熟石灰与碳酸钠溶液发生反应的化学方程式为___________ 。
(3)熟石灰和碳酸钙常用作建筑材料。
①工业上常采用煅烧碳酸钙的方法来制备 ,发生反应的化学方程式为
,发生反应的化学方程式为___________ 。
②若将 通入冷的熟石灰
通入冷的熟石灰 中,可制得漂白粉,漂白粉的有效成分为
中,可制得漂白粉,漂白粉的有效成分为___________ (填化学式),漂白粉久置于空气中容易变质,其原因为___________ 和 (用化学方程式表示)。
(用化学方程式表示)。
(4)将少量的稀盐酸加入碳酸钠溶液中,发生反应的离子方程式为___________ 。
甲同学设计的实验方案:石灰石
 生石灰
生石灰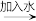 熟石灰
熟石灰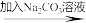 碳酸钙。
碳酸钙。乙同学设计的实验方案:石灰石
 氯化钙
氯化钙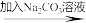 碳酸钙。
碳酸钙。回答下列问题:
(1)生石灰与氯化钙均可用作食品的干燥剂。
①生石灰能用作食品干燥剂的原理为
②氯化钙在水中的电离方程式为
(2)熟石灰与碳酸钠溶液发生反应的化学方程式为
(3)熟石灰和碳酸钙常用作建筑材料。
①工业上常采用煅烧碳酸钙的方法来制备
 ,发生反应的化学方程式为
,发生反应的化学方程式为②若将
 通入冷的熟石灰
通入冷的熟石灰 中,可制得漂白粉,漂白粉的有效成分为
中,可制得漂白粉,漂白粉的有效成分为 (用化学方程式表示)。
(用化学方程式表示)。(4)将少量的稀盐酸加入碳酸钠溶液中,发生反应的离子方程式为
您最近一年使用:0次



