工业上硝酸的制备和自然界中硝酸的生成既有相同之处,又有区别。图中路线a、b、c是工业制备硝酸的主要途径,路线Ⅰ、Ⅱ、Ⅲ是雷电固氮过程中生成硝酸的途径。
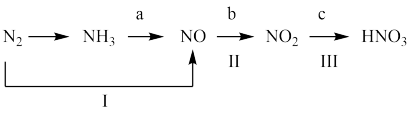
(1)写出N2的—种用途:__________ 。
(2)实验室制取NH3的化学方程式为______ 。
(3)写出工业制硝酸中c过程中反应的化学方程式:______ 。
(4)硝酸是一种具有强氧化性、腐蚀性的强酸,其还原产物因硝酸溶液浓度的不同而有变化。浓硝酸的还原产物主要为NO2,稀硝酸的还原产物主要为NO。实验室中,常用Cu与浓HNO3反应制取NO2,用Cu与稀HNO3反应制取NO。
①请写出实验室中用Cu与浓HNO3反应制取NO2的化学方程式:_____ 。该反应中发生氧化反应的物质是_____ 。
②64.0gCu与适量的浓HNO3反应,铜全部溶解后,共收集到1mol NO2和NO的混合气体,反应中消耗HNO3的物质的量是____ (填标号)。
A.1.5mol B.2.0mol C.2.5mol D.3.0mol
③实际上HNO3不仅可被还原为NO2或NO,浓度更稀时HNO3还可以被还原为N2O、N2、NH4NO3等。请将3种物质: 、
、 和
和 分别填入下面对应的横线上,组成一个未配平的化学方程式并配平其对应的离子方程式。
分别填入下面对应的横线上,组成一个未配平的化学方程式并配平其对应的离子方程式。
i.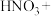
____ 
___ 
___ 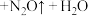
ii.
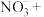

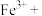
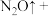

_______________ 。

(1)写出N2的—种用途:
(2)实验室制取NH3的化学方程式为
(3)写出工业制硝酸中c过程中反应的化学方程式:
(4)硝酸是一种具有强氧化性、腐蚀性的强酸,其还原产物因硝酸溶液浓度的不同而有变化。浓硝酸的还原产物主要为NO2,稀硝酸的还原产物主要为NO。实验室中,常用Cu与浓HNO3反应制取NO2,用Cu与稀HNO3反应制取NO。
①请写出实验室中用Cu与浓HNO3反应制取NO2的化学方程式:
②64.0gCu与适量的浓HNO3反应,铜全部溶解后,共收集到1mol NO2和NO的混合气体,反应中消耗HNO3的物质的量是
A.1.5mol B.2.0mol C.2.5mol D.3.0mol
③实际上HNO3不仅可被还原为NO2或NO,浓度更稀时HNO3还可以被还原为N2O、N2、NH4NO3等。请将3种物质:
 、
、 和
和 分别填入下面对应的横线上,组成一个未配平的化学方程式并配平其对应的离子方程式。
分别填入下面对应的横线上,组成一个未配平的化学方程式并配平其对应的离子方程式。i.
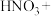


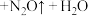
ii.

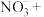

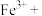
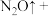

更新时间:2020-09-25 09:41:24
|
相似题推荐
填空题
|
较易
(0.85)
名校
【推荐1】以下为中学化学中常见的几种物质:①Fe ②熔融NaCl ③NaHSO4 ④CO2 ⑤H2SO4 ⑥酒精 ⑦KHCO3溶液 ⑧BaSO4 ⑨NaOH请回答下面问题.
(1)属于电解质的是(填序号)_____________ .属于酸的是_______ .属于盐的是:_______ .
(2)写出⑤的电离方程式:_______________________ .
(3)⑦与⑨发生反应的离子方程式为________________ .
(4)上述物质中有两种物质之间可发生氧化还原反应,该反应的化学反应方程式为____ .还原剂为_____________
(1)属于电解质的是(填序号)
(2)写出⑤的电离方程式:
(3)⑦与⑨发生反应的离子方程式为
(4)上述物质中有两种物质之间可发生氧化还原反应,该反应的化学反应方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】氨的催化氧化是工业上制硝酸的基础反应:4NH3+xO2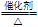 4NO+6H2O。
4NO+6H2O。
回答下列问题:
(1)该化学方程式中x的数值是_______ 。
(2)作为还原剂的物质是(填化学式)__________ 。
(3)若反应中生成了4 mol一氧化氮,则消耗氨的物质的量是________ 。
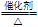 4NO+6H2O。
4NO+6H2O。回答下列问题:
(1)该化学方程式中x的数值是
(2)作为还原剂的物质是(填化学式)
(3)若反应中生成了4 mol一氧化氮,则消耗氨的物质的量是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】(1)常作食盐中补碘剂的含氧酸盐的化学名称___________ 。
(2)“芒硝”可作为中药药材,主要治疗热积便秘、腹满胀痛、目赤、口疮等病症,其化学式为________ 。
(3)写出炼铁高炉中生成炉渣的化学方程式_____________ 。
(4)镁与氧化硼( )可发生类似“铝热反应”的反应,写出该反应的化学方程式
)可发生类似“铝热反应”的反应,写出该反应的化学方程式_________ 。
(5) 可作为
可作为 水溶液中硫元素发生自身氧化还原反应的催化剂,其催化经历了ⅰ和ⅱ两个过程。ⅰ的离子方程式为
水溶液中硫元素发生自身氧化还原反应的催化剂,其催化经历了ⅰ和ⅱ两个过程。ⅰ的离子方程式为______________ 。
ⅰ.……=……
ⅱ.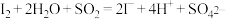
(2)“芒硝”可作为中药药材,主要治疗热积便秘、腹满胀痛、目赤、口疮等病症,其化学式为
(3)写出炼铁高炉中生成炉渣的化学方程式
(4)镁与氧化硼(
 )可发生类似“铝热反应”的反应,写出该反应的化学方程式
)可发生类似“铝热反应”的反应,写出该反应的化学方程式(5)
 可作为
可作为 水溶液中硫元素发生自身氧化还原反应的催化剂,其催化经历了ⅰ和ⅱ两个过程。ⅰ的离子方程式为
水溶液中硫元素发生自身氧化还原反应的催化剂,其催化经历了ⅰ和ⅱ两个过程。ⅰ的离子方程式为ⅰ.……=……
ⅱ.
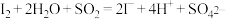
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】盐酸、硫酸和硝酸是中学阶段常见的“三大酸”。现就三大酸与金属铜反应的情况,回答下列问题:
(1)稀盐酸不与Cu反应,若在稀盐酸中加入H2O2(常见氧化剂,作氧化剂时还原产物为水)后,则可使铜顺利溶解,溶液呈现蓝色。则该反应的离子反应方程式为_______
(2)在100mL 18.4 mol∙L−1浓硫酸中加入过量铜片,加热使之反应。
①写出发生反应的化学方程式_______ 。
②生成的气体在标准状况下的实际体积为_______ (填序号) 。
a.等于20.61L b.大于20.61L c.小于20.61L
③若使剩余的铜片继续溶解,可在其中加入硝酸盐溶液(如KNO3溶液),则该反应的离子方程式为_______ 。
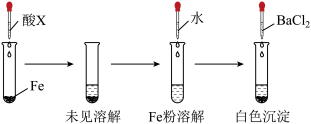
(3)根据如图操作及现象推断酸X为_______ (填序号)
a.浓盐酸 b.浓硫酸 c.浓硝酸
(1)稀盐酸不与Cu反应,若在稀盐酸中加入H2O2(常见氧化剂,作氧化剂时还原产物为水)后,则可使铜顺利溶解,溶液呈现蓝色。则该反应的离子反应方程式为
(2)在100mL 18.4 mol∙L−1浓硫酸中加入过量铜片,加热使之反应。
①写出发生反应的化学方程式
②生成的气体在标准状况下的实际体积为
a.等于20.61L b.大于20.61L c.小于20.61L
③若使剩余的铜片继续溶解,可在其中加入硝酸盐溶液(如KNO3溶液),则该反应的离子方程式为
(3)根据如图操作及现象推断酸X为
a.浓盐酸 b.浓硫酸 c.浓硝酸

您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
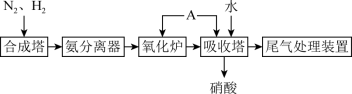
【推荐2】氨既是一种重要的化工产品,又是一种重要的化工原料。下图为合成氨以及氨氧化制硝酸的流程示意:___________ (填“放热”或“吸热”)反应。
(2)从合成气中分离出氨,主要利用了氨气___________ 的性质;从氨分离器中分离出的另两种气体可回到___________ (填写装置名称)中再利用。
(3)请写出氧化炉内发生反应的化学方程式___________ 。
(4)向吸收塔中通入过量A是___________ ,作用是___________ 。
(5)硝酸可氧化绝大多数金属,而工业上盛装大量浓硝酸可用铝制容器,原因是___________ 。
(6)①可利用浓氨水检验氯气管道是否泄漏,若泄漏,可观察到的现象___________ 。
②碳酸氢铵是一种常用氮肥,但因___________ (用化学方程式表达),所以必须放置阴凉处保存。
(2)从合成气中分离出氨,主要利用了氨气
(3)请写出氧化炉内发生反应的化学方程式
(4)向吸收塔中通入过量A是
(5)硝酸可氧化绝大多数金属,而工业上盛装大量浓硝酸可用铝制容器,原因是
(6)①可利用浓氨水检验氯气管道是否泄漏,若泄漏,可观察到的现象
②碳酸氢铵是一种常用氮肥,但因
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】“价-类”二维图是学习元素化合物性质的重要方法,利用所学知识能更好的了解氮的循环。

(1)I.“价-类”二维图中A的类别为___________ ; 丙为钠盐,其化学式为___________ 。
(2)甲为常见的碱性气体,是制造氮肥、炸药等物质的化工原料。实验室制备甲的化学方程式为___________ 。
(3)用以下物质研究乙的性质,预测能与乙发生反应的物质为___________(填标号)。
(4)丁主要用于染料、医药、印染、漂白等方面,且丁的焰色反应呈黄色。丁在酸性条件下,与KI按物质的量1∶1恰好完全反应,且生成能使淀粉变蓝的物质,则产物中含氮元素物质的化学式为___________ 。
II.海洋生物参与氮循环过程如图所示(其它含氮物质不参与反应)。
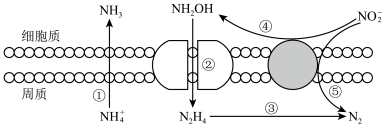
(5)以上六种含氮微粒中,一共呈现了氮元素的___________ 种价态。
(6)反应③和⑤中,若生成等量的N2,则转移的电子数之比为___________ 。

(1)I.“价-类”二维图中A的类别为
(2)甲为常见的碱性气体,是制造氮肥、炸药等物质的化工原料。实验室制备甲的化学方程式为
(3)用以下物质研究乙的性质,预测能与乙发生反应的物质为___________(填标号)。
| A.Na2SO4 | B.Mg | C.CO2 | D.NH3·H2O |
II.海洋生物参与氮循环过程如图所示(其它含氮物质不参与反应)。

(5)以上六种含氮微粒中,一共呈现了氮元素的
(6)反应③和⑤中,若生成等量的N2,则转移的电子数之比为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】氮元素是生命的基础,自然界中氮的循环过程如下图所示,请分析此图并回答有关问题。
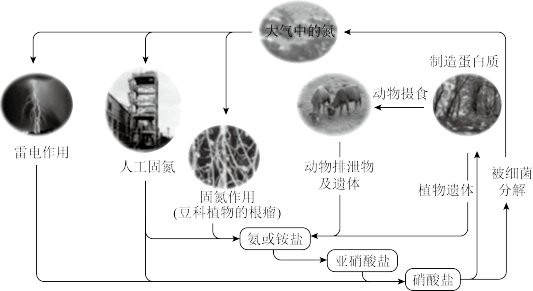
(1)大气中的氮以_______ (填化学式)形式存在。图中共表示了_______ 种固氮的途径。
(2)含氮量是衡量氮肥肥效的指标之一。现有三种氮肥:CO(NH2)2(尿素)、NH4NO3和(NH4)2SO4,其中肥效最高的是_______ (填化学式)。
(3)农谚说:“雷雨发庄稼”。原因是雷电时实现了氮的固定,为植物提供_______ 态氮肥。若某地某次雷电时产生了200mol的NO,假设其全部转化为氮肥,则此次雷电相当于给土壤施加了_______ 千克尿素。
(4)氨的含氮量比尿素更高,但氨却很少直接施加在土壤中作为肥料,试分析可能的原因是_______ 。(写出一条即可)

(1)大气中的氮以
(2)含氮量是衡量氮肥肥效的指标之一。现有三种氮肥:CO(NH2)2(尿素)、NH4NO3和(NH4)2SO4,其中肥效最高的是
(3)农谚说:“雷雨发庄稼”。原因是雷电时实现了氮的固定,为植物提供
(4)氨的含氮量比尿素更高,但氨却很少直接施加在土壤中作为肥料,试分析可能的原因是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】在氮的单质和常见的含氮化合物中(用化学式作答):
(1)常用作保护气的物质是_______ ;
(2)常用作制冷剂的物质是_______ ;
(3)能与酸反应生成盐,在常温下为气态的物质是_______ ;它与盐酸等强酸反应的离子方程式是_______ 。
(4)铵盐与NaOH等强碱的溶液在加热条件下反应的离子方程式是______ 。
(1)常用作保护气的物质是
(2)常用作制冷剂的物质是
(3)能与酸反应生成盐,在常温下为气态的物质是
(4)铵盐与NaOH等强碱的溶液在加热条件下反应的离子方程式是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】依据图1中氮元素及其化合物的转化关系,回答问题:


(1)实验室常用NH4Cl与Ca(OH)2制取氨气,该反应的化学方程式为____________ 。
(2)收集氨气的方法是________ 。
(3)下列试剂不能用于干燥NH3的是__________ (填字母)。
A.碱石灰 B.无水CaCl2 C.NaOH固体
(4)工业上以NH3、空气、水为原料生产硝酸分为三步:
①NH3→NO化学方程式为_______________________________ 。
②NO→NO2实验现象是__________________ 。
③NO2 +H2O→HNO3氧化剂与还原剂物质的量之比为_________________ 。
(5)将X转化为HNO3__________ (填“是”或“不是”)氧化还原反应。
(6)若要将NH3→N2,从原理上看,下列试剂可行的是_________ 。
A.O2 B.Na C.NH4Cl D.NO2
(7)标准状况下,将500 L氨气溶于水形成1 L氨水,则此氨水的物质的量浓度为______ mol∙L−1 (保留三位有效数字)。


(1)实验室常用NH4Cl与Ca(OH)2制取氨气,该反应的化学方程式为
(2)收集氨气的方法是
(3)下列试剂不能用于干燥NH3的是
A.碱石灰 B.无水CaCl2 C.NaOH固体
(4)工业上以NH3、空气、水为原料生产硝酸分为三步:
①NH3→NO化学方程式为
②NO→NO2实验现象是
③NO2 +H2O→HNO3氧化剂与还原剂物质的量之比为
(5)将X转化为HNO3
(6)若要将NH3→N2,从原理上看,下列试剂可行的是
A.O2 B.Na C.NH4Cl D.NO2
(7)标准状况下,将500 L氨气溶于水形成1 L氨水,则此氨水的物质的量浓度为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】I.回答下列问题。
(1)下列变化中属于吸热反应的是___________ 。
①铝片与稀盐酸的反应;②将胆矾加热变为白色粉末;③干冰汽化;④甲烷在氧气中的燃烧反应;⑤ 固体溶于水;⑥C与CO2反应生成CO
固体溶于水;⑥C与CO2反应生成CO
(2)反应A+B→C(放热)分两步进行①A+B→X(吸热);②X→C(放热)。下列示意图中,能正确表示总反应过程中能量变化的是___________。
(3)过氧化氢一定条件下可发生分解:2H2O2(l)=2H2O(l)+O2(g),断裂1mol H2O2(l)中的O-O键和1mol O2(g)中的O=O键所需的能量依次为142kJ、497.3kJ,断裂H2O2(l)和H2O(l)中1molH-O键所需能量依次为367 kJ、467 kJ,则2 mol H2O2(l)反应生成2 mol H2O(l)和1mol O2(g)___________ (填“吸收"或“放出”)的能量为___________ kJ。
Ⅱ.氮元素形成的化合物种类十分丰富。请根据以下工业制硝酸的原理示意图回答含氮化合物相关的问题:___________ (填“氧化剂”或“还原剂”)。
(5)写出氧化炉中反应的化学方程式___________ 。
(6)用NaClO溶液吸收硝酸尾气,可提高尾气中NO的去除率。在酸性NaClO溶液中,HClO氧化NO生成 和
和 ,其离子方程式为
,其离子方程式为___________ 。
(1)下列变化中属于吸热反应的是
①铝片与稀盐酸的反应;②将胆矾加热变为白色粉末;③干冰汽化;④甲烷在氧气中的燃烧反应;⑤
 固体溶于水;⑥C与CO2反应生成CO
固体溶于水;⑥C与CO2反应生成CO(2)反应A+B→C(放热)分两步进行①A+B→X(吸热);②X→C(放热)。下列示意图中,能正确表示总反应过程中能量变化的是___________。
A.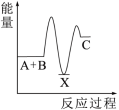 | B.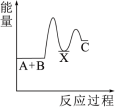 | C.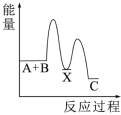 | D.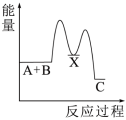 |
(3)过氧化氢一定条件下可发生分解:2H2O2(l)=2H2O(l)+O2(g),断裂1mol H2O2(l)中的O-O键和1mol O2(g)中的O=O键所需的能量依次为142kJ、497.3kJ,断裂H2O2(l)和H2O(l)中1molH-O键所需能量依次为367 kJ、467 kJ,则2 mol H2O2(l)反应生成2 mol H2O(l)和1mol O2(g)
Ⅱ.氮元素形成的化合物种类十分丰富。请根据以下工业制硝酸的原理示意图回答含氮化合物相关的问题:
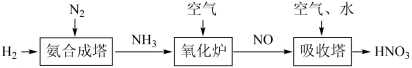
(5)写出氧化炉中反应的化学方程式
(6)用NaClO溶液吸收硝酸尾气,可提高尾气中NO的去除率。在酸性NaClO溶液中,HClO氧化NO生成
 和
和 ,其离子方程式为
,其离子方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】某化学兴趣小组利用下列图示装置探究氨气的性质。

(1)①中湿润的红色石蕊试纸变蓝,说明氨水溶液呈___________ 性,化学方程式为___________ 。
(2)向②中滴入浓盐酸,现象为___________ ,反应的化学方程式为___________ 。
(3)将灼热的铂丝伸入③中锥形瓶,可观察到铂丝保持红热,有红棕色气体及少量白烟生成。该过程会同时发生多个反应,写出NH3和O2催化氧化的化学方程式:___________ ,锥形瓶中出现白烟,该物质的化学式为___________ ,瓶中红棕色气体为___________ (填化学式)。

(1)①中湿润的红色石蕊试纸变蓝,说明氨水溶液呈
(2)向②中滴入浓盐酸,现象为
(3)将灼热的铂丝伸入③中锥形瓶,可观察到铂丝保持红热,有红棕色气体及少量白烟生成。该过程会同时发生多个反应,写出NH3和O2催化氧化的化学方程式:
您最近一年使用:0次




